एमएलएच1
डीएनए असंगत सुधार प्रोटीन एमएलएच1 या म्यूटल प्रोटीन होमोलॉग 1 प्रोटीन है जो मनुष्यों में गुणसूत्र 3 (मानव) पर स्थित एमएलएच1 जीन द्वारा एन्कोड किया जाता है। इस प्रकार कि जीन है जो सामान्यतः वंशानुगत नॉनपोलिपोसिस कोलोरेक्टल कैंसर से जुड़ा होता है। होमोलॉजी (जीव विज्ञान) मानव एमएलएच1 के ऑर्थोलॉजी का अध्ययन माउस और बडिंग यीस्ट 'सैक्रोमाइसेस सेरेविसिया' सहित अन्य जीवों में भी किया गया है।
कार्य
इस जीन की पहचान वंशानुगत नॉनपोलिपोसिस कोलन कैंसर में अधिकांशतः उत्परिवर्तित स्थान के रूप में की गई थी। यह ई. कोलाई डीएनए असंगत सुधार जीन, म्यूटएल का मानव होमोलोग है, जो असंगत पहचान, स्ट्रैंड डिस्क्रिमिनेशन और स्ट्रैंड रिमूवल के समय प्रोटीन-प्रोटीन परस्पर क्रिया की मध्यस्थता करता है। एमएलएच1 में दोष वंशानुगत नॉनपोलिपोसिस कोलन कैंसर में देखी गई माइक्रोसेटेलाइट अस्थिरता से जुड़े हैं। अलग-अलग आइसोफोर्मों को एन्कोडिंग करने वाले वैकल्पिक रूप से स्प्लिस्ड ट्रांसक्रिप्ट वेरिएंट का वर्णन किया गया है, किन्तु उनकी पूर्ण लंबाई निर्धारित नहीं की गई है।[1]
डीएनए असंगत सुधार की भूमिका
एमएलएच1 प्रोटीन सात डीएनए असंगत सुधार प्रोटीन की प्रणाली का घटक है जो मनुष्यों में डीएनए असंगत सुधार कों प्रारंभ करने के लिए अनुक्रमिक चरणों में समन्वित रूप से काम करता है।[2] असंगत सुधार में दोष, लगभग 13% कोलोरेक्टल कैंसर में पाए जाते हैं, अन्य डीएनए असंगत सुधार प्रोटीन की कमियों की तुलना में एमएलएच1 की कमी के कारण अधिक बार होते हैं।[3] मनुष्यों में सात डीएनए असंगत सुधार प्रोटीन एमएलएच1, एमएलएच3, एमएसएच2, एमएसएच3, एमएसएच6, पीएमएस1 और पीएमएस2 हैं।[2] इसके अतिरिक्त एक्सोन्यूक्लिएज 1 1-डिपेंडेंट और एक्सो1-इंडिपेंडेंट डीएनए असंगत सुधार उपमार्ग हैं।[4]
डीएनए असंगत तब होता है जब आधार अनुचित विधि से दूसरे आधार के साथ जोड़ा जाता है, या जहां डीएनए के स्ट्रैंड में छोटा जोड़ या विलोपन होता है जो दूसरे स्ट्रैंड से मेल नहीं खाता है। असंगत सामान्यतः डीएनए प्रतिकृति त्रुटियों के परिणामस्वरूप या आनुवंशिक पुनर्संयोजन के समय होते हैं। उन असंगत को पहचानना और उनकी सुधार करना कोशिकाओं के लिए महत्वपूर्ण है क्योंकि ऐसा करने में विफलता के परिणामस्वरूप माइक्रोसेटेलाइट अस्थिरता और उन्नत सहज उत्परिवर्तन दर (म्यूटेटर फेनोटाइप) होता है। 20 कैंसर का मूल्यांकन किया गया है, संपूर्ण जीनोम अनुक्रमण म्यूटेशन आवृत्ति माइक्रोसैटेलाइट अस्थिर कोलन कैंसर (असंगत सुधार की कमी) में म्यूटेशन की दूसरी उच्चतम आवृत्ति (मेलेनोमा के बाद) थी।
एमएसएच2 और एमएसएच6 के बीच हेटेरोडिमर पहले असंगत को पहचानता है, चूँकि एमएसएच2 और एमएसएच3 के बीच हेटेरोडिमर भी प्रक्रिया प्रारंभ कर सकता है। एमएसएच2-एमएसएच6 हेटेरोडिमर का गठन एमएलएच1 और पीएमएस2 के दूसरे हेटेरोडिमर को समायोजित करता है, चूँकि एमएलएच1 और या तो पीएमएस3 या एमएलएच3 के बीच हेटेरोडिमर पीएमएस2 का स्थानापन्न कर सकता है। हेटेरोडिमर्स के 2 सेटों के बीच बनने वाला यह प्रोटीन जटिल असंगत दोष की सुधार की प्रारंभ को सक्षम बनाता है।[2]
असंगत सुधार में सम्मिलित अन्य जीन उत्पादों (डीएनए असंगत सुधार जीन द्वारा प्रारंभ के बाद) में डीएनए पोलीमरेज़ डेल्टा, प्रोलिफ़ेरेटिंग सेल परमाणु प्रतिजन, प्रतिकृति प्रोटीन ए, एचएमजीबी1, प्रतिकृति कारक सी और एलआईजी1, प्लस हिस्टोन और क्रोमेटिन संशोधित कारक सम्मिलित हैं।[5][6]
कैंसर में दोषयुक्त अभिव्यक्ति
| कैंसर प्रकार | कमी की आवृत्ति में कैंसर | सन्निकट क्षेत्र दोष में कमी की आवृत्ति |
|---|---|---|
| पेट | 32%[7][8] | 24%-28% |
| पेट (फोवोलर प्रकार का ट्यूमर) | 74%[9] | 71% |
| उदर ज्वर में
काश्मीर घाटी |
73%[10] | 20% |
| एसोफेअल | 73%[11] | 27% |
| सिर और गर्दन स्क्वैमस सेल
कैंसर (एचएनएससीसी) |
31%-33%[12][13] | 20%-25% |
| गैर-लघु कोशिका फेफड़े का कैंसर (एनएससीएलसी) | 69%[14] | 72% |
| मलाशय | 10%[3] |
एपिजेनेटिक नियंत्रण
डीएनए की सुधार की कमी वाले विकीर्ण कैंसर के केवल अल्पसंख्यक में डीएनए की सुधार करने वाले जीन में उत्परिवर्तन होता है। चूँकि, डीएनए की सुधार की कमी वाले अधिकांश विकीर्ण कैंसर में एक या एक से अधिक कैंसर एपिजेनेटिक्स परिवर्तन होते हैं जो डीएनए की सुधार जीन अभिव्यक्ति को कम करते हैं।[15] उपरोक्त तालिका में, एमएलएच1 की अधिकांश कमियाँ एमएलएच1 जीन के प्रवर्तक क्षेत्र के मिथाइलेशन के कारण थीं। एमएलएच1 अभिव्यक्ति को कम करने वाला अन्य एपिजेनेटिक तंत्र एमआईआर-155 कैंसर एमआईआर-155 कों प्रदर्शित करती है।[16] एमआईआर-155 लक्ष्य एमएलएच1 और एमएसएच2 और एमआईआर-155 की अभिव्यक्ति और एमएलएच1 या एमएसएच2 प्रोटीन की अभिव्यक्ति के बीच व्युत्क्रम सहसंबंध मानव कोलोरेक्टल कैंसर में पाया जाता है।[16]
क्षेत्र दोषों में कमी
एपिथेलीयम क्षेत्र दोष उपकला का क्षेत्र है जिसे एपिजेनेटिक परिवर्तन और उत्परिवर्तन द्वारा पूर्वनिर्मित किया गया है जिससे इसे कैंसर के विकास की ओर अग्रसर किया जा सकता है। जैसा कि रुबिन द्वारा बताया गया है, कैंसर अनुसंधान में अधिकांश अध्ययन विवो में अच्छी तरह से परिभाषित ट्यूमर या इन विट्रो में असतत नियोप्लास्टिक फॉसी पर किए गए हैं।[17] फिर भी इस बात के प्रमाण हैं कि उत्परिवर्ती फेनोटाइप मानव कोलोरेक्टल ट्यूमर में पाए जाने वाले 80% से अधिक दैहिक उत्परिवर्तन टर्मिनल क्लोनल विस्तार की प्रारंभ से पहले होते हैं।[18] इसी तरह, वोगेलस्टीन एट अल [19] बताते हैं कि ट्यूमर में पहचाने जाने वाले दैहिक उत्परिवर्तन के आधे से अधिक पूर्व-नियोप्लास्टिक चरण ( क्षेत्र दोष में) में, स्पष्ट रूप से सामान्य कोशिकाओं के विकास के समय होते हैं।
ऊपर दी गई तालिका में, अधिकांश कैंसर के आसपास के क्षेत्र दोषों (हिस्टोलॉजिक रूप से सामान्य ऊतक) में एमएलएच1 की कमी देखी गई थी। यदि एमएलएच1 को एपिजेनेटिक रूप से कम कर दिया जाता है, जिससे यह संभवतः स्टेम सेल पर चयनात्मक लाभ प्रदान नहीं करता है। चूँकि, एमएलएच1 की कम या अनुपस्थित अभिव्यक्ति से उत्परिवर्तन की दर में वृद्धि होती है, और एक या अधिक उत्परिवर्तित जीन सेल को चयनात्मक लाभ प्रदान कर सकते हैं। उत्परिवर्तित स्टेम सेल विस्तारित क्लोन उत्पन्न करते समय अभिव्यक्ति-अपूर्ण एमएलएच 1 जीन को चुनिंदा तटस्थ या केवल थोड़ा हानिकारक यात्री (हिच-हाइकर) जीन के रूप में साथ ले जाया जा सकता है। एपिजेनेटिक रूप से असंगत एमएलएच1 के साथ क्लोन की निरंतर उपस्थिति आगे उत्परिवर्तन उत्पन्न करना जारी रखता है, जिनमें कुछ ट्यूमर उत्पन्न कर सकते हैं।
अन्य डीएनए सुधार जीनों के समन्वय में नियंत्रण
कैंसर में, कई डीएनए की सुधार करने वाले जीन अधिकांशतः एक साथ असंगत पाए जाते हैं।[15] उदाहरण में, एमएलएच1, जियांग एट अल को सम्मिलित करना है |[20] एक अध्ययन किया जहां उन्होंने गैर- तारिकाकोशिकार्बुद व्यक्तियों से सामान्य मस्तिष्क के ऊतकों की तुलना में 40 एस्ट्रोसाइटोमास में 27 डीएनए सुधार जीनों की एमआरएनए अभिव्यक्ति का मूल्यांकन किया था। 27 डीएनए सुधार जीन का मूल्यांकन किया गया था, 13 डीएनए सुधार जीन, एमएलएच1, एमएलएच3, O-6-मिथाइलगुआनिन-डीएनए मिथाइलट्रांसफेरेज़, एनटीएचएल1, ओक्सोगुआनिन ग्लाइकोसिलेज़, एसएमयूजी1, ईआरसीसी1, ईआरसीसी2, ईआरसीसी3, ईआरसीसी4, रेड50, डीएनए सुधार प्रोटीन एक्सआरसीसी4 और केयू80 थे। एस्ट्रोसाइटोमास के सभी तीन ग्रेड (II, III और IV) में सभी महत्वपूर्ण रूप से डाउन-रेगुलेटेड हैं। निम्न ग्रेड के साथ-साथ उच्च ग्रेड एस्ट्रोसाइटोमास में इन 13 जीनों के नियंत्रण ने सुझाव दिया कि वे एस्ट्रोसाइटोमा के प्रारंभी और बाद के चरणों में महत्वपूर्ण हो सकते हैं। अन्य उदाहरण में, किताजीमा एट अल है।[21] पाया गया कि एमएलएच1 और ओ-6-मिथाइलगुआनिन-डीएनए मिथाइलट्रांसफेरेज़ अभिव्यक्ति के लिए प्रतिरक्षण को गैस्ट्रिक कैंसर के 135 प्रतिरूपों में सूक्ष्म से सहसंबद्ध किया गया था और एमएलएच1 और एमजीएमटी के हानि को ट्यूमर की प्रगति के समय समकालिक रूप से त्वरित किया गया था।
कई डीएनए सुधार जीनों की त्रुटिपूर्ण अभिव्यक्ति अधिकांशतः कैंसर में पाई जाती है,[15] और सामान्यतः कैंसर में पाए जाने वाले हजारों म्यूटेशन में योगदान कर सकते हैं (संपूर्ण जीनोम अनुक्रमण म्यूटेशन आवृत्ति देखें)।
अर्धसूत्रीविभाजन
डीएनए असंगत सुधार में अपनी भूमिका के अतिरिक्त, एमएलएच1 प्रोटीन अर्धसूत्रीविभाजन गुणसूत्रल क्रॉसओवर में भी सम्मिलित है।[22] एमएलएच1 एमएलएच3 के साथ हेटेरोडिमर बनाता है जो अर्धसूत्रीविभाजन II के मेटाफ़ेज़ II के माध्यम से अंडाणुओं की प्रगति के लिए आवश्यक प्रतीत होता है।[23] मादा और नर एमएलएच1(-/-) उत्परिवर्तित चूहे बांझ होते हैं, और बंध्यता काइस्मा (आनुवांशिकी) के निम्न स्तर से जुड़ा होता है।[22][24] एमएलएच1(-/-) में शुक्राणुजनन के समय उत्परिवर्ती चूहों के गुणसूत्र अधिकांशतः समय से पहले अलग हो जाते हैं और अर्धसूत्रीविभाजन के पहले विभाजन में निरंतर अवरुद्ध होते है।[22] मनुष्यों में, एमएलएच1 जीन का सामान्य रूप शुक्राणु क्षति और पुरुष बांझपन के बढ़ते कठिन परिस्थिति से जुड़ा है।[25]
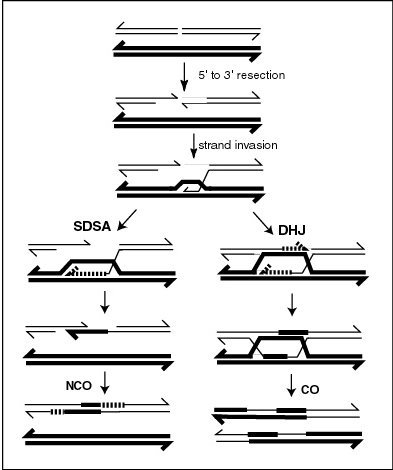
एमएलएच1 प्रोटीन अर्धसूत्री गुणसूत्रों में क्रॉसिंग ओवर की साइटों के लिए स्थानीयकृत प्रतीत होता है।[22] अर्धसूत्रीविभाजन के समय आनुवंशिक पुनर्संयोजन अधिकांशतः डीएनए डबल-स्ट्रैंड ब्रेक (डीएसबी) द्वारा प्रारंभ किया जाता है जैसा कि साथ में चित्र में दिखाया गया है। पुनर्संयोजन के समय, ब्रेक के 5' सिरों पर डीएनए के खंड प्रक्रिया में कट जाते हैं जिसे शोधन कहा जाता है। इसके बाद आने वाले स्ट्रैंड आक्रमण चरण में, टूटे हुए डीएनए अणु का ओवरहैंगिंग 3' छोर फिर समरूप गुणसूत्र के डीएनए पर आक्रमण करता है जो डी-पाश (डी-लूप) बनाने के लिए टूटा नहीं है। भूग्रस्त आक्रमण के बाद, घटनाओं का आगे का क्रम क्रॉसओवर (सीओ) या एक गैर-क्रॉसओवर (एनसीओ) पुनः संयोजक (आनुवांशिक पुनर्संयोजन देखें) के लिए जाने वाले दो मुख्य मार्गों का अनुसरण कर सकता है। सीओ की ओर जाने वाले मार्ग में डबल हॉलिडे जंक्शन (डीएचजे) इंटरमीडिएट सम्मिलित है। सीओ पुनर्संयोजन को पूरा करने के लिए हॉलिडे जंक्शनों को हल करने की आवश्यकता है।
बडिंग यीस्ट सैक्रोमाइसेस सेरेविसिया में, जैसा कि माउस में होता है, एमएलएच1 एमएलएच3 के साथ हेटेरोडिमर बनाता है। अर्धसूत्रीविभाजन सीओ को एमएलएच1-एमएलएच3 प्रोटीन डिमर की क्रियाओं के माध्यम से हॉलिडे जंक्शनों के विभेदन की आवश्यकता होती है। एमएलएच1-एमएलएच3 प्रोटीन डिमर एंडोन्यूक्लिएज है जो डीएनए सुपरकॉइल डबल-स्ट्रैंडेड डीएनए में सिंगल-स्ट्रैंड ब्रेक बनाता है।[26][27] एमएलएच1-एमएलएच3 विशेष रूप से हॉलिडे जंक्शनों से जुड़ता है और अर्धसूत्रीविभाजन के समय हॉलिडे जंक्शनों को संसाधित करने के लिए बड़े परिसर के भाग के रूप में कार्य कर सकता है।[26] एमएलएच1-एमएलएच3 हेटेरोडिमर (एमयूटीएल गामा) ईएक्सओ1 और एसजीएस1 (ब्लूम सिंड्रोम प्रोटीन के ऑर्थोलॉग) के साथ मिलकर संयुक्त अणु विभेदन मार्ग को परिभाषित करता है जो बडिंग यीस्ट में बहुसंख्यक क्रॉसओवर और स्तनधारियों में निष्कर्ष का उत्पादन करता है |[28]
नैदानिक महत्व
यह टरकोट-सिंड्रोम से भी जुड़ा हो सकता है।[29]
इंटरेक्शन
एमएलएच1 को प्रोटीन-प्रोटीन इंटरेक्शन के साथ दिखाया गया है:
यह भी देखें
- असंगत सुधार एमयूटीएच: ई. कोलाई और साल्मोनेला में उपस्थित एंडोन्यूक्लिज़
संदर्भ
- ↑ "Entrez Gene: MLH1 mutL homolog 1, colon cancer, nonpolyposis type 2 (E. coli)".
- ↑ 2.0 2.1 2.2 Pal T, Permuth-Wey J, Sellers TA (2008). "डिम्बग्रंथि के कैंसर में बेमेल-मरम्मत की कमी की नैदानिक प्रासंगिकता की समीक्षा". Cancer. 113 (4): 733–42. doi:10.1002/cncr.23601. PMC 2644411. PMID 18543306.
{{cite journal}}: zero width space character in|title=at position 57 (help) - ↑ 3.0 3.1 Truninger K, Menigatti M, Luz J, Russell A, Haider R, Gebbers JO, Bannwart F, Yurtsever H, Neuweiler J, Riehle HM, Cattaruzza MS, Heinimann K, Schär P, Jiricny J, Marra G (2005). "Immunohistochemical analysis reveals high frequency of PMS2 defects in colorectal cancer". Gastroenterology. 128 (5): 1160–71. doi:10.1053/j.gastro.2005.01.056. PMID 15887099.
- ↑ Goellner EM, Putnam CD, Kolodner RD (2015). "एक्सोन्यूक्लिज़ 1-आश्रित और स्वतंत्र बेमेल मरम्मत". DNA Repair (Amst.). 32: 24–32. doi:10.1016/j.dnarep.2015.04.010. PMC 4522362. PMID 25956862.
- ↑ Li GM (2008). "डीएनए बेमेल मरम्मत के तंत्र और कार्य". Cell Res. 18 (1): 85–98. doi:10.1038/cr.2007.115. PMID 18157157.
- ↑ Li GM (2014). "New insights and challenges in mismatch repair: getting over the chromatin hurdle". DNA Repair (Amst.). 19: 48–54. doi:10.1016/j.dnarep.2014.03.027. PMC 4127414. PMID 24767944.
- ↑ Kupčinskaitė-Noreikienė R, Skiecevičienė J, Jonaitis L, Ugenskienė R, Kupčinskas J, Markelis R, Baltrėnas V, Sakavičius L, Semakina I, Grižas S, Juozaitytė E (2013). "CpG island methylation of the MLH1, MGMT, DAPK, and CASP8 genes in cancerous and adjacent noncancerous stomach tissues". Medicina (Kaunas). 49 (8): 361–6. PMID 24509146.
- ↑ Waki T, Tamura G, Tsuchiya T, Sato K, Nishizuka S, Motoyama T (2002). "Promoter methylation status of E-cadherin, hMLH1, and p16 genes in nonneoplastic gastric epithelia". Am. J. Pathol. 161 (2): 399–403. doi:10.1016/S0002-9440(10)64195-8. PMC 1850716. PMID 12163364.
- ↑ Endoh Y, Tamura G, Ajioka Y, Watanabe H, Motoyama T (2000). "Frequent hypermethylation of the hMLH1 gene promoter in differentiated-type tumors of the stomach with the gastric foveolar phenotype". Am. J. Pathol. 157 (3): 717–22. doi:10.1016/S0002-9440(10)64584-1. PMC 1949419. PMID 10980110.
- ↑ Wani M, Afroze D, Makhdoomi M, Hamid I, Wani B, Bhat G, Wani R, Wani K (2012). "Promoter methylation status of DNA repair gene (hMLH1) in gastric carcinoma patients of the Kashmir valley". Asian Pac. J. Cancer Prev. 13 (8): 4177–81. doi:10.7314/apjcp.2012.13.8.4177. PMID 23098428.
- ↑ Chang Z, Zhang W, Chang Z, Song M, Qin Y, Chang F, Guo H, Wei Q (2015). "Expression characteristics of FHIT, p53, BRCA2 and MLH1 in families with a history of oesophageal cancer in a region with a high incidence of oesophageal cancer". Oncol Lett. 9 (1): 430–436. doi:10.3892/ol.2014.2682. PMC 4246613. PMID 25436004.
- ↑ Tawfik HM, El-Maqsoud NM, Hak BH, El-Sherbiny YM (2011). "Head and neck squamous cell carcinoma: mismatch repair immunohistochemistry and promoter hypermethylation of hMLH1 gene". Am J Otolaryngol. 32 (6): 528–36. doi:10.1016/j.amjoto.2010.11.005. PMID 21353335.
- ↑ Zuo C, Zhang H, Spencer HJ, Vural E, Suen JY, Schichman SA, Smoller BR, Kokoska MS, Fan CY (2009). "Increased microsatellite instability and epigenetic inactivation of the hMLH1 gene in head and neck squamous cell carcinoma". Otolaryngol Head Neck Surg. 141 (4): 484–90. doi:10.1016/j.otohns.2009.07.007. PMID 19786217. S2CID 8357370.
- ↑ Safar AM, Spencer H, Su X, Coffey M, Cooney CA, Ratnasinghe LD, Hutchins LF, Fan CY (2005). "Methylation profiling of archived non-small cell lung cancer: a promising prognostic system". Clin. Cancer Res. 11 (12): 4400–5. doi:10.1158/1078-0432.CCR-04-2378. PMID 15958624.
- ↑ 15.0 15.1 15.2 Bernstein C, Bernstein H (2015). "गैस्ट्रोइंटेस्टाइनल कैंसर के लिए प्रगति में डीएनए की मरम्मत की एपिजेनेटिक कमी". World J Gastrointest Oncol. 7 (5): 30–46. doi:10.4251/wjgo.v7.i5.30. PMC 4434036. PMID 25987950.
- ↑ 16.0 16.1 Valeri N, Gasparini P, Fabbri M, Braconi C, Veronese A, Lovat F, Adair B, Vannini I, Fanini F, Bottoni A, Costinean S, Sandhu SK, Nuovo GJ, Alder H, Gafa R, Calore F, Ferracin M, Lanza G, Volinia S, Negrini M, McIlhatton MA, Amadori D, Fishel R, Croce CM (2010). "Modulation of mismatch repair and genomic stability by miR-155". Proc. Natl. Acad. Sci. U.S.A. 107 (15): 6982–7. Bibcode:2010PNAS..107.6982V. doi:10.1073/pnas.1002472107. PMC 2872463. PMID 20351277.
- ↑ Rubin H (March 2011). "Fields and field cancerization: the preneoplastic origins of cancer: asymptomatic hyperplastic fields are precursors of neoplasia, and their progression to tumors can be tracked by saturation density in culture". BioEssays. 33 (3): 224–31. doi:10.1002/bies.201000067. PMID 21254148. S2CID 44981539.
- ↑ Tsao JL, Yatabe Y, Salovaara R, Järvinen HJ, Mecklin JP, Aaltonen LA, Tavaré S, Shibata D (February 2000). "व्यक्तिगत कोलोरेक्टल ट्यूमर इतिहास का आनुवंशिक पुनर्निर्माण". Proc. Natl. Acad. Sci. U.S.A. 97 (3): 1236–41. Bibcode:2000PNAS...97.1236T. doi:10.1073/pnas.97.3.1236. PMC 15581. PMID 10655514.
- ↑ Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA, Kinzler KW (March 2013). "कैंसर जीनोम परिदृश्य". Science. 339 (6127): 1546–58. Bibcode:2013Sci...339.1546V. doi:10.1126/science.1235122. PMC 3749880. PMID 23539594.
- ↑ Jiang Z, Hu J, Li X, Jiang Y, Zhou W, Lu D (2006). "Expression analyses of 27 DNA repair genes in astrocytoma by TaqMan low-density array". Neurosci. Lett. 409 (2): 112–7. doi: