ऑटोकैटलिसिस
This article needs additional citations for verification. (September 2010) (Learn how and when to remove this template message) |
एक एकल रासायनिक प्रतिक्रिया को ऑटोकैटलिटिक कहा जाता है यदि प्रतिक्रिया उत्पादों में से एक उसी या युग्मित प्रतिक्रिया के लिए उत्प्रेरक भी हो।[1] इस तरह की प्रतिक्रिया को ऑटोकैटलिटिक प्रतिक्रिया कहा जाता है।
रासायनिक प्रतिक्रियाओं के एक 'सेट' को सामूहिक रूप से ऑटोकैटलिटिक कहा जा सकता है यदि उन प्रतिक्रियाओं की एक संख्या प्रतिक्रिया उत्पादों के रूप में उत्पन्न होती है, अन्य प्रतिक्रियाओं के लिए पर्याप्त उत्प्रेरक है कि रासायनिक प्रतिक्रियाओं का पूरा सेट आत्मनिर्भर है जिसका इनपुट दिया गया है ऊर्जा और खाद्य अणु (ऑटोकैटलिटिक सेट देखें)।
रासायनिक प्रतिक्रियाएं
दो अभिकारकों और दो उत्पादों की रासायनिक अभिक्रिया को इस प्रकार लिखा जा सकता है:
जहां ग्रीक अक्षर स्टोइकोमेट्रिक गुणांक हैं और बड़े लैटिन अक्षर रासायनिक प्रजातियों का प्रतिनिधित्व करते हैं। रासायनिक प्रतिक्रिया आगे और पीछे दोनों दिशाओं में आगे बढ़ती है। यह समीकरण किसी भी संख्या में अभिकारकों, उत्पादों और प्रतिक्रियाओं के लिए आसानी से सामान्यीकृत होता है।
रासायनिक संतुलन
रासायनिक संतुलन में आगे और पीछे की प्रतिक्रिया दर ऐसी होती है कि प्रत्येक रासायनिक प्रजाति को उसी दर से बनाया जा रहा है जिस दर पर इसे नष्ट किया जा रहा है। दूसरे शब्दों में, अग्र अभिक्रिया की दर प्रतिवर्ती अभिक्रिया की दर के बराबर होती है।
यहाँ, कोष्ठक रासायनिक प्रजातियों की सांद्रता को मोल (इकाई) प्रति लीटर और k . में दर्शाते हैं+ और को− दर स्थिरांक हैं।
संतुलन से दूर
संतुलन से दूर, आगे और पीछे की प्रतिक्रिया दर अब संतुलित नहीं है और अभिकारकों और उत्पादों की एकाग्रता अब स्थिर नहीं है। हर आगे की प्रतिक्रिया के लिए A के अणु नष्ट हो जाते हैं। प्रत्येक विपरीत प्रतिक्रिया के लिए A के अणु बनते हैं। प्रारंभिक प्रतिक्रिया चरण के मामले में प्रत्येक दिशा में प्रतिक्रिया क्रम आणविकता के बराबर होता है, ताकि ए के मोलों की संख्या में परिवर्तन की दर तब हो
समीकरणों की इस प्रणाली में एक स्थिर स्थिर बिंदु (गणित) होता है जब आगे की दरें और विपरीत दरें समान होती हैं (जब हर प्रजाति के लिए)। इसका मतलब यह है कि प्रणाली संतुलन की स्थिति में विकसित होती है, और यह एकमात्र ऐसी स्थिति है जिसके लिए वह विकसित होती है।[2]
स्वत: उत्प्रेरक अभिक्रियाएं
ऑटोकैटलिटिक प्रतिक्रियाएं वे हैं जिनमें कम से कम एक उत्पाद एक अभिकारक है। शायद सबसे सरल ऑटोकैटलिटिक प्रतिक्रिया लिखी जा सकती है[1]
दर समीकरणों के साथ (प्राथमिक प्रतिक्रिया के लिए)
- .
यह प्रतिक्रिया वह है जिसमें प्रजाति A का एक अणु प्रजाति B के अणु के साथ परस्पर क्रिया करता है। A अणु B अणु में परिवर्तित हो जाता है। अंतिम उत्पाद में मूल बी अणु और प्रतिक्रिया में निर्मित बी अणु होता है।
इन दर समीकरणों की प्रमुख विशेषता यह है कि वे अरेखीय हैं; दाईं ओर का दूसरा पद B की सांद्रता के वर्ग के रूप में भिन्न होता है। यह सुविधा सिस्टम के कई निश्चित बिंदुओं को जन्म दे सकती है, ठीक उसी तरह जैसे द्विघात समीकरण में कई जड़ें हो सकती हैं। एकाधिक निश्चित बिंदु सिस्टम के कई राज्यों के लिए अनुमति देते हैं। एकाधिक स्थूल राज्यों में मौजूद एक प्रणाली एक राज्य में एक प्रणाली की तुलना में अधिक व्यवस्थित (कम एन्ट्रॉपी है) है।
A और B की सांद्रता समय के अनुसार बदलती रहती है[1][3] : तथा
- .
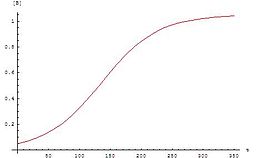
इन समीकरणों के लिए ग्राफ एक सिग्मॉइड फ़ंक्शन (विशेष रूप से एक रसद समारोह ) है, जो ऑटोकैटलिटिक प्रतिक्रियाओं के लिए विशिष्ट है: ये रासायनिक प्रतिक्रियाएं शुरुआत में धीरे-धीरे आगे बढ़ती हैं (प्रेरण अवधि) क्योंकि थोड़ा उत्प्रेरक मौजूद है, प्रतिक्रिया की दर उत्तरोत्तर बढ़ जाती है उत्प्रेरक की मात्रा बढ़ने पर प्रतिक्रिया आगे बढ़ती है और फिर प्रतिक्रियाशील एकाग्रता कम होने पर यह फिर से धीमी हो जाती है। यदि किसी प्रयोग में किसी अभिकारक या उत्पाद की सांद्रता सिग्मॉइड वक्र का अनुसरण करती है, तो प्रतिक्रिया स्वतः उत्प्रेरक हो सकती है।
ये गतिज समीकरण उदाहरण के लिए कार्बोज़ाइलिक तेजाब और अल्कोहल (रसायन विज्ञान) के कुछ एस्टर के एसिड-उत्प्रेरित हाइड्रोलिसिस पर लागू होते हैं।[3]उत्प्रेरित तंत्र को शुरू करने के लिए शुरू में कम से कम कुछ एसिड मौजूद होना चाहिए; यदि नहीं, तो प्रतिक्रिया एक वैकल्पिक अनियंत्रित पथ से शुरू होनी चाहिए जो आमतौर पर धीमी होती है। उत्प्रेरित तंत्र के लिए उपरोक्त समीकरणों का अर्थ होगा कि अम्ल उत्पाद की सांद्रता हमेशा के लिए शून्य रहती है।[3]
आदेश का निर्माण
पृष्ठभूमि
ऊष्मप्रवैगिकी का दूसरा नियम कहता है कि एक भौतिक या रासायनिक प्रणाली और उसके परिवेश (एक बंद प्रणाली ) के विकार (एन्ट्रॉपी) समय के साथ बढ़ना चाहिए। अपने आप में छोड़े गए सिस्टम तेजी से यादृच्छिक हो जाते हैं, और एकसमान गति जैसी प्रणाली की व्यवस्थित ऊर्जा अंततः गर्मी स्नान में कणों की यादृच्छिक गति को कम कर देती है।
हालाँकि, ऐसे कई उदाहरण हैं जिनमें भौतिक प्रणालियाँ स्वतः ही उभरती या व्यवस्थित हो जाती हैं। उदाहरण के लिए, उनके द्वारा किए गए विनाश के बावजूद, एक बंद कमरे में हवा के अणुओं की यादृच्छिक गति की तुलना में तूफान में एक बहुत ही व्यवस्थित भंवर गति होती है। रासायनिक प्रणालियों द्वारा बनाया गया क्रम और भी शानदार है; सबसे नाटकीय जीवन से जुड़ी व्यवस्था है।
यह दूसरे कानून के अनुरूप है, जिसके लिए यह आवश्यक है कि समय के साथ एक प्रणाली और उसके परिवेश का कुल विकार बढ़ना चाहिए। सिस्टम के परिवेश के क्रम में और भी अधिक कमी करके सिस्टम में ऑर्डर बनाया जा सकता है।[4] तूफान के उदाहरण में, वायुमंडल के भीतर असमान ताप से तूफान बनते हैं। पृथ्वी का वायुमंडल तब तापीय संतुलन से बहुत दूर है। पृथ्वी के वायुमंडल का क्रम बढ़ता है, लेकिन सूर्य के क्रम की कीमत पर। जैसे-जैसे उम्र बढ़ती है सूर्य और अधिक अव्यवस्थित होता जा रहा है और बाकी ब्रह्मांड में प्रकाश और सामग्री को फेंकता है। पृथ्वी पर व्यवस्थित रूप से तूफान उत्पन्न होने के बावजूद सूर्य और पृथ्वी का कुल विकार बढ़ जाता है।
जीवित रासायनिक प्रणालियों के लिए एक समान उदाहरण मौजूद है। सूर्य हरे पौधों को ऊर्जा प्रदान करता है। हरे पौधे अन्य जीवित रासायनिक प्रणालियों के लिए भोजन हैं। पौधों द्वारा अवशोषित और रासायनिक ऊर्जा में परिवर्तित होने वाली ऊर्जा पृथ्वी पर एक ऐसी प्रणाली उत्पन्न करती है जो व्यवस्थित और रासायनिक संतुलन से दूर है। यहां, रासायनिक संतुलन से अंतर संतुलन राशि से अधिक अभिकारकों द्वारा निर्धारित किया जाता है। एक बार फिर, सूर्य की एन्ट्रापी वृद्धि की कीमत पर पृथ्वी पर आदेश उत्पन्न होता है। द्वितीय नियम के अनुरूप पृथ्वी और शेष ब्रह्मांड की कुल एन्ट्रापी बढ़ जाती है।
कुछ ऑटोकैटलिटिक प्रतिक्रियाएं भी अपने परिवेश की कीमत पर एक प्रणाली में आदेश उत्पन्न करती हैं। उदाहरण के लिए, (घड़ी की प्रतिक्रियाओं) में प्रतिक्रिया मध्यवर्ती होती है, जिसकी सांद्रता समय के साथ दोलन करती है, जो लौकिक क्रम के अनुरूप होती है। अन्य प्रतिक्रियाएं स्थानिक क्रम के अनुरूप रासायनिक प्रजाति यों का स्थानिक पृथक्करण उत्पन्न करती हैं। जैविक प्रणालियों में चयापचय पथ और चयापचय नेटवर्क में अधिक जटिल प्रतिक्रियाएं शामिल हैं।
संतुलन से दूरी बढ़ने पर क्रम में संक्रमण आमतौर पर निरंतर नहीं होता है। आदेश आमतौर पर अचानक प्रकट होता है। रासायनिक संतुलन और व्यवस्था के विकार के बीच की दहलीज को चरण संक्रमण के रूप में जाना जाता है। एक चरण संक्रमण के लिए शर्तों को गैर-संतुलन थर्मोडायनामिक्स की गणितीय मशीनरी के साथ निर्धारित किया जा सकता है।
अस्थायी क्रम
एक रासायनिक प्रतिक्रिया अंतिम रासायनिक संतुलन की स्थिति के बारे में दोलन नहीं कर सकती है क्योंकि थर्मोडायनामिक्स के दूसरे नियम के लिए आवश्यक है कि एक थर्मोडायनामिक प्रणाली संतुलन के करीब पहुंच जाए और इससे पीछे न हटे। स्थिर तापमान और दबाव पर एक बंद प्रणाली के लिए, गिब्स मुक्त ऊर्जा को लगातार कम करना चाहिए और दोलन नहीं करना चाहिए। हालाँकि यह संभव है कि कुछ प्रतिक्रिया मध्यवर्ती की सांद्रता दोलन करती है, और यह भी कि उत्पादों के बनने की दर दोलन करती है।[5]
आदर्श उदाहरण: लोटका-वोल्टेरा समीकरण
दो ऑटोकैटलिटिक प्रतिक्रियाओं के एक युग्मित सेट पर विचार करें जिसमें एक अभिकारक A की सांद्रता उसके संतुलन मूल्य से बहुत अधिक है। इस मामले में, आगे की प्रतिक्रिया दर रिवर्स दरों की तुलना में इतनी बड़ी है कि हम रिवर्स दरों की उपेक्षा कर सकते हैं।
दर समीकरणों के साथ
- .
यहाँ, हमने अभिकारक A के ह्रास की उपेक्षा की है, क्योंकि इसकी सांद्रता इतनी अधिक है। तीन प्रतिक्रियाओं के लिए दर स्थिरांक हैं , , तथा , क्रमश।
दर समीकरणों की इस प्रणाली को लोटका-वोल्टेरा समीकरण के रूप में जाना जाता है और यह शिकारी-शिकार संबंधों में जनसंख्या की गतिशीलता के साथ सबसे अधिक निकटता से जुड़ा हुआ है। समीकरणों की यह प्रणाली प्रतिक्रिया मध्यवर्ती एक्स और वाई की दोलन सांद्रता उत्पन्न कर सकती है। दोलनों का आयाम ए की एकाग्रता पर निर्भर करता है (जो बिना दोलन के घट जाती है)। इस तरह के दोलन आकस्मिक अस्थायी क्रम का एक रूप है जो संतुलन में मौजूद नहीं है।
एक और आदर्श उदाहरण: ब्रुसेलेटर
एक प्रणाली का एक और उदाहरण जो लौकिक व्यवस्था को प्रदर्शित करता है वह ब्रुसेलेटर है।[4]यह प्रतिक्रियाओं की विशेषता है
दर समीकरणों के साथ
जहां, सुविधा के लिए, दर स्थिरांक 1 पर सेट किए गए हैं।

ब्रसेलेटर का एक निश्चित बिंदु होता है
- .
स्थिर बिंदु अस्थिर हो जाता है जब
प्रणाली के एक दोलन के लिए अग्रणी। लोटका-वोल्टेरा समीकरण के विपरीत, ब्रुसेलेटर के दोलन प्रारंभ में मौजूद अभिकारक की मात्रा पर निर्भर नहीं करते हैं। इसके बजाय, पर्याप्त समय के बाद, दोलन एक सीमा चक्र के करीब पहुंच जाते हैं।[6]
स्थानिक क्रम
स्थानिक स्वतःस्फूर्त समरूपता तोड़ने का एक आदर्श उदाहरण वह मामला है जिसमें हमारे पास एक पारगम्य झिल्ली द्वारा अलग की गई सामग्री के दो बक्से होते हैं ताकि सामग्री दो बक्से के बीच फैल सके। यह माना जाता है कि लगभग समान प्रारंभिक स्थितियों के साथ प्रत्येक बॉक्स में समान ब्रूसेलेटर हैं।[4]
यहां, संख्यात्मक सबस्क्रिप्ट इंगित करते हैं कि सामग्री किस बॉक्स में है। प्रसार गुणांक डी के आनुपातिक अतिरिक्त शब्द हैं जो बक्से के बीच सामग्री के आदान-प्रदान के लिए जिम्मेदार हैं।
यदि सिस्टम को प्रत्येक बॉक्स में समान शर्तों के साथ शुरू किया जाता है, तो एक छोटे से उतार-चढ़ाव से दो बॉक्स के बीच सामग्री अलग हो जाएगी। एक बॉक्स में X की प्रधानता होगी, और दूसरे में Y की प्रधानता होगी।
वास्तविक उदाहरण
घड़ी की प्रतिक्रिया ओं के वास्तविक उदाहरण बेलौसोव-ज़ाबोटिंस्की प्रतिक्रिया (बीजेड प्रतिक्रिया), ब्रिग्स-रौशर प्रतिक्रिया, ब्रे-लीभाफ्स्की प्रतिक्रिया और आयोडीन घड़ी प्रतिक्रिया हैं। ये ऑसिलेटरी प्रतिक्रियाएं हैं, और उत्पादों और अभिकारकों की सांद्रता को डंपिंग अनुपात दोलनों के संदर्भ में अनुमानित किया जा सकता है।
सबसे प्रसिद्ध प्रतिक्रिया, बीजेड प्रतिक्रिया, पोटेशियम ब्रोमेट <केम> (केबीआरओ 3) </केम>, मैलोनिक एसिड <केम> (सीएच 2 (सीओओएच) 2) </केम>, और मैंगनीज सल्फेट के मिश्रण से बनाई जा सकती है। सल्फ्यूरिक एसिड <केम>(H2SO4)</केम> सॉल्वेंट के रूप में गर्म घोल में तैयार किया जाता है।[7]
प्रकाशिकी उदाहरण
एक अन्य ऑटोकैटलिटिक प्रणाली प्रकाश द्वारा संचालित है जो फोटो-पोलीमराइजेशन प्रतिक्रियाओं के लिए युग्मित है। ऑप्टिकल ऑटोकैटलिसिस नामक एक प्रक्रिया में, अपवर्तक सूचकांक में पोलीमराइज़ेशन-प्रेरित वृद्धि के माध्यम से, प्रकाश की तीव्रता और फोटो-पोलीमराइज़ेशन दर के बीच सकारात्मक प्रतिक्रिया बनाई जाती है। उच्च अपवर्तनांक वाले क्षेत्रों पर कब्जा करने के लिए प्रकाश की प्राथमिकता के परिणामस्वरूप उच्च आणविक भार वाले क्षेत्रों में प्रकाश का रिसाव होता है, जिससे फोटो-रासायनिक प्रतिक्रिया बढ़ जाती है। सकारात्मक प्रतिक्रिया के रूप में व्यक्त किया जा सकता है:[8]
यह देखते हुए कि फोटो-पोलीमराइजेशन दर तीव्रता के समानुपाती है[9] और वह अपवर्तनांक आणविक भार के समानुपाती होता है,[10] तीव्रता और फोटो-पोलीमराइजेशन के बीच सकारात्मक प्रतिक्रिया ऑटो-कैटेलिटिक व्यवहार को स्थापित करती है। ऑप्टिकल ऑटो-कैटेलिसिस को फोटोपॉलिमर में सहज पैटर्न के गठन के परिणामस्वरूप दिखाया गया है।[11][12][13] होसीन और सहकर्मियों ने पाया कि ऑप्टिकल ऑटोकैटलिसिस फोटोरिएक्टिव पॉलिमर मिश्रणों में भी हो सकता है, और यह प्रक्रिया बाइनरी चरण आकारिकी को प्रकाश प्रोफ़ाइल के समान पैटर्न के साथ प्रेरित कर सकती है।[8]प्रकाश ऑप्टिकल मॉड्यूलेशन अस्थिरता से गुजरता है, ऑप्टिकल फिलामेंट्स की एक भीड़ में सहज विभाजन होता है, और बहुलक प्रणाली इस प्रकार मिश्रण संरचना के भीतर फिलामेंट्स बनाती है।[8]परिणाम एक नई प्रणाली है जो जोड़ों को स्पिनोडल अपघटन के लिए ऑप्टिकल ऑटोकैटलिटिक व्यवहार करता है।
जैविक उदाहरण
यह ज्ञात है कि एक महत्वपूर्ण चयापचय चक्र, ग्लाइकोलाइसिस , अस्थायी क्रम प्रदर्शित करता है।[14] ग्लाइकोलाइसिस में शर्करा के एक अणु का क्षरण और एडीनोसिन ट्राइफॉस्फेट के दो अणुओं का समग्र उत्पादन होता है। इसलिए जीवित कोशिकाओं के ऊर्जावानों के लिए प्रक्रिया का बहुत महत्व है। वैश्विक ग्लाइकोलाइसिस प्रतिक्रिया में ग्लूकोज, एडेनोसिन डाइफॉस्फेट , निकोटिनामाइड एडेनाइन डाईन्यूक्लियोटाइड , पाइरुविक तेजाब , एडेनोसाइन ट्रायफ़ोस्फेट और एनएडीएच शामिल हैं।
- <केम>ग्लूकोज{} + 2ADP{} + 2P_\mathit{i}{} + 2NAD -> 2(pyruvate){} + 2ATP{} + 2NADH</केम>।
प्रक्रिया का विवरण काफी शामिल है, हालांकि, प्रक्रिया का एक भाग फॉस्फोफ्रक्टोकिनेस (पीएफके) द्वारा स्वत: उत्प्रेरित होता है। प्रक्रिया का यह हिस्सा उस मार्ग में दोलनों के लिए जिम्मेदार है जो एक सक्रिय और एक निष्क्रिय रूप के बीच दोलन की प्रक्रिया की ओर ले जाता है। इस प्रकार, ऑटोकैटलिटिक प्रतिक्रिया प्रक्रिया को संशोधित कर सकती है।
पतली परतों की सिलाई का आकार
एक पतली परत के डिजाइन को तैयार करने के लिए प्रतिक्रिया-प्रसार प्रणाली सिद्धांत के साथ मिलकर एक ऑटोकैटलिटिक प्रतिक्रिया से परिणामों का उपयोग करना संभव है। ऑटोकैटलिटिक प्रक्रिया ऑक्सीकरण फ्रंट (भौतिकी) के गैर-रेखीय व्यवहार को नियंत्रित करने की अनुमति देती है, जिसका उपयोग मनमाने ढंग से अंतिम ज्यामिति उत्पन्न करने के लिए आवश्यक प्रारंभिक ज्यामिति को स्थापित करने के लिए किया जाता है।[15] यह के गीले ऑक्सीकरण में सफलतापूर्वक किया गया है की मनमानी आकार की परतें प्राप्त करने के लिए .
चरण संक्रमण
अभिकारकों की प्रारंभिक मात्रा प्रणाली के रासायनिक संतुलन से दूरी निर्धारित करती है। प्रारंभिक सांद्रता जितनी अधिक होगी, प्रणाली संतुलन से उतनी ही आगे होगी। जैसे-जैसे प्रारंभिक सांद्रता बढ़ती है, एन्ट्रापी में अचानक परिवर्तन होता है। इस अचानक परिवर्तन को चरण संक्रमण के रूप में जाना जाता है। चरण संक्रमण में, मैक्रोस्कोपिक मात्रा में उतार-चढ़ाव, जैसे कि रासायनिक सांद्रता, बढ़ जाती है क्योंकि सिस्टम अधिक क्रमबद्ध अवस्था (निचली एन्ट्रापी, जैसे बर्फ) और अधिक अव्यवस्थित अवस्था (उच्च एन्ट्रापी, जैसे तरल पानी) के बीच दोलन करता है। इसके अलावा, चरण संक्रमण पर, मैक्रोस्कोपिक समीकरण, जैसे कि दर समीकरण, विफल हो जाते हैं। दर समीकरण सूक्ष्म विचारों से प्राप्त किए जा सकते हैं। व्युत्पत्तियां आमतौर पर सूक्ष्म गतिशील समीकरणों के औसत क्षेत्र सिद्धांत सन्निकटन पर निर्भर करती हैं। बड़े उतार-चढ़ाव की उपस्थिति में माध्य क्षेत्र सिद्धांत टूट जाता है (चर्चा के लिए माध्य क्षेत्र सिद्धांत लेख देखें)। इसलिए, चूंकि एक चरण संक्रमण के पड़ोस में बड़े उतार-चढ़ाव होते हैं, मैक्रोस्कोपिक समीकरण, जैसे कि दर समीकरण, विफल हो जाते हैं। जैसे-जैसे प्रारंभिक एकाग्रता आगे बढ़ती है, सिस्टम एक क्रमबद्ध स्थिति में बस जाता है जिसमें उतार-चढ़ाव फिर से छोटे होते हैं।[4]
असममित ऑटोकैटलिसिस
असममित ऑटोकैटलिसिस तब होता है जब प्रतिक्रिया उत्पाद chiral होता है और इस प्रकार अपने स्वयं के उत्पादन के लिए चिरल उत्प्रेरक के रूप में कार्य करता है। इस प्रकार की प्रतिक्रियाएं, जैसे कि सोई प्रतिक्रिया , में यह गुण होता है कि वे एक बहुत छोटे एनैन्टीओमेरिक अतिरिक्त को एक बड़े में बढ़ा सकते हैं। यह जैविक समरूपता की उत्पत्ति में एक महत्वपूर्ण कदम के रूप में प्रस्तावित किया गया है।[16]
जीवन की उत्पत्ति में भूमिका
1995 में स्टुअर्ट कॉफ़मैन ने प्रस्तावित किया कि जीवन शुरू में ऑटोकैटलिटिक रासायनिक नेटवर्क के रूप में उभरा।[17] यूनाइटेड किंगडम के नैतिकतावादी रिचर्ड डॉकिन्स ने अपनी 2004 की किताब द एंसेस्टर्स टेल में ऑटोकैटलिसिस के बारे में जीवोत्पत्ति के संभावित स्पष्टीकरण के रूप में लिखा था। वह कैलिफोर्निया में स्क्रिप्स अनुसंधान संस्थान में जूलियस रेबेकी और उनके सहयोगियों द्वारा किए गए प्रयोगों का हवाला देते हैं जिसमें उन्होंने ऑटोकैटलिस्ट एमिनो एडेनोसिन ट्राइसिड एस्टर (एटीई) के साथ एमिनो एडेनोसिन और पेंटाफ्लोरोफेनिल एस्टर को जोड़ा। प्रयोग की एक प्रणाली में AATE के वेरिएंट शामिल थे जो स्वयं के संश्लेषण को उत्प्रेरित करते थे। इस प्रयोग ने इस संभावना को प्रदर्शित किया कि ऑटोकैटलिस्ट आनुवंशिकता के साथ संस्थाओं की आबादी के भीतर प्रतिस्पर्धा का प्रदर्शन कर सकते हैं, जिसे प्राकृतिक चयन के प्राथमिक रूप के रूप में व्याख्या किया जा सकता है, और यह कि कुछ पर्यावरणीय परिवर्तन (जैसे विकिरण) इनमें से कुछ स्वयं की रासायनिक संरचना को बदल सकते हैं। -प्रतिकृति अणु (म्यूटेशन के लिए एक एनालॉग) इस तरह से जो या तो प्रतिक्रिया करने की क्षमता को बढ़ा सकते हैं या हस्तक्षेप कर सकते हैं, इस प्रकार जनसंख्या में दोहराने और फैलाने की क्षमता में वृद्धि या हस्तक्षेप कर सकते हैं।[18] जीवन की प्रक्रियाओं में ऑटोकैटलिसिस एक प्रमुख भूमिका निभाता है। दो शोधकर्ता जिन्होंने जीवन की उत्पत्ति में इसकी भूमिका पर जोर दिया है, वे हैं रॉबर्ट उलानोविक्ज़ [19] और स्टुअर्ट कॉफ़मैन।[20] ऑटोकैटलिसिस rRNA के प्रारंभिक टेप में होता है। इंट्रोन्स दो न्यूक्लियोफिलिक ट्रान्सएस्टरीफिकेशन प्रतिक्रियाओं की प्रक्रिया द्वारा खुद को उत्तेजित करने में सक्षम हैं। ऐसा करने में सक्षम आरएनए को कभी-कभी राइबोजाइम के रूप में जाना जाता है। इसके अतिरिक्त, साइट्रिक एसिड चक्र रिवर्स में चलने वाला एक ऑटोकैटलिटिक चक्र है।
अंततः, जैविक चयापचय को स्वयं एक विशाल ऑटोकैटलिटिक सेट के रूप में देखा जा सकता है, जिसमें एक जैविक कोशिका के सभी आणविक घटक अणुओं के इसी सेट से जुड़ी प्रतिक्रियाओं द्वारा निर्मित होते हैं।
ऑटोकैटलिटिक प्रतिक्रियाओं के उदाहरण
- सिल्वर हैलाइड फिल्म/कागज का फोटोग्राफिक प्रसंस्करण
- डी एन ए की नकल
- हेलोफॉर्म प्रतिक्रिया
- फॉर्मोज प्रतिक्रिया (जिसे बटलरोव प्रतिक्रिया के रूप में भी जाना जाता है)
- टिन कीट
- ऑक्सालिक अम्ल के साथ परमैंगनेट की अभिक्रिया[21]
- सिरका सिंड्रोम
- हीमोग्लोबिन द्वारा ऑक्सीजन का बंधन*
- सैलिसिलिक एसिड और एसिटिक एसिड में एस्पिरिन का स्वतःस्फूर्त क्षरण, जिससे सीलबंद कंटेनरों में बहुत पुरानी एस्पिरिन सिरके की हल्की गंध आती है।
- ब्रोमीन के साथ acetophenone का α-ब्रोमिन ेशन।
- लिसेगांग के छल्ले
- समाधान चरण में धातु नैनोकणों की ऑटोकैटलिटिक सतह वृद्धि[22]
यह भी देखें
- उत्प्रेरक चक्र
- प्रतिक्रिया-प्रसार प्रणाली
- मोर्फोजेनेसिस
संदर्भ
- ↑ 1.0 1.1 1.2 Steinfeld J.I., Francisco J.S. and Hase W.L. Chemical Kinetics and Dynamics (2nd ed., Prentice-Hall 1999) p.151-2 ISBN 0-13-737123-3
- ↑ Ross, John; Garcia-Colin, Leopoldo S. (March 1989). "संतुलन से दूर रासायनिक प्रणालियों के ऊष्मप्रवैगिकी". The Journal of Physical Chemistry. 93 (5): 2091–2092. doi:10.1021/j100342a075.
- ↑ 3.0 3.1 3.2 Moore J.W. and Pearson R.G. Kinetics and Mechanism (John Wiley 1981) p.26 ISBN 0-471-03558-0
- ↑ 4.0 4.1 4.2 4.3 Ilya Prigogine (1980). बीइंग से बीइंग तक: भौतिक विज्ञान में समय और जटिलता. San Francisco: W. H. Freeman. ISBN 978-0-7167-1107-0.
- ↑ Espenson, J.H. Chemical Kinetics and Reaction Mechanisms (2nd ed., McGraw-Hill 2002) p.190 ISBN 0-07-288362-6
- ↑ "संग्रहीत प्रति" (PDF). Archived from the original (PDF) on 2008-12-17. Retrieved 2015-10-15. Dynamics of the Brusselator
- ↑ Peterson, Gabriel. "बेलौसोव-ज़ाबोटिंस्की प्रतिक्रिया". Archived from the original on December 31, 2012.
- ↑ 8.0 8.1 8.2 Biria, Saeid; Malley, Phillip P. A.; Kahan, Tara F.; Hosein, Ian D. (2016-11-15). "ऑप्टिकल ऑटोकैटलिसिस फोटोक्योरिंग के दौरान पॉलिमर मिश्रणों के चरण पृथक्करण में उपन्यास स्थानिक गतिशीलता स्थापित करता है". ACS Macro Letters. 5 (11): 1237–1241. doi:10.1021/acsmacrolett.6b00659. PMID 35614732.
- ↑ Decker, Christian (1998-02-01). "पोलीमराइजेशन में यूवी विकिरण का उपयोग". Polymer International (in English). 45 (2): 133–141. doi:10.1002/(SICI)1097-0126(199802)45:2<133::AID-PI969>3.0.CO;2-F.
- ↑ Askadskii, A. A. (1990). "बहुलक नेटवर्क के गुणों पर क्रॉसलिंकिंग घनत्व का प्रभाव". Polymer Science U.S.S.R. 32 (10): 2061–2069. doi:10.1016/0032-3950(90)90361-9.
- ↑ Burgess, Ian B.; Shimmell, Whitney E.; Saravanamuttu, Kalaichelvi (2007-04-01). "एक photopolymerizable माध्यम में असंगत सफेद प्रकाश की मॉड्यूलेशन अस्थिरता के कारण सहज पैटर्न का गठन". Journal of the American Chemical Society. 129 (15): 4738–4746. doi:10.1021/ja068967b. ISSN 0002-7863. PMID 17378567.
- ↑ Basker, Dinesh K.; Brook, Michael A.; Saravanamuttu, Kalaichelvi (2015). "एपॉक्साइड्स के धनायनित पॉलिमराइजेशन के दौरान नॉनलाइनियर लाइट वेव्स और सेल्फ-इंस्क्राइब्ड वेवगाइड माइक्रोस्ट्रक्चर का सहज उदय". The Journal of Physical Chemistry C (in English). 119 (35): 20606–20617. doi:10.1021/acs.jpcc.5b07117.
- ↑ Biria, Saeid; Malley, Philip P. A.; Kahan, Tara F.; Hosein, Ian D. (2016-03-03). "फ्री-रेडिकल पॉलिमराइजेशन के दौरान क्रॉस-लिंकिंग एक्रिलेट सिस्टम में ट्यून करने योग्य नॉनलाइनियर ऑप्टिकल पैटर्न फॉर्मेशन और माइक्रोस्ट्रक्चर". The Journal of Physical Chemistry C. 120 (8): 4517–4528. doi:10.1021/acs.jpcc.5b11377. ISSN 1932-7447.
- ↑ G. Nicolis and Ilya Prigogine (1977). कोई भी संतुलन प्रणाली में स्व-संगठन. New York: John Wiley and Sons. ISBN 978-0-471-02401-9.
- ↑ Alfaro-Bittner, K.; Rojas, R.G.; Lafleur, G.; Calvez, S.; Almuneau, G.; Clerc, M.G.; Barbay, S. (22 April 2019). "मनमाना मेसा ज्यामिति में पार्श्व गीले ऑक्सीकरण की मॉडलिंग". Physical Review Applied. 11 (4): 044067. doi:10.1103/PhysRevApplied.11.044067. S2CID 149766853.
- ↑ Soai K, Sato I, Shibata T (2001). "असममित ऑटोकैटलिसिस और कार्बनिक यौगिकों में चिरल समरूपता की उत्पत्ति।". The Chemical Record. 1 (4): 321–32. doi:10.1002/tcr.1017. PMID 11893072.
- ↑ Stuart Kauffman (1995). ब्रह्मांड में घर पर: स्व-संगठन और जटिलता के नियमों की खोज. Oxford University Press. ISBN 978-0-19-509599-9.
- ↑ Rebeck, Julius (July 1994). "सिंथेटिक स्व-प्रतिकृति अणु". Scientific American. 271 (1): 48–55. Bibcode:1994SciAm.271a..48R. doi:10.1038/scientificamerican0794-48.
- ↑ Ecology, the Ascendent Perspective", Robert Ulanowicz, Columbia Univ. Press 1997.
- ↑ Investigations, Stuart Kauffman.
- ↑ Kovacs KA, Grof P, Burai L, Riedel M (2004). "परमैंगनेट/ऑक्सालेट प्रतिक्रिया के तंत्र को संशोधित करना". J. Phys. Chem. A. 108 (50): 11026–11031. Bibcode:2004JPCA..10811026K. doi:10.1021/jp047061u.
- ↑ Yin, Xi; Shi, Miao; Wu, Jianbo; Pan, Yung-Tin; Gray, Danielle L.; Bertke, Jeffery A.; Yang, Hong (11 September 2017). "लिगैंड रसायन विज्ञान द्वारा नियंत्रित प्लेटिनम नैनोक्रिस्टल के विभिन्न गठन मोड का मात्रात्मक विश्लेषण". Nano Letters. 17 (10): 6146–6150. Bibcode:2017NanoL..17.6146Y. doi:10.1021/acs.nanolett.7b02751. PMID 28873317.
बाहरी संबंध
- Some Remarks on Autocatalysis and Autopoiesis (Barry McMullin)
- Jain, Sanjay; Krishna, Sandeep (21 December 1998). "Autocatalytic Sets and the Growth of Complexity in an Evolutionary Model". Physical Review Letters. 81 (25): 5684–5687. arXiv:adap-org/9809003. Bibcode:1998PhRvL..81.5684J. doi:10.1103/PhysRevLett.81.5684. S2CID 14471886.