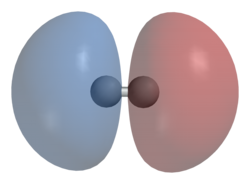
सिग्मा बंध

रसायन विज्ञान में, सिग्मा बंध (σ बंध) सबसे मजबूत प्रकार के सहसंयोजक रासायनिक बंध हैं।[1] ये परमाणु कक्षकों के बीच परस्पर अतिव्यापन द्वारा बनते हैं। समरूपता समूह की भाषा और उपकरणों का उपयोग करके द्विपरमाणुक अणुओं के लिए सिग्मा बंध को सबसे सरल रूप में परिभाषित किया गया है। इस औपचारिक दृष्टिकोण में, एक - बंध बंध अक्ष के परितः घूर्णन के संबंध में सममित होता है। इस परिभाषा के अनुसार, सिग्मा बंध के सामान्य रूप हैं s+s, pz+p, s+pz और dz2+dz2 (जहाँ z को आबंध की धुरी या अंतःनाभिकीय अक्ष के रूप में परिभाषित किया गया है)।[2]
क्वांटम सिद्धांत यह भी इंगित करता है कि समान समरूपता के आणविक ऑर्बिटल् (MO) वास्तव में मिश्रित या कक्षीय संकरण हैं। द्विपरमाणुक अणुओं के इस मिश्रण के व्यावहारिक परिणाम के रूप में, तरंग कार्य s+s और pz+pz आणविक कक्षक मिश्रित हो जाते हैं। मिश्रण (या संकरण या सम्मिश्रण) की सीमा समरूपता के आणविक ऑर्बिटल् की सापेक्ष ऊर्जा पर निर्भर करती है।
(होमोडायटोमिक्स) समद्विपरमाण्विक (होमोन्यूक्लियर डायटोमिक अणु) के लिए, बॉन्डिंग σ ऑर्बिटल् में कोई ऐसा नोडल प्लेन नहीं होता है, जिस पर वेवफंक्शन शून्य होता है, फिर चाहें वो बंध बने हुए परमाणुओं के बीच हो या दो परमाणुओं के बीच बने बंध से होकर गुजरता हो। संबंधित प्रतिरक्षी, या σ* ऑर्बिटल्, दो बंधित परमाणुओं के बीच एक नोडल तल की उपस्थिति से परिभाषित होता है।
ऑर्बिटल् के प्रत्यक्ष अतिव्यापन के कारण सिग्मा बंध सबसे मजबूत प्रकार के सहसंयोजक बंध हैं, और इन बंधों के इलेक्ट्रॉन को कभी-कभी सिग्मा इलेक्ट्रॉनों के रूप में जाना जाता है।[3]
प्रतीक σ ग्रीक अक्षर सिग्मा है। जब बंध अक्ष के नीचे देखा जाता है, तो σ MO में एक गोलाकार समरूपता होती है, इसलिए यह एक समान ध्वनि वाले "s" परमाणु कक्षीय जैसा दिखता है।
सामान्यतः, एक एकल बंध एक सिग्मा बंध होता है जबकि एक मल्टीपल बंध एक सिग्मा बंध से बना होता है जिसमें पाई या अन्य बंध होते हैं। एक द्विबंध में एक सिग्मा और एक पाई बंध होता है, और एक त्रिबंध बंध में एक सिग्मा और दो पाई बंध होता है।
| —— | ———————————————— | ————— |
Atomic orbitals |

| |
| Symmetric (s–s and p–p) sigma bonds between atomic orbitals |
A pi bond, for comparison | |
| —— | ———————————————— | ————— |
 σs–hybrid |
 σs–p | |
बहुपरमाणुक अणु
सिग्मा बंध परमाणु कक्षाओं के शीर्ष पर अतिव्यापी द्वारा प्राप्त किए जाते हैं। सिग्मा बॉन्डिंग की अवधारणा का विस्तार बॉन्डिंग इंटरैक्शन का वर्णन करने के लिए किया जाता है जिसमें एक परमाणु कक्षीय के एकल लोब का दूसरे के एकल लोब के साथ ओवरलैप शामिल होता है। उदाहरण के लिए, प्रोपेन को दस सिग्मा बंधों के रूप में वर्णित किया गया है, प्रत्येक दो सी-सी बंध के लिए एक और आठ सी-एच बंध के लिए एक-एक।
बहु-बंधुआ परिसर
संक्रमण धातु परिसर जिसमें कई बॉन्ड होते हैं, जैसे कि डाइहाइड्रोजन कॉम्प्लेक्स , में कई बॉन्डेड परमाणुओं के बीच सिग्मा बॉन्ड होते हैं। इन सिग्मा बॉन्ड को अन्य बॉन्डिंग इंटरैक्शन के साथ पूरक किया जा सकता है, जैसे कि पीआई बैकबॉन्डिंग | π-बैक डोनेशन, जैसा कि डब्ल्यू (सीओ) के मामले में है।3(ट्राइसीसाइक्लोहेक्सिलफॉस्फीन|पीसीवाई3)2(एच2), और यहां तक कि -बॉन्ड, जैसा कि क्रोमियम (II) एसीटेट के मामले में होता है।[4]
कार्बनिक अणु
कार्बनिक अणु अक्सर चक्रीय यौगिक होते हैं जिनमें एक या एक से अधिक छल्ले होते हैं, जैसे बेंजीन , और अक्सर पाई बंध के साथ कई सिग्मा बंधों से बने होते हैं। सिग्मा बंध नियम के अनुसार, एक अणु में सिग्मा बंधों की संख्या परमाणुओं की संख्या और वलय की संख्या घटा एक के बराबर होती है।
- एनσ = एनatoms + नहींrings - 1
यह नियम ग्राफ की यूलर विशेषता का एक विशेष-मामला अनुप्रयोग है जो अणु का प्रतिनिधित्व करता है।
बिना वलय वाले अणु को एक पेड़ (ग्राफ सिद्धांत) के रूप में दर्शाया जा सकता है, जिसमें परमाणुओं की संख्या माइनस वन (जैसे dihydrogen , एच) के बराबर कई बंधन होते हैं।2, केवल एक सिग्मा बंध, या अमोनिया , NH . के साथ3, 3 सिग्मा बंध के साथ)। किन्हीं दो परमाणुओं के बीच 1 से अधिक सिग्मा बंध नहीं होते हैं।
छल्ले वाले अणुओं में अतिरिक्त सिग्मा बंध होते हैं, जैसे बेंजीन के छल्ले, जिनमें 6 कार्बन परमाणुओं के लिए रिंग के भीतर 6 सी-सी सिग्मा बंध होते हैं। अंगारिन अणु, सी14H10, में तीन वलय हैं ताकि नियम 24 + 3 - 1 = 26 के रूप में सिग्मा बंधों की संख्या देता है। इस मामले में 16 सी-सी सिग्मा बंध और 10 सी-एच बंध हैं।
यह नियम उन अणुओं के मामले में विफल हो जाता है, जो कागज पर सपाट होने पर, वास्तव में अणु की तुलना में भिन्न संख्या में छल्ले होते हैं - उदाहरण के लिए, बकमिनस्टरफुलरीन , सी60, जिसमें 32 वलय, 60 परमाणु और 90 सिग्मा बंध हैं, प्रत्येक बंधित परमाणुओं के लिए एक; हालांकि, 60 + 32 - 1 = 91, 90 नहीं। ऐसा इसलिए है क्योंकि सिग्मा नियम यूलर विशेषता का एक विशेष मामला है, जहां प्रत्येक अंगूठी को एक चेहरा माना जाता है, प्रत्येक सिग्मा बंधन एक किनारा होता है, और प्रत्येक परमाणु एक शीर्ष होता है। सामान्यतः, एक अतिरिक्त चेहरा किसी रिंग के अंदर नहीं, बल्कि ट्रंकेटेड_िकोसाहेड्रोन#ट्रंकेटेड_कोसाहेड्रल_ग्राफ को सौंपा जाता है, रिंगों में से एक बाहरी पेंटागन बनाता है; उस रिंग के अंदर ग्राफ़ के बाहर है। अन्य आकृतियों पर विचार करते समय यह नियम और विफल हो जाता है - टॉरॉयडल फुलरीन इस नियम का पालन करेगा कि एक अणु में सिग्मा बंधों की संख्या बिल्कुल परमाणुओं की संख्या और छल्ले की संख्या है, जैसे नैनोट्यूब - जो, जब फ्लैट खींचा जाता है जैसे कि एक के माध्यम से देख रहा हो अंत से, बीच में एक चेहरा होगा, जो नैनोट्यूब के दूर के अंत के अनुरूप होगा, जो एक अंगूठी नहीं है, और बाहर के अनुरूप एक चेहरा होगा।
यह भी देखें
संदर्भ
- ↑ Moore, John; Stanitski, Conrad L.; Jurs, Peter C. (2009-01-21). रसायन विज्ञान के सिद्धांत: आण्विक विज्ञान. ISBN 9780495390794.
- ↑ Clayden, Jonathan; Greeves, Nick; Warren, Stuart (March 2012) [2002]. कार्बनिक रसायन शास्त्र (2nd ed.). Oxford: OUP Oxford. pp. 101–136. ISBN 978-0199270293.
- ↑ Keeler, James; Wothers, Peter (May 2008). रासायनिक संरचना और प्रतिक्रियाशीलता (1st ed.). Oxford: OUP Oxford. pp. 27–46. ISBN 978-0199289301.
- ↑ Kubas, Gregory (2002). "मेटल डाइहाइड्रोजन और -बॉन्ड कॉम्प्लेक्स: संरचना, सिद्धांत और प्रतिक्रियाशीलता". J. Am. Chem. Soc. 124 (14): 3799–3800. doi:10.1021/ja0153417.
इस पृष्ठ में अनुपलब्ध आंतरिक कड़ियों की सूची
- द्विपरमाणुक अणु
- परमाणु कक्षीय
- आणविक कक्षीय
- तरंग क्रिया
- डबल बंधन
- एकल बंधन
- वृत्ताकार समरूपता
- पी बंध
- क्रोमियम (द्वितीय) एसीटेट