कैल्शियम कार्बाइड: Difference between revisions
No edit summary |
No edit summary |
||
| Line 129: | Line 129: | ||
===कार्बाइड लैंप=== | ===कार्बाइड लैंप=== | ||
{{Main|कार्बाइड लैंप}}[[Image:Carbide lamp lit.jpg|thumb|right|कार्बाइड लैंप | {{Main|कार्बाइड लैंप}}[[Image:Carbide lamp lit.jpg|thumb|right|ज्योतिर्मय कार्बाइड लैंप ]]कैल्शियम कार्बाइड का उपयोग कार्बाइड लैंप में किया जाता है। कार्बाइड पर द्रव गिरने से एसिटिलीन गैस निकलती है, जो दहन के पश्चात प्रकाश उत्पन्न करती है। किन्तु ये लैंप मोमबत्तियों की अपेक्षा अधिक स्थिर और तीव्र प्रकाश उत्पन्न करते थे, ये [[कोयला]] खानों में हानिकारक थे, जहां ज्वलनशील [[मीथेन]] गैस ने इन्हें गंभीर बना दिया था। कोयला खानों में ज्वलनशील गैसों की उपस्थिति के कारण [[ दीपों की भीड़ |डेवी लैंप]] जैसे खनिक [[सुरक्षा लैंप]] का उपयोग किया गया, जिसमें तार का गेज मीथेन प्रज्वलन के संकट को कम करता है। कार्बाइड लैंप का उपयोग अभी भी [[स्लेट]], तांबे और [[ विश्वास |टिन]] की खानों में बड़े स्तर पर किया जाता था जहां मीथेन कोई गंभीर संकट नहीं है। अधिकांश खनिकों के लैंप को अब इलेक्ट्रिक [[ हेडलैम्प (आउटडोर) |हेडलैम्प (आउटडोर)]] ने परिवर्तित कर दिया है। | ||
कुछ | कुछ निम्न सक्षम देशों में खनन के लिए कार्बाइड लैंप का उपयोग किया जाता है, उदाहरण के लिए पोटोसी, [[बोलीविया]] के निकट चांदी की खानों में, गुफाओं और अन्य भूमिगत क्षेत्रों के अनुसन्धान करने वाले कुछ गुफाओं द्वारा अभी भी कार्बाइड लैंप का उपयोग किया जाता है,<ref>{{Cite web| url = http://www.teara.govt.nz/TheBush/BushAndMountainRecreation/Caving/4/en | title =Caving equipment and culture (from Te Ara Encyclopedia of New Zealand)}}</ref> चूँकि इस उपयोग में इन्हें तीव्रता से [[प्रकाश उत्सर्जक डायोड]] लाइटों द्वारा प्रतिस्थापित किया जा रहा है। | ||
प्रारंभिक ऑटोमोबाइल, मोटरसाइकिल और साइकिलों में [[हेडलाइट]] | प्रारंभिक ऑटोमोबाइल, मोटरसाइकिल और साइकिलों में [[हेडलाइट|हेडलाइट्स]] के रूप में कार्बाइड लैंप का भी बड़े स्तर पर उपयोग किया जाता था, किन्तु उनका स्थान पूर्ण रूप से इलेक्ट्रिक लैंप ने ग्रहण कर लिया है।<ref>{{Cite book| author = Clemmer, Gregg| title = American Miners' Carbide Lamps: A Collectors Guide to American Carbide Mine Lighting| publisher = Westernlore Publications| year = 1987}}</ref> | ||
'''अन्य उपयोग''' | '''अन्य उपयोग''' | ||
कैल्शियम कार्बाइड का उपयोग कभी-कभी एसिटिलीन के स्रोत के रूप में किया जाता है, जो [[ईथीलीन]] गैस की | कैल्शियम कार्बाइड का उपयोग कभी-कभी एसिटिलीन के स्रोत के रूप में किया जाता है, जो [[ईथीलीन]] गैस की जैसे परिपक्व होने वाला एजेंट है।<ref>{{Cite journal |author=Abeles, F. B. and Gahagan, H. E. III |year=1968 |title=Abscission: The Role of Ethylene, Ethylene Analogues, Carbon Dioxide, and Oxygen |journal=[[Plant Physiol.]] |volume=43 |issue=8 |pages=1255–1258 |doi=10.1104/pp.43.8.1255 |pmc=1087003 |pmid=16656908}}</ref> चूँकि, यह कुछ देशों में अवैध है, क्योंकि कैल्शियम कार्बाइड से एसिटिलीन के उत्पादन में, संदूषण से प्रायः फॉस्फीन और [[आर्सेन]] का उत्पादन होता है।<ref>{{Cite news|url=http://www.dnaindia.com/ahmedabad/1836343/report-bet-on-it-your-mango-is-ripened-using-carbide|title=इसपर शर्त लगाओ। आपका आम कार्बाइड से पकाया गया है|date=2013-05-18|work=dna|access-date=2018-08-25|language=en-US}}</ref><ref>{{Cite web|url=https://www.researchgate.net/publication/229429873|title=Eating Artificially Ripened Fruits is Harmful}}</ref> इन अशुद्धियों को एसिटिलीन गैस को अम्लीय [[कॉपर (II) सल्फेट]] समाधान के माध्यम से पारित करके विस्थापित किया जा सकता है, किन्तु, विकासशील देशों में, इस सावधानी की प्रायः उपेक्षा की जाती है। | ||
कैल्शियम कार्बाइड का उपयोग [[बिग-बैंग तोप]] जैसी खिलौना तोपों के साथ-साथ [[बांस की तोप]] | कैल्शियम कार्बाइड का उपयोग [[बिग-बैंग तोप]] जैसी खिलौना तोपों के साथ-साथ [[बांस की तोप|बांस की तोपों]] में भी किया जाता है। नीदरलैंड में नए साल के आसपास दूध मथने के लिए कैल्शियम कार्बाइड का उपयोग किया जाता है।<ref>{{cite web|title=कार्बिड शूटिंग एक पार्टी होने वाली है|url=http://www.ad.nl/dossier-rotterdam/carbidschieten-wordt-feest~af671013/|language=nl|publisher=[[Algemeen Dagblad]]|date=2016-12-24}}</ref> | ||
कैल्शियम कार्बाइड का उपयोग मिट्टी की नमी की मात्रा निर्धारित करने के लिए किया जाता है। जब मिट्टी और कैल्शियम कार्बाइड को | कैल्शियम कार्बाइड, कैल्शियम फॉस्फाइड के साथ, फ्लोटिंग, स्व-प्रज्वलित नौसेना [[ चमक |सिग्नल]] फ्लेयर्स में उपयोग किया जाता है, जैसे कि होम्स समुद्री जीवन संरक्षण एसोसिएशन द्वारा उत्पादित आदि। | ||
कैल्शियम कार्बाइड को व्यावसायिक रूप से | |||
कैल्शियम कार्बाइड का उपयोग मिट्टी की नमी की मात्रा निर्धारित करने के लिए किया जाता है। जब मिट्टी और कैल्शियम कार्बाइड को संवृत दबाव सिलेंडर में मिलाया जाता है, तो मिट्टी में पानी की मात्रा कैल्शियम कार्बाइड के साथ प्रतिक्रिया करके एसिटिलीन का त्याग करती है जिसके दबाव को नमी की मात्रा निर्धारित करने के लिए मापा जा सकता है।<ref>{{Cite web|first=Randhir |last=Singh|website=Civil Engineering Portal|title=Determining Water Content In Soil – Calcium Carbide Method|date=17 December 2008|url=https://www.engineeringcivil.com/determining-water-content-in-soil-calcium-carbide-method.html|access-date=7 September 2020}}</ref><ref>{{cite web|title=ASTM D4944-18, Standard Test Method for Field Determination of Water (Moisture) Content of Soil by the Calcium Carbide Gas Pressure Tester|author=ASTM International|publisher=ASTM International|url=https://www.astm.org/Standards/D4944.htm|access-date=7 September 2020}}</ref> | |||
कैल्शियम कार्बाइड को व्यावसायिक रूप से मोल विकर्षक के रूप में विक्रय जाता है I<ref>{{cite web|first=T.M.E.|last=du Bois|title=मोलेहिल तबाही|date=20 February 2014|url=https://dspace.library.uu.nl/handle/1874/290102|page=21|hdl=1874/290102}}</ref> जब यह पानी के संपर्क में आता है, तो उत्पन्न गैस मोल्स को दूर ले जाती है।<ref>{{Cite web|website=mysunnylawn.com|title=कार्बाइड से यार्ड के मस्सों से कैसे छुटकारा पाएं|url=http://www.mysunnylawn.com/a90851.php}}</ref> | |||
== संदर्भ == | == संदर्भ == | ||
Revision as of 10:58, 17 August 2023
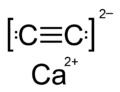
| |

| |
| Names | |
|---|---|
| Preferred IUPAC name
Calcium acetylide | |
| Systematic IUPAC name
Calcium ethynediide | |
| Other names
Calcium percarbide
Calcium carbide Calcium dicarbide | |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
| EC Number |
|
PubChem CID
|
|
| UNII | |
| |
| |
| Properties | |
| CaC2 | |
| Molar mass | 64.099 g/mol |
| Appearance | White powder to grey/black crystals |
| Density | 2.22 g/cm3 |
| Melting point | 2,160 °C (3,920 °F; 2,430 K) |
| Boiling point | 2,300 °C (4,170 °F; 2,570 K) |
| Reacts to produce Acetylene | |
| Structure[1] | |
| Tetragonal (I phase) Monoclinic (II phase) Monoclinic (III phase) | |
| I4/mmm (I phase) C2/c (II phase) C2/m (III phase) | |
| 6 | |
| Thermochemistry | |
Std molar
entropy (S⦵298) |
70 J·mol−1·K−1 |
Std enthalpy of
formation (ΔfH⦵298) |
−63 kJ·mol−1 |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
Main hazards
|
Reacts with water to release acetylene gas[2] |
| GHS labelling: | |
 
| |
| Danger | |
| H260 | |
| NFPA 704 (fire diamond) | |
| 305 °C (581 °F; 578 K) (acetylene) | |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
कैल्शियम कार्बाइड, जिसे कैल्शियम एसिटाइलाइड भी कहा जाता है, CaC2 रासायनिक सूत्र के साथ रासायनिक यौगिक होते है। औद्योगिक रूप से इसका मुख्य उपयोग एसिटिलीन और कैल्शियम सायनामाइड के उत्पादन में होता है।[3]
शुद्ध सामग्री रंगहीन होती है, किन्तु रासायनिक शुद्धता कैल्शियम कार्बाइड के टुकड़े भूरे रंग के होते हैं और इनमें लगभग 80-85% CaC2 (शेष CaO (कैल्शियम ऑक्साइड), Ca3P2 (कैल्शियम फॉस्फाइड), CaS (कैल्शियम सल्फाइड), Ca3N2 (कैल्शियम नाइट्राइड), SiC (सिलिकन कार्बाइड), आदि) होता है। नमी की उपस्थिति में, तकनीकी-ग्रेड कैल्शियम कार्बाइड लहसुन की याद दिलाती है एवं अप्रिय गंध उत्सर्जित करती है।[4]
कैल्शियम कार्बाइड के अनुप्रयोगों में एसिटिलीन गैस का निर्माण, कार्बाइड लैंप में एसिटिलीन का उत्पादन, उर्वरक के लिए रसायनों का निर्माण और स्टील बनाना सम्मिलित है।
उत्पादन
कैल्शियम कार्बाइड का उत्पादन औद्योगिक रूप से इलेक्ट्रिक आर्क फर्नेस में लगभग 2,200 °C (3,990 °F) पर चूने और कोक के मिश्रण से किया जाता है I[5] यह एंडोथर्मिक प्रतिक्रिया है, जिसमें कार्बन मोनोऑक्साइड को निकालने के लिए 110 kilocalories (460 kJ) और उच्च तापमान की आवश्यकता होती है।[6] यह विधि 1892 में अपने आविष्कार के पश्चात् से परिवर्तित नहीं हुई है:
- CaO + 3 C → CaC2 + CO
इस प्रतिक्रिया के लिए आवश्यक उच्च तापमान पारंपरिक दहन द्वारा व्यावहारिक रूप से प्राप्त नहीं किया जा सकता है, इसलिए प्रतिक्रिया ग्रेफाइट इलेक्ट्रोड के साथ इलेक्ट्रिक आर्क भट्टी में की जाती है। उत्पादित कार्बाइड उत्पाद में सामान्यतः वजन के अनुसार लगभग 80% कैल्शियम कार्बाइड होता है। कार्बाइड को पीसकर छोटी-छोटी गांठें बनाई जाती हैं जो कुछ मिमी से 50 मिमी तक हो सकती हैं। अशुद्धियाँ सूक्ष्म अंशों में केंद्रित होती हैं। उत्पाद की CaC2 सामग्री का परीक्षण हाइड्रोलिसिस पर उत्पादित एसिटिलीन की मात्रा को मापकर किया जाता है। उदाहरण के आधार पर, मोटे अंशों की सामग्री के लिए ब्रिटिश और जर्मन मानक क्रमशः 295 L/kg और 300 L/kg हैं (101 केपीए दबाव पर और 20 °C (68 °F) तापमान)। कार्बाइड में उपस्थित अशुद्धियों में कैल्शियम फॉस्फाइड सम्मिलित होता है, जो हाइड्रोलाइज्ड होने पर फॉस्फीन उत्पन्न करता है।[7]
यह प्रतिक्रिया रसायन विज्ञान में औद्योगिक क्रांति का एक महत्वपूर्ण भाग थी, और 20 वीं शताब्दी के प्रारम्भ से पूर्व नायग्रा फॉल्स में अधिक मात्रा में उत्पादित जलविद्युत ऊर्जा के परिणामस्वरूप संयुक्त राज्य अमेरिका में संभव हो गई थी।[8] इलेक्ट्रिक आर्क फर्नेस विधि का अनुसन्धान 1892 में टी. एल. विल्सन द्वारा किया गया था, और स्वतंत्र रूप से उसी वर्ष एच. मोइसन द्वारा भी किया गया था।[9][10][11] जज्से, बोस्निया और हर्जेगोविना में, ऑस्ट्रियाई उद्योगपति जोसेफ क्रान्ज़ और उनकी बोस्निशे-इलेक्ट्रिज़िटेट्स एजी कंपनी, जिसका उत्तराधिकारी पश्चात् में इलेक्ट्रो-बोस्ना बन गया I1899 में यूरोप में कैल्शियम कार्बाइड के उत्पादन के लिए सबसे बड़ी रासायनिक फैक्टरी प्रारंभ की थी। फैक्टरी के लिए विद्युत् की आपूर्ति करने के लिए प्लिवा नदी पर 8 मेगावाट की स्थापित क्षमता वाला जलविद्युत पावर स्टेशन बनाया गया था, जो दक्षिणपूर्व यूरोप में प्रथम पावर स्टेशन था, और 24 मार्च 1899 को प्रारम्भ हो गया था।[12]
क्रिस्टल संरचना
शुद्ध कैल्शियम कार्बाइड रंगहीन ठोस होता है। कक्ष के तापमान पर सामान्य क्रिस्टलीय रूप विकृत सेंधा नमक संरचना है, जिसमें C22− इकाइयाँ समानांतर होती हैं।[13] तीन भिन्न-भिन्न बहुरूपता (सामग्री विज्ञान) हैं जो कक्ष के तापमान पर प्रदर्शित होती हैं: चतुष्कोणीय संरचना और दो भिन्न-भिन्न मोनोक्लिनिक संरचनाएँ आदि।[1]
अनुप्रयोग
एसिटिलीन का उत्पादन
पानी के साथ कैल्शियम कार्बाइड की प्रतिक्रिया, एसिटिलीन और कैल्शियम हाइड्रॉक्साइड का उत्पादन का उत्पादन करती है,[5] इसका अनुसन्धान 1862 में फ्रेडरिक वॉहलर ने किया था।
यह प्रतिक्रिया एसिटिलीन के औद्योगिक निर्माण का आधार थी, और कैल्शियम कार्बाइड का प्रमुख औद्योगिक उपयोग है।
एसिटिलीन मुख्य रूप से मीथेन के आंशिक दहन से निर्मित होता है या हाइड्रोकार्बन के टूटने से एथिलीन धारा में साइड उत्पाद के रूप में प्रदर्शित होता है। इस प्रकार प्रतिवर्ष लगभग 400,000 टन का उत्पादन होता है (एसिटिलीन देखें)।
चीन में, कैल्शियम कार्बाइड से प्राप्त एसिटिलीन रासायनिक उद्योग के लिए कच्चा माल बना हुआ है, विशेष रूप से पॉलीविनाइल क्लोराइड के उत्पादन के लिए आयातित तेल के उपयोग की तुलना में स्थानीय रूप से उत्पादित एसिटिलीन अधिक लाभदायी है।[14] चीन में कैल्शियम कार्बाइड का उत्पादन बढ़ रहा है। 2005 में उत्पादन 8.94 मिलियन टन था, किन्तु उत्पादन क्षमता 17 मिलियन टन थी।[15]
संयुक्त राज्य अमेरिका, यूरोप और जापान में, कैल्शियम कार्बाइड का उपभोग सामान्यतः कम होता जा रहा है।[16] 1990 के दशक के समय अमेरिका में उत्पादन स्तर 236,000 टन प्रति वर्ष था।[13]
कैल्शियम सायनामाइड का उत्पादन
कैल्शियम कार्बाइड उच्च तापमान पर नाइट्रोजन के साथ प्रतिक्रिया करके कैल्शियम सायनामाइड बनाता है:[5]
- CaC2 + N2 → CaCN2 + C
सामान्यतः नाइट्रोलाइम के रूप में जाना जाने वाला कैल्शियम साइनामाइड का उपयोग उर्वरक के रूप में किया जाता है। यह सायनामाइड, H2NCN में जल अपघटित हो जाता है I[5]
इस्पात निर्माण
कैल्शियम कार्बाइड का उपयोग किया जाता है:
- लोहे के निर्गंधीकरण में (पिग आयरन, [[कच्चा लोहा]] और स्टील)[7] उपयोग किया जाता है I
- अर्थशास्त्र के आधार पर, इस्पात निर्माण में स्क्रैप अनुपात को तरल लोहे तक बढ़ाने के लिए ईंधन के रूप में उपयोग किया जाता है I
- लैडल (धातुकर्म) उपचार सुविधाओं में शक्तिशाली डीऑक्सीडाइज़र के रूप में उपयोग किया जाता है I
कार्बाइड लैंप
कैल्शियम कार्बाइड का उपयोग कार्बाइड लैंप में किया जाता है। कार्बाइड पर द्रव गिरने से एसिटिलीन गैस निकलती है, जो दहन के पश्चात प्रकाश उत्पन्न करती है। किन्तु ये लैंप मोमबत्तियों की अपेक्षा अधिक स्थिर और तीव्र प्रकाश उत्पन्न करते थे, ये कोयला खानों में हानिकारक थे, जहां ज्वलनशील मीथेन गैस ने इन्हें गंभीर बना दिया था। कोयला खानों में ज्वलनशील गैसों की उपस्थिति के कारण डेवी लैंप जैसे खनिक सुरक्षा लैंप का उपयोग किया गया, जिसमें तार का गेज मीथेन प्रज्वलन के संकट को कम करता है। कार्बाइड लैंप का उपयोग अभी भी स्लेट, तांबे और टिन की खानों में बड़े स्तर पर किया जाता था जहां मीथेन कोई गंभीर संकट नहीं है। अधिकांश खनिकों के लैंप को अब इलेक्ट्रिक हेडलैम्प (आउटडोर) ने परिवर्तित कर दिया है।
कुछ निम्न सक्षम देशों में खनन के लिए कार्बाइड लैंप का उपयोग किया जाता है, उदाहरण के लिए पोटोसी, बोलीविया के निकट चांदी की खानों में, गुफाओं और अन्य भूमिगत क्षेत्रों के अनुसन्धान करने वाले कुछ गुफाओं द्वारा अभी भी कार्बाइड लैंप का उपयोग किया जाता है,[17] चूँकि इस उपयोग में इन्हें तीव्रता से प्रकाश उत्सर्जक डायोड लाइटों द्वारा प्रतिस्थापित किया जा रहा है।
प्रारंभिक ऑटोमोबाइल, मोटरसाइकिल और साइकिलों में हेडलाइट्स के रूप में कार्बाइड लैंप का भी बड़े स्तर पर उपयोग किया जाता था, किन्तु उनका स्थान पूर्ण रूप से इलेक्ट्रिक लैंप ने ग्रहण कर लिया है।[18]
अन्य उपयोग
कैल्शियम कार्बाइड का उपयोग कभी-कभी एसिटिलीन के स्रोत के रूप में किया जाता है, जो ईथीलीन गैस की जैसे परिपक्व होने वाला एजेंट है।[19] चूँकि, यह कुछ देशों में अवैध है, क्योंकि कैल्शियम कार्बाइड से एसिटिलीन के उत्पादन में, संदूषण से प्रायः फॉस्फीन और आर्सेन का उत्पादन होता है।[20][21] इन अशुद्धियों को एसिटिलीन गैस को अम्लीय कॉपर (II) सल्फेट समाधान के माध्यम से पारित करके विस्थापित किया जा सकता है, किन्तु, विकासशील देशों में, इस सावधानी की प्रायः उपेक्षा की जाती है।
कैल्शियम कार्बाइड का उपयोग बिग-बैंग तोप जैसी खिलौना तोपों के साथ-साथ बांस की तोपों में भी किया जाता है। नीदरलैंड में नए साल के आसपास दूध मथने के लिए कैल्शियम कार्बाइड का उपयोग किया जाता है।[22]
कैल्शियम कार्बाइड, कैल्शियम फॉस्फाइड के साथ, फ्लोटिंग, स्व-प्रज्वलित नौसेना सिग्नल फ्लेयर्स में उपयोग किया जाता है, जैसे कि होम्स समुद्री जीवन संरक्षण एसोसिएशन द्वारा उत्पादित आदि।
कैल्शियम कार्बाइड का उपयोग मिट्टी की नमी की मात्रा निर्धारित करने के लिए किया जाता है। जब मिट्टी और कैल्शियम कार्बाइड को संवृत दबाव सिलेंडर में मिलाया जाता है, तो मिट्टी में पानी की मात्रा कैल्शियम कार्बाइड के साथ प्रतिक्रिया करके एसिटिलीन का त्याग करती है जिसके दबाव को नमी की मात्रा निर्धारित करने के लिए मापा जा सकता है।[23][24]
कैल्शियम कार्बाइड को व्यावसायिक रूप से मोल विकर्षक के रूप में विक्रय जाता है I[25] जब यह पानी के संपर्क में आता है, तो उत्पन्न गैस मोल्स को दूर ले जाती है।[26]
संदर्भ
- ↑ 1.0 1.1 Konar, Sumit; Nylén, Johanna; Svensson, Gunnar; Bernin, Diana; Edén, Mattias; Ruschewitz, Uwe; Häussermann, Ulrich (2016). "The many phases of CaC2". Journal of Solid State Chemistry. Elsevier BV. 239: 204–213. Bibcode:2016JSSCh.239..204K. doi:10.1016/j.jssc.2016.04.030. ISSN 0022-4596.
- ↑ NFPA Hazard Rating Information for Common Chemicals. Northeastern University
- ↑ Patnaik, Pradyot (2003). अकार्बनिक रासायनिक यौगिकों की पुस्तिका. McGraw-Hill. ISBN 0-07-049439-8.
- ↑ Vincoli, Jeffrey Wayne (25 November 1996). खतरनाक रसायनों के लिए जोखिम प्रबंधन. CRC Press. p. 429. ISBN 978-1-56670-200-3.
- ↑ 5.0 5.1 5.2 5.3 Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 298. ISBN 978-0-08-037941-8.
- ↑ Calculated from data in the CRC Handbook of Chemistry and Physics.
- ↑ 7.0 7.1 Calcium Carbide[permanent dead link], Bernhard Langhammer, Ullmann's Encyclopedia of Industrial Chemistry, Wiley Interscience. (Subscription required)
- ↑ Freeman, Horace (1919). "सायनामाइड का निर्माण". The Chemical News and the Journal of Physical Science. 117: 232.
- ↑ Morehead, J. T. and de Chalmot, G. (1896). "The Manufacture of Calcium Carbide". Journal of the American Chemical Society. 18 (4): 311–331. doi:10.1021/ja02090a001.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ Moissan, H. (1892). "Chimie Minérale – Description d'un nouveau four électrique". Comptes rendus hebdomadaires des séances de l'Académie des sciences. 115: 1031.
- ↑ Renouf, Edward (1899). "एसिटिलीन का उपयोग". Popular Science Monthly: 335–347.
- ↑ "Zgrada Prve hidrocentrale na Balkanu - Komisija za očuvanje nacionalnih spomenika". old.kons.gov.ba (in srpskohrvatski / српскохрватски). KONS. Retrieved 15 March 2019.
- ↑ 13.0 13.1 Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ Dun, Ya (2006-01-23). "पीवीसी उद्योग में समस्याएं". Hong Kong Trade Development Council. Archived from the original on 2007-12-28.
{{cite web}}: CS1 maint: bot: original URL status unknown (link) - ↑ "सरकार कैल्शियम कार्बाइड क्षेत्र के विकास पर अंकुश लगाने के लिए कदम उठा रही है". China Daily via BusyTrade.com. 2007-05-16. Archived from the original on 2007-02-11.
{{cite news}}: CS1 maint: bot: original URL status unknown (link) - ↑ Lacson, Jamie; Schlag, Stefan; Toki, Goro (December 2004). "कैल्शियम कार्बाइड". SRI Consulting.
- ↑ "Caving equipment and culture (from Te Ara Encyclopedia of New Zealand)".
- ↑ Clemmer, Gregg (1987). American Miners' Carbide Lamps: A Collectors Guide to American Carbide Mine Lighting. Westernlore Publications.
- ↑ Abeles, F. B. and Gahagan, H. E. III (1968). "Abscission: The Role of Ethylene, Ethylene Analogues, Carbon Dioxide, and Oxygen". Plant Physiol. 43 (8): 1255–1258. doi:10.1104/pp.43.8.1255. PMC 1087003. PMID 16656908.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ "इसपर शर्त लगाओ। आपका आम कार्बाइड से पकाया गया है". dna (in English). 2013-05-18. Retrieved 2018-08-25.
- ↑ "Eating Artificially Ripened Fruits is Harmful".
- ↑ "कार्बिड शूटिंग एक पार्टी होने वाली है" (in Nederlands). Algemeen Dagblad. 2016-12-24.
- ↑ Singh, Randhir (17 December 2008). "Determining Water Content In Soil – Calcium Carbide Method". Civil Engineering Portal. Retrieved 7 September 2020.
- ↑ ASTM International. "ASTM D4944-18, Standard Test Method for Field Determination of Water (Moisture) Content of Soil by the Calcium Carbide Gas Pressure Tester". ASTM International. Retrieved 7 September 2020.
- ↑ du Bois, T.M.E. (20 February 2014). "मोलेहिल तबाही". p. 21. hdl:1874/290102.
- ↑ "कार्बाइड से यार्ड के मस्सों से कैसे छुटकारा पाएं". mysunnylawn.com.
बाहरी संबंध
- Calcium Carbide & Acetylene at The Periodic Table of Videos (University of Nottingham)
- Calcium Carbide Manufacturing
- 2008 Material Safety Data Sheet

