टाइरोसिन किनसे: Difference between revisions
m (added Category:Vigyan Ready using HotCat) |
No edit summary |
||
| (One intermediate revision by one other user not shown) | |||
| Line 45: | Line 45: | ||
तथापि प्रोटीन टाइरोसिन काइनेज की संभावित भूमिका चूहों में एंडोटॉक्सिन के कारण संचार विफलता और अंग की शिथिलता की स्थिति में है, जहां अवरोधक टाइरफोस्टिन और [[genistein|जेनिस्टिन]] के प्रभाव प्रोटीन टायरोसिन काइनेज के साथ सम्मिलित होते हैं।<ref name="Ruetten_1997"/> कोशिकाओं की झिल्लियों में उपस्थित रिसेप्टर्स द्वारा प्राप्त परिवेश में सिग्नल कोशिका साइटोप्लाज्म में संचारित होते हैं। बाए एट अल (2009), के अनुसार रिसेप्टर टाइरोसिन काइनेसेस के कारण ट्रांसमेम्ब्रेन सिग्नलिंग, परस्पर क्रियाओं पर अत्यधिक निर्भर करता है, उदाहरण के लिए, एसएच2 प्रोटीन डोमेन द्वारा मध्यस्थता, प्रयोग के माध्यम से यह निर्धारित किया गया है कि एसएच2 प्रोटीन डोमेन चयनात्मकता टाइरोसिन काइनेज से संयोजित कोशिकीय प्रक्रियाओं की मध्यस्थता में कार्यात्मक है। रिसेप्टर टाइरोसिन काइनेसेस इस विधि से, वृद्धि कारक रिसेप्टर सिग्नलिंग को प्रभावित कर सकता है। यह अधिक वास्तविक कोशिकीय संचार कार्यों मेटाज़ोन्स में से है।<ref name="Dengjel_2009">{{cite journal | vauthors = Dengjel J, Kratchmarova I, Blagoev B | title = रिसेप्टर टाइरोसिन किनेज सिग्नलिंग: क्वांटिटेटिव प्रोटिओमिक्स से एक दृश्य| journal = Molecular BioSystems | volume = 5 | issue = 10 | pages = 1112–1121 | date = October 2009 | pmid = 19756300 | doi = 10.1039/b909534a | url = https://zenodo.org/record/895954 }}</ref> | तथापि प्रोटीन टाइरोसिन काइनेज की संभावित भूमिका चूहों में एंडोटॉक्सिन के कारण संचार विफलता और अंग की शिथिलता की स्थिति में है, जहां अवरोधक टाइरफोस्टिन और [[genistein|जेनिस्टिन]] के प्रभाव प्रोटीन टायरोसिन काइनेज के साथ सम्मिलित होते हैं।<ref name="Ruetten_1997"/> कोशिकाओं की झिल्लियों में उपस्थित रिसेप्टर्स द्वारा प्राप्त परिवेश में सिग्नल कोशिका साइटोप्लाज्म में संचारित होते हैं। बाए एट अल (2009), के अनुसार रिसेप्टर टाइरोसिन काइनेसेस के कारण ट्रांसमेम्ब्रेन सिग्नलिंग, परस्पर क्रियाओं पर अत्यधिक निर्भर करता है, उदाहरण के लिए, एसएच2 प्रोटीन डोमेन द्वारा मध्यस्थता, प्रयोग के माध्यम से यह निर्धारित किया गया है कि एसएच2 प्रोटीन डोमेन चयनात्मकता टाइरोसिन काइनेज से संयोजित कोशिकीय प्रक्रियाओं की मध्यस्थता में कार्यात्मक है। रिसेप्टर टाइरोसिन काइनेसेस इस विधि से, वृद्धि कारक रिसेप्टर सिग्नलिंग को प्रभावित कर सकता है। यह अधिक वास्तविक कोशिकीय संचार कार्यों मेटाज़ोन्स में से है।<ref name="Dengjel_2009">{{cite journal | vauthors = Dengjel J, Kratchmarova I, Blagoev B | title = रिसेप्टर टाइरोसिन किनेज सिग्नलिंग: क्वांटिटेटिव प्रोटिओमिक्स से एक दृश्य| journal = Molecular BioSystems | volume = 5 | issue = 10 | pages = 1112–1121 | date = October 2009 | pmid = 19756300 | doi = 10.1039/b909534a | url = https://zenodo.org/record/895954 }}</ref> | ||
== विनियमन == | == विनियमन == | ||
| Line 129: | Line 129: | ||
गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर (जीआईएसटी) कैंसर के कीमोथेरेपी उपचार के लिए जाने जाते हैं और उन्नत स्थितियों में किसी भी प्रकार की चिकित्सा (2001 में) का उत्तर नहीं देते हैं। यद्यपि, मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रॉमल ट्यूमर वाले रोगी के उपचार में टायरोसिन काइनेज अवरोधक एसटीआई 571 (इमैटिनिब) प्रभावी है।<ref name="Joensuu_2001">{{cite journal | vauthors = Joensuu H, Roberts PJ, Sarlomo-Rikala M, Andersson LC, Tervahartiala P, Tuveson D, Silberman S, Capdeville R, Dimitrijevic S, Druker B, Demetri GD | display-authors = 6 | title = मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर वाले रोगी में टाइरोसिन किनेज अवरोधक STI571 का प्रभाव| journal = The New England Journal of Medicine | volume = 344 | issue = 14 | pages = 1052–1056 | date = April 2001 | pmid = 11287975 | doi = 10.1056/NEJM200104053441404 }</ref> गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर में मेसेंकाईमल नियोप्लाज्म्स का समूह होता है जो गैस्ट्रोइंटेस्टाइनल ट्रैक्ट में संयोजी-ऊतक बनाने वाली कोशिकाओं के अग्रदूतों से बनता है।<ref name="Joensuu_2001"/> इनमें से अधिकतर ट्यूमर उदर में पाए जाते हैं, यद्यपि वे छोटी आंत में या आंतों के मार्ग में कहीं और भी स्थित हो सकते हैं। इन ट्यूमर की कोशिकाओं में वृद्धि कारक रिसेप्टर होता है जो टाइरोसिन काइनेज गतिविधि से जुड़ा होता है।<ref name="Joensuu_2001"/> इस वृद्धि कारक रिसेप्टर को [[ सी किट |सी किट]] कहा जाता है और यह प्रोटो-ओन्कोजीन (सी-किट) द्वारा निर्मित होता है। सी-किट का उत्परिवर्तन टाइरोसिन काइनेज की संवैधानिक गतिविधि का कारण बनता है, जिसके परिणामस्वरूप कैंसर गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर होता है। सी-किट म्यूटेशन के परिणामों में अप्रतिबंधित टाइरोसिन काइनेज गतिविधि और कोशिका प्रसार, सी-किट का अनियमित फॉस्फोराइलेशन और कुछ संचार मार्गों का विघटन सम्मिलित है।<ref name="Joensuu_2001"/> इमैटिनिब के साथ उपचार गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर में असामान्य कोशिका सिग्नलिंग तंत्र को बाधित कर सकता है। इसके परिणामस्वरूप रोगियों में महत्वपूर्ण प्रतिक्रिया होती है और निरंतर रोग नियंत्रण होता है। 2001 तक यह संदेह नहीं रह गया था कि यह अवरोधक मनुष्यों में प्रभावी और सुरक्षित हो सकता है।<ref name="Wiley_2001"/> इसी प्रकार, प्रोटीन टायरोसिन काइनेज अवरोधक एसटीआई 571 ट्यूमर के भौतिक आकार को कम करने के लिए पाया गया; परीक्षण के 4 माह में उनका आकार लगभग 65% कम हो गया, और लगातार कम होता गया। नए घाव प्रकट नहीं हुए, और कई यकृत मेटास्टेस पूरी रूप से अस्तित्वहीन हो गए। अध्ययन में सम्मिलित रोगी उपचार के पश्चात स्वस्थ रहा।<ref name="Joensuu_2001"/> उन्नत गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर के लिए उपचार का कोई प्रभावी साधन नहीं है, किन्तु एसटीआई 571 प्रारंभिक चरण के कैंसर में प्रभावी उपचार का प्रतिनिधित्व करता है, जो प्रतिकूल टाइरोसिन काइनेज गतिविधि को अवरोधित करके संवैधानिक रूप से सक्रिय सी-किट से संयोजित है।<ref name="Joensuu_2001"/> | गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर (जीआईएसटी) कैंसर के कीमोथेरेपी उपचार के लिए जाने जाते हैं और उन्नत स्थितियों में किसी भी प्रकार की चिकित्सा (2001 में) का उत्तर नहीं देते हैं। यद्यपि, मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रॉमल ट्यूमर वाले रोगी के उपचार में टायरोसिन काइनेज अवरोधक एसटीआई 571 (इमैटिनिब) प्रभावी है।<ref name="Joensuu_2001">{{cite journal | vauthors = Joensuu H, Roberts PJ, Sarlomo-Rikala M, Andersson LC, Tervahartiala P, Tuveson D, Silberman S, Capdeville R, Dimitrijevic S, Druker B, Demetri GD | display-authors = 6 | title = मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर वाले रोगी में टाइरोसिन किनेज अवरोधक STI571 का प्रभाव| journal = The New England Journal of Medicine | volume = 344 | issue = 14 | pages = 1052–1056 | date = April 2001 | pmid = 11287975 | doi = 10.1056/NEJM200104053441404 }</ref> गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर में मेसेंकाईमल नियोप्लाज्म्स का समूह होता है जो गैस्ट्रोइंटेस्टाइनल ट्रैक्ट में संयोजी-ऊतक बनाने वाली कोशिकाओं के अग्रदूतों से बनता है।<ref name="Joensuu_2001"/> इनमें से अधिकतर ट्यूमर उदर में पाए जाते हैं, यद्यपि वे छोटी आंत में या आंतों के मार्ग में कहीं और भी स्थित हो सकते हैं। इन ट्यूमर की कोशिकाओं में वृद्धि कारक रिसेप्टर होता है जो टाइरोसिन काइनेज गतिविधि से जुड़ा होता है।<ref name="Joensuu_2001"/> इस वृद्धि कारक रिसेप्टर को [[ सी किट |सी किट]] कहा जाता है और यह प्रोटो-ओन्कोजीन (सी-किट) द्वारा निर्मित होता है। सी-किट का उत्परिवर्तन टाइरोसिन काइनेज की संवैधानिक गतिविधि का कारण बनता है, जिसके परिणामस्वरूप कैंसर गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर होता है। सी-किट म्यूटेशन के परिणामों में अप्रतिबंधित टाइरोसिन काइनेज गतिविधि और कोशिका प्रसार, सी-किट का अनियमित फॉस्फोराइलेशन और कुछ संचार मार्गों का विघटन सम्मिलित है।<ref name="Joensuu_2001"/> इमैटिनिब के साथ उपचार गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर में असामान्य कोशिका सिग्नलिंग तंत्र को बाधित कर सकता है। इसके परिणामस्वरूप रोगियों में महत्वपूर्ण प्रतिक्रिया होती है और निरंतर रोग नियंत्रण होता है। 2001 तक यह संदेह नहीं रह गया था कि यह अवरोधक मनुष्यों में प्रभावी और सुरक्षित हो सकता है।<ref name="Wiley_2001"/> इसी प्रकार, प्रोटीन टायरोसिन काइनेज अवरोधक एसटीआई 571 ट्यूमर के भौतिक आकार को कम करने के लिए पाया गया; परीक्षण के 4 माह में उनका आकार लगभग 65% कम हो गया, और लगातार कम होता गया। नए घाव प्रकट नहीं हुए, और कई यकृत मेटास्टेस पूरी रूप से अस्तित्वहीन हो गए। अध्ययन में सम्मिलित रोगी उपचार के पश्चात स्वस्थ रहा।<ref name="Joensuu_2001"/> उन्नत गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर के लिए उपचार का कोई प्रभावी साधन नहीं है, किन्तु एसटीआई 571 प्रारंभिक चरण के कैंसर में प्रभावी उपचार का प्रतिनिधित्व करता है, जो प्रतिकूल टाइरोसिन काइनेज गतिविधि को अवरोधित करके संवैधानिक रूप से सक्रिय सी-किट से संयोजित है।<ref name="Joensuu_2001"/> | ||
== अवरोधक == | == अवरोधक == | ||
| Line 209: | Line 209: | ||
[[Category:Collapse templates|Tyrosine Kinase]] | [[Category:Collapse templates|Tyrosine Kinase]] | ||
[[Category:Created On 09/06/2023|Tyrosine Kinase]] | [[Category:Created On 09/06/2023|Tyrosine Kinase]] | ||
[[Category:Lua-based templates]] | |||
[[Category:Machine Translated Page|Tyrosine Kinase]] | [[Category:Machine Translated Page|Tyrosine Kinase]] | ||
[[Category:Navigational boxes| ]] | [[Category:Navigational boxes| ]] | ||
| Line 216: | Line 217: | ||
[[Category:Portal templates with redlinked portals|Tyrosine Kinase]] | [[Category:Portal templates with redlinked portals|Tyrosine Kinase]] | ||
[[Category:Short description with empty Wikidata description|Tyrosine Kinase]] | [[Category:Short description with empty Wikidata description|Tyrosine Kinase]] | ||
[[Category:Vigyan Ready]] | [[Category:Templates Vigyan Ready]] | ||
[[Category:Templates that add a tracking category]] | |||
[[Category:Templates that generate short descriptions]] | |||
[[Category:Templates using TemplateData]] | |||
Latest revision as of 09:13, 5 September 2023
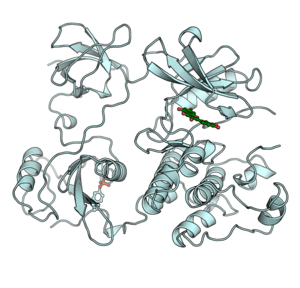
| Protein tyrosine kinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Identifiers | |||||||||
| Symbol | Pkinase_Tyr | ||||||||
| Pfam | PF07714 | ||||||||
| InterPro | IPR001245 | ||||||||
| SMART | TyrKc | ||||||||
| PROSITE | PDOC00629 | ||||||||
| SCOP2 | 1apm / SCOPe / SUPFAM | ||||||||
| OPM superfamily | 186 | ||||||||
| OPM protein | 2k1k | ||||||||
| CDD | cd00192 | ||||||||
| Membranome | 3 | ||||||||
| |||||||||
टाइरोसिन काइनेज एंजाइम होता है जो एडेनोसाइन ट्रायफ़ोस्फेट से फॉस्फेट समूह को कोशिका के भीतर विशिष्ट प्रोटीन के टायरोसिन अवशेषों में स्थानांतरित कर सकता है। यह कई कोशिकीय कार्यों में ऑन अथवा ऑफ स्विच के रूप में कार्य करता है।
टाइरोसिन काइनेसेस एंजाइमों के बड़े वर्ग से संबंधित होते हैं, जिन्हें प्रोटीन काइनेसेस के रूप में जाना जाता है, जो फॉस्फेट को सेरीन और थ्रेओनीन जैसे अन्य अमीनो अम्ल से भी संयोजित करते हैं। काइनेसेस द्वारा प्रोटीन का फॉस्फोरिलन कोशिका (सिग्नल ट्रांसडक्शन) के भीतर संकेतों को संचारित करने और कोशिका विभाजन जैसी कोशिकीय गतिविधि को विनियमित करने के लिए महत्वपूर्ण तंत्र होता है।
प्रोटीन काइनेज उत्परिवर्तित हो सकते हैं, प्रारम्भ स्थिति में स्टक हो सकते हैं, और कोशिका के अनियमित विकास का कारण बन सकते हैं, जो कैंसर के विकास के लिए आवश्यक चरण है। इसलिए, काइनेज अवरोधक जैसे इमैटिनिब और ओसिमर्टिनिब, अधिकांशतः कैंसर के उपचार में प्रभावी होते हैं।
अधिकांश टाइरोसिन काइनेसेस में संबद्ध प्रोटीन टाइरोसिन फॉस्फेट होता है, जो फॉस्फेट समूह को विस्थापित कर देता है।
प्रतिक्रिया
प्रोटीन काइनेसेस एंजाइमों का समूह है जिसमें उत्प्रेरक सबयूनिट होता है जो गामा (टर्मिनल) फॉस्फेट को न्यूक्लियोसाइड ट्राइफॉस्फेट (अधिकांशतः एटीपी) से प्रोटीन सब्सट्रेट साइड-चेन में अधिक अमीनो अम्ल अवशेषों में स्थानांतरित करता है, जिसके परिणामस्वरूप प्रोटीन कार्य को प्रभावित करने वाला परिवर्तनकारी परिवर्तन होता है। एंजाइम दो व्यापक वर्गों में आते हैं, जो सब्सट्रेट विशिष्टता सेरीन/थ्रेओनीन-विशिष्ट और टायरोसिन-विशिष्ट (इस लेख का विषय) के संबंध में विशेषता रखते हैं।[1]
कार्य
काइनेज एंजाइमों का बड़ा समूह है जो न्यूक्लियोसाइड ट्राइफॉस्फेट दाता, जैसे एटीपी, से स्वीकर्ता अणु के लिए फॉस्फोरिल समूह के हस्तांतरण को उत्प्रेरित करने के लिए उत्तरदायी है।[2] टाइरोसिन काइनेसेस प्रोटीन में टाइरोसिन अवशेषों के फॉस्फोरिलन को उत्प्रेरित करता है।[2] जिसके प्रतिकार में टाइरोसिन अवशेषों का फॉस्फोरिलन प्रोटीन के कार्य में परिवर्तन का कारण बनता है जिसमें वे निहित होते हैं।[2]
टाइरोसिन अवशेषों पर फॉस्फोरिलन प्रोटीन में एंजाइम गतिविधि, उपकोशिकीय स्थानीयकरण और अणुओं के मध्य परस्पर क्रिया जैसे गुणों की विस्तृत श्रृंखला को नियंत्रित करता है।[3] इसके अतिरिक्त, टाइरोसिन काइनेसेस कई सिग्नल ट्रांसडक्शन कैस्केड में कार्य करता है, जिसमें बाह्यकोशिकीय सिग्नल कोशिका झिल्ली के माध्यम से कोशिका द्रव्य और अधिकांशतः कोशिका केंद्रक तक प्रेषित होते हैं, जहां जीन प्रकटन को संशोधित किया जा सकता है।[3] अंत में उत्परिवर्तन के कारण कुछ टाइरोसिन काइनेसेस संवैधानिक रूप से सक्रिय हो सकते हैं, निरंतर कार्यात्मक अवस्था जो कैंसर के प्रारम्भ अथवा प्रगति में योगदान कर सकती है।
टाइरोसिन काइनेसेस विभिन्न प्रकार की प्रक्रियाओं, मार्गों और क्रियाओं में कार्य करते हैं, और शरीर में महत्वपूर्ण घटनाओं के लिए उत्तरदायी होते हैं। रिसेप्टर टाइरोसिन काइनेसेस ट्रांसमेम्ब्रेन सिग्नलिंग में कार्य करते हैं, जबकि कोशिका कार्य के भीतर टाइरोसिन काइनेसेस केंद्रक तक सिग्नल ट्रांसडक्शन में कार्य करते हैं।<[4] केंद्रक में टायरोसिन काइनेज गतिविधि में कोशिका-चक्र नियंत्रण और प्रतिलेखन कारकों के गुण सम्मिलित होते हैं।[3] इस प्रकार, वास्तव में, टाइरोसिन काइनेज गतिविधि माइटोजेनेसिस अथवा कोशिका में समसूत्रण के प्रेरण में सम्मिलित होती है; इस प्रक्रिया के समय साइटोसोल में प्रोटीन और केंद्रक में प्रोटीन टाइरोसिन अवशेषों पर फॉस्फोराइलेट होते हैं।[3] कोशिकीय विकास और प्रजनन टाइरोसिन काइनेज पर निर्भर हो सकते हैं। टाइरोसिन काइनेज कार्य केन्द्रक आव्यूह में देखा गया है, जिसमें क्रोमेटिन नहीं अपितु केन्द्रक आवरक और "फ़िब्रोस वेब" सम्मिलित है जो डीएनए को भौतिक रूप से स्थिर करने का कार्य करता है।[3] विशिष्ट रूप से, Lyn, Src (जीन) सदस्य में अन्य प्रकार का काइनेज जिसे केन्द्रक आव्यूह में पहचाना गया था, कोशिका चक्र को नियंत्रित करता हुआ प्रतीत होता है। एसआरसी सदस्य टाइरोसिन काइनेसेस निकटता से संबंधित हैं किन्तु विभिन्न प्रकार की कार्यक्षमता प्रदर्शित करते हैं। एसआरसी फैमिली टाइरोसिन काइनेसेस की भूमिकाएँ अथवा अभिव्यक्तियाँ कोशिका प्रकार के साथ कोशिका वृद्धि और विशिष्टीकरण के समय अधिक भिन्न होती हैं।[3] सामान्य रूप से लिन और एसआरसी फैमिली टाइरोसिन काइनेसेस को सिग्नल ट्रांसडक्शन पाथवे में कार्य करने के लिए जाना जाता है।[3] इस तथ्य के प्रमाण हैं कि लिन कोशिका झिल्ली पर स्थानीयकृत है; लिन विभिन्न प्रकार के रिसेप्टर अणुओं के साथ शारीरिक और कार्यात्मक दोनों प्रकार से संयोजित है।[3]
तंतुकोशिका- कोशिका का प्रकार जो बाह्य आव्यूह और कोलेजन को संश्लेषित करता है और घाव भरने में सम्मिलित होता है - जिसे पॉलीओमावायरस द्वारा रूपांतरित किया गया है, जिसके कोशिकीय आव्यूह में उच्च टाइरोसिन गतिविधि होती है। इसके अतिरिक्त, टाइरोसिन काइनेज गतिविधि को कोशिकीय परिवर्तन से संबंधित होने के लिए निर्धारित किया गया है।[3] यह भी प्रदर्शित किया गया है कि टाइरोसिन पर मध्य-टी एंटीजन का फॉस्फोरिलन भी कोशिका परिवर्तन से संयोजित है, वह परिवर्तन जो कोशिकीय विकास अथवा प्रजनन के समान है।[3]
जीवित जीव के सामान्य अस्तित्व में यांत्रिक बल और नियामक संकेतों का संचरण अधिक वास्तविक है। प्रोटीन टाइरोसिन काइनेज भी इस कार्य में भूमिका निभाता है। पीटीके2 नामक प्रोटीन टाइरोसिन काइनेज, जिसे फोकल आसंजन काइनेज (एफएके) भी कहा जाता है, कोशिकीय फोकल आसंजनों के प्रभाव में होने की संभावना होती है, जिस प्रकार एफएके के इम्यूनोफ्लोरेसेंट स्थानीयकरण से संकेत प्राप्त होता है। फोकल आसंजन मैक्रोमोलेक्युलर संरचनाएं होती हैं जो यांत्रिक बल और नियामक संकेतों के संचरण में कार्य करती हैं।[5]
कोशिकीय प्रसार, जैसा कि ऊपर कुछ विस्तार से बताया गया है, टाइरोसिन काइनेज पर निर्भर हो सकता है।[3] केन्द्रक आव्यूह में टाइरोसिन काइनेज कार्य देखा गया है। लिन, काइनेज का वह प्रकार जिसका केन्द्रक आव्यूह में सर्वप्रथम अन्वेषण किया गया था, टाइरोसिन काइनेसेस के एसआरसी फैमिली का अंश है, जो कि विभेदित, कैल्शियम-उत्तेजित केर्टिनोसाइट्स के केंद्रक में समाहित हो सकता है। लिन, केन्द्रक आव्यूह में, केन्द्रक आवरक और "फ़िब्रोस वेब" के मध्य जो डीएनए को भौतिक रूप से स्थिर करता है, आव्यूह के सहयोग से कार्य करता पाया गया। इसके अतिरिक्त, यह कोशिका चक्र पर निर्भर प्रतीत होता है।[3] यद्यपि, केन्द्रक आव्यूह के भीतर कुल टाइरोसिन काइनेज गतिविधि में लिन प्रोटीन का योगदान अज्ञात है; क्योंकि लिन को केवल आंशिक रूप से प्राप्त किया गया था, इसकी गतिविधि का त्रुटिहीन माप प्रबंधित नहीं किया जा सका।[3] संकेत, जैसे कि वेजेस्ना एट अल. (1996) के अनुसार, लिन पॉलीपेप्टाइड्स केन्द्रक आव्यूह में टाइरोसिन काइनेज गतिविधि से संयोजित हैं। प्राप्त किया गया लिन एंजाइमेटिक रूप से सक्रिय था, जो इस धारणा के लिए समर्थन प्रदान करता था।
तथापि प्रोटीन टाइरोसिन काइनेज की संभावित भूमिका चूहों में एंडोटॉक्सिन के कारण संचार विफलता और अंग की शिथिलता की स्थिति में है, जहां अवरोधक टाइरफोस्टिन और जेनिस्टिन के प्रभाव प्रोटीन टायरोसिन काइनेज के साथ सम्मिलित होते हैं।[4] कोशिकाओं की झिल्लियों में उपस्थित रिसेप्टर्स द्वारा प्राप्त परिवेश में सिग्नल कोशिका साइटोप्लाज्म में संचारित होते हैं। बाए एट अल (2009), के अनुसार रिसेप्टर टाइरोसिन काइनेसेस के कारण ट्रांसमेम्ब्रेन सिग्नलिंग, परस्पर क्रियाओं पर अत्यधिक निर्भर करता है, उदाहरण के लिए, एसएच2 प्रोटीन डोमेन द्वारा मध्यस्थता, प्रयोग के माध्यम से यह निर्धारित किया गया है कि एसएच2 प्रोटीन डोमेन चयनात्मकता टाइरोसिन काइनेज से संयोजित कोशिकीय प्रक्रियाओं की मध्यस्थता में कार्यात्मक है। रिसेप्टर टाइरोसिन काइनेसेस इस विधि से, वृद्धि कारक रिसेप्टर सिग्नलिंग को प्रभावित कर सकता है। यह अधिक वास्तविक कोशिकीय संचार कार्यों मेटाज़ोन्स में से है।[6]
विनियमन
जब टायरोसिन काइनेज एंजाइम अन्य कारकों से प्रभावित होता है तो कभी-कभी बड़े परिवर्तन उत्पन्न होते हैं। कारकों में अणु होता है जो प्रोटीन द्वारा विपरीत रूप से बाधित होता है, जिसे लिगैंड कहा जाता है। कई रिसेप्टर टाइरोसिन काइनेसेस, यद्यपि निश्चित रूप से सभी नहीं, प्रोटीन-काइनेज गतिविधि तब तक नहीं करते जब तक कि इनमें से किसी लिगेंड द्वारा आधिपत्य नहीं किया जाता है अथवा सक्रिय नहीं किया जाता है।[2] यद्यपि अधिक शोध से संकेत प्राप्त होता है कि रिसेप्टर्स एंडोसोम के भीतर सक्रिय रहते हैं, कभी यह विचार भी किया गया था कि लिगेंड के कारण होने वाली एंडोसाइटोसिस उस प्रक्रिया के लिए उत्तरदायी घटना थी जिसमें रिसेप्टर्स निष्क्रिय होते हैं। सक्रिय रिसेप्टर टाइरोसिन काइनेज रिसेप्टर्स को कम समय में आंतरिक किया जाता है (तंत्र में पुनः पुनर्नवीनीकरण किया जाता है) और अंततः लाइसोसोम में पहुंचाया जाता है, जहां वे पाचन में भाग लेने वाले कैटोबोलिक अम्ल हाइड्रॉलिसिस के निकट कार्य करते हैं। भिन्न-भिन्न रिसेप्टर टाइरोसिन काइनेज तंत्र में भिन्न-भिन्न भूमिकाओं में आंतरिक सिग्नलिंग कॉम्प्लेक्स सम्मिलित होते हैं, जिनकी विशिष्टताओं पर शोध किया गया था।[7] इसके अतिरिक्त, लिगेंड प्रतिवर्ती आबद्धकर में भाग लेते हैं, अवरोधक गैर-सहसंयोजक रूप से बाधित करते हैं (विभिन्न प्रकार के अवरोध इस पर निर्भर करते हैं कि क्या ये अवरोधक एंजाइम तथा एंजाइम-सब्सट्रेट परिसर, दोनों को बाधित करते हैं अथवा बाधित नहीं करते हैं)। बहुसंयोजकता विशेषता है जो संबंधित वैज्ञानिक अनुसंधान में सम्मिलित कुछ व्यक्तियों के लिए विशेष रुचि रखती है, यह ऐसी घटना है जो इकाई पर स्थित कई लिगेंडों के समवर्ती बंधन से दूसरे पर कई संयोगी रिसेप्टर्स के लिए होती है।[8] किसी भी स्थिति में, लिगैंड का अपने साथी से आबद्धकर कई प्रोटीनों की कार्यक्षमता पर होने वाले प्रभावों के कारण स्पष्ट होता है।[2] लिगैंड-सक्रिय रिसेप्टर टाइरोसिन काइनेसेस, जैसा कि उन्हें कभी-कभी संदर्भित किया जाता है, अद्भुत विशेषता प्रदर्शित करता है। टाइरोसिन रिसेप्टर काइनेज जब अपने लिगैंड से संयोजित हो जाता है, तो यह कोशिका के साइटोसोल में रहने वाले टायरोसिन काइनेज से संयोजित होने में सक्षम हो जाता है।[2]
क्रिया में इस ट्रिगर-प्रणाली का उदाहरण वह प्रक्रिया है जिसके द्वारा एरिथ्रोसाइट्स के गठन को विनियमित किया जाता है। स्तनधारियों में यह प्रणाली होती है, जो गुर्दे में प्रारम्भ होती है जहां विकासात्मक संकेत निर्मित होता है।[2] विकासात्मक संकेत, जिसे साइटोकिन भी कहा जाता है, इस स्थिति में एरिथ्रोपोइटिन है। (साइटोकिन्स हेमेटोपोएटिक कोशिका प्रसार और विभेदन के प्रमुख नियामक हैं।) हेमेटोपोएटिक साइटोकाइन रिसेप्टर्स सक्रिय होने पर एरिथ्रोपोइटिन की गतिविधि प्रारम्भ होती है।[9] एरिथ्रोसाइट विनियमन में, एरिथ्रोपोइटिन प्रोटीन होता है जिसमें 165 अमीनो अम्ल होते हैं जो साइटोप्लाज्मिक प्रोटीन काइनेज जेएके को सक्रिय करने में भूमिका निभाते हैं।[2] कुछ नए शोधों के परिणामों ने यह भी संकेत दिया है कि उपरोक्त साइटोकिन रिसेप्टर्स जानूस काइनेज सदस्यों के साथ कार्य करते हैं। साइटोकिन रिसेप्टर्स जेएके काइनेसेस को सक्रिय करते हैं। इसके पश्चात कोशिका झिल्ली में स्थित कई सिग्नलिंग प्रोटीन के फॉस्फोरिलन का परिणाम होता है। यह पश्चात में लिगैंड-मध्यस्थ रिसेप्टर्स और अंतःकोशिकी सिग्नलिंग मार्ग सक्रियण दोनों की उत्तेजना को प्रभावित करता है।[9] जेएके काइनेसेस के लिए सबस्ट्रेट्स कुछ जीन प्रतिक्रियाओं और अन्य में मध्यस्थता करते हैं।[9] प्रक्रिया रक्त कोशिकाओं के उत्पादन में मध्यस्थता के लिए भी उत्तरदायी होती है।[2] इस स्थिति में, एरिथ्रोपोइटिन संबंधित प्लाज्मा झिल्ली रिसेप्टर से संयोजित हो जाता है, जिससे रिसेप्टर मंद हो जाता है।[2] डिमर बाइंडिंग के माध्यम से काइनेज जेएके को सक्रिय करने के लिए उत्तरदायी है।[2] एरिथ्रोपोइटिन रिसेप्टर के साइटोप्लाज्मिक डोमेन में स्थित टायरोसिन अवशेषों को सक्रिय प्रोटीन काइनेज जेएके द्वारा परिणामस्वरूप फास्फोराइलेट किया जाता है।[2] वस्तुतः, यह भी है कि एरिथ्रोसाइट गठन को विनियमित करने के लिए लिगैंड द्वारा रिसेप्टर टाइरोसिन काइनेज को किस प्रकार सक्रिय किया जा सकता है।
अन्य उदाहरण
इसके समान कारक-प्रभावित प्रोटीन टाइरोसिन काइनेज गतिविधि के अतिरिक्त उदाहरण उपस्थित हैं। एडेप्टर प्रोटीन जैसे कि Grb2 रिसेप्टर प्रोटीन काइनेसेस के प्रभाव में फॉस्फेट-टायरोसिन अवशेषों को बाधित कर देगा। यह तंत्र सामान्य है जो प्रोटीन-प्रोटीन अंतःक्रिया को उत्तेजित करता है।।[2]
इसके अतिरिक्त, परिस्थिति का वर्णन करने के लिए, इंसुलिन से जुड़े कारकों को टाइरोसिन काइनेज को प्रभावित करने के लिए निर्धारित किया गया है। इंसुलिन रिसेप्टर सब्सट्रेट अणु होते हैं जो इंसुलिन के प्रभाव को विनियमित करके सिग्नलिंग में कार्य करते हैं।[2] कई रिसेप्टर एंजाइमों में निकटता से संबंधित संरचना और रिसेप्टर टाइरोसिन काइनेज गतिविधि होती है, और यह निर्धारित किया गया है कि मूलभूत अथवा प्रोटोटाइपिक रिसेप्टर एंजाइम इंसुलिन है।[2] इंसुलिन रिसेप्टर सबस्ट्रेट्स आईआरएस2 और आईआरएस3 प्रत्येक में विशिष्ट ऊतक कार्य और वितरण होता है जो रिसेप्टर टाइरोसिन काइनेसेस द्वारा प्रारम्भ किए गए मार्गों में सिग्नलिंग क्षमताओं को विस्तारित करने के लिए कार्य करता है।[2] सक्रिय आईआरएस-1 अणु इंसुलिन द्वारा निर्मित सिग्नल को विस्तारित करते हैं।[2] इसके विपरीत, इंसुलिन रिसेप्टर प्रणाली, एंडोसोमल सिग्नलिंग की प्रभावकारिता को कम करती प्रतीत होती है।[7]
एपिडर्मल वृद्धि कारक रिसेप्टर प्रणाली का उपयोग मध्यवर्ती उदाहरण के रूप में किया गया है।[7] इस स्थिति में कुछ संकेत वास्तविक कोशिका की सतह से उत्पन्न होते हैं किन्तु अन्य संकेत इंडोसोम के भीतर से प्राप्त होते प्रतीत होते हैं। लिगैंड-विशिष्ट संकेतों को बनाने के लिए इस प्रकार का कार्य साधन हो सकता है।[7] यह इस धारणा का समर्थन करता है कि ट्रैफिकिंग, एमआरएनए अनुवादन के पश्चात प्रोटीन के संशोधन के लिए शब्द है, जो रिसेप्टर सिग्नलिंग के कार्य के लिए महत्वपूर्ण हो सकता है।
- Phosphate Group.PNG
फास्फेट
संरचना
प्रोटीन टाइरोसिन काइनेज, प्रोटीन में, प्रोटीन काइनेज डोमेन होता है, जिसमें एन टर्मिनल लोब होता है जिसमें 5 बीटा शीट स्ट्रैंड और अल्फा हेलिक्स होता है जिसे सी-हेलिक्स कहा जाता है, और सी टर्मिनल डोमेन में सामान्यतः 6 अल्फा हेलिकॉप्टर (हेलिसेस D, E, F, G, H, और I) होते हैं। काइनेज डोमेन नियंत्रण कटैलिसीस के केंद्र में दो लूप होते हैं। कैटेलिटिक लूप में एचआरडी मोटिफ (सामान्यतः अनुक्रम हिज-आर्ग-एस्प के साथ) होता है। इस मूल भाव का एसपारटिक अम्ल उत्प्रेरण के समय Tyr पर सब्सट्रेट OH समूह के साथ हाइड्रोजन बंध बनाता है। अन्य पाश सक्रियण पाश है, जिसकी स्थिति और रचना आंशिक रूप से निर्धारित करती है कि काइनेज सक्रिय है अथवा निष्क्रिय है। सक्रियण पाश DFG मूल भाव से (सामान्यतः अनुक्रम Asp-Phe-Gly के साथ) प्रारम्भ होता है।[10]
प्रोटीन डेटा बैंक में टाइरोसिन काइनेज की 1500 से अधिक 3डी संरचनाएं उपलब्ध हैं। जिसके उदाहरण में PDB: 1IRK, मानव इंसुलिन रिसेप्टर के टाइरोसिन काइनेज डोमेन की क्रिस्टल संरचना सम्मिलित है।
फैमिली
टाइरोसिन काइनेसेस को दो मुख्य फैमिलीज़ में विभाजित किया गया है:
- ट्रांसमेम्ब्रेन रिसेप्टर-लिंक्ड काइनेसेस
- वे जो साइटोप्लाज्मिक प्रोटीन हैं
मानव जीनोम में 90 से अधिक प्रोटीन टाइरोसिन काइनेसेस (पीटीके) पाए गए हैं। वे दो वर्गों, रिसेप्टर और गैर-रिसेप्टर टाइरोसिन काइनेसेस में विभाजित हैं।
रिसेप्टर
2004 तक, 58 रिसेप्टर टाइरोसिन काइनेसेस (आरटीके) ज्ञात थे, जिन्हें 20 सब-फैमिलीज़ में विभाजित किया गया था। वे विभिन्न कोशिकीय गतिविधियों में महत्वपूर्ण भूमिका निभाते हैं जिनमें विकास (न्यूरोट्रॉफ़िन संकेत द्वारा), कोशिकीय विभेदीकरण, चयापचय, आसंजन, गतिशीलता और मृत्यु सम्मिलित हैं।[11]
आरटीके बाह्य डोमेन से बना है, जो विशिष्ट लिगैंड, ट्रांसमेम्ब्रेन डोमेन और अंतःकोशिकी कैटेलिटिक डोमेन को बाधित करने में सक्षम है, जो चयनित सबस्ट्रेट्स को बाधित करने और फॉस्फोराइलेट करने में सक्षम है। लिगैंड को बाह्य क्षेत्र में बाधित करने से आरटीके में संरचनात्मक पुनर्व्यवस्था की श्रृंखला होती है जो इसके एंजाइमेटिक सक्रियण की ओर ले जाती है। विशेष रूप से, काइनेज डोमेन के कुछ भागों का संचलन, एडेनोसिन ट्राइफॉस्फेट (एटीपी) और सबस्ट्रेट (जैव रसायन) को सक्रिय साइट तक मुफ्त पहुंच प्रदान करता है। यह अंतःकोशिकी प्रोटीन के फॉस्फोराइलेशन के माध्यम से घटनाओं का जलप्रपात ट्रिगर करता है जो अंततः केंद्रक को बाह्य संचारित ("ट्रांसड्यूस") करता है, जिससे जीन अभिव्यक्ति में परिवर्तन होता है।
कई आरटीके ऑन्कोजेनेसिस में या तो जीन उत्परिवर्तन अथवा गुणसूत्र अनुवाद द्वारा,[12] या केवल अति-अभिव्यक्ति द्वारा सम्मिलित हैं। प्रत्येक स्थिति में, परिणाम अति-सक्रिय काइनेज होता है, जो कैंसर कोशिकाओं को असामान्य, लिगेंड-स्वतंत्र, गैर-विनियमित विकास प्रोत्साहन प्रदान करता है।
साइटोप्लाज्मिक/गैर-रिसेप्टर
मनुष्यों में, 32 साइटोप्लाज्मिक प्रोटीन टाइरोसिन काइनेसेस होते हैं (EC 2.7.10.2).
प्रमाणित किया गया प्रथम गैर-रिसेप्टर टायरोसिन किनेज v-src ऑन्कोजेनिक प्रोटीन था। अधिकांश पशु कोशिकाओं में टाइरोसिन काइनेसेस के एसआरसी फैमिली के अधिक सदस्य होते हैं। चिकन सार्कोमा वायरस, ऊपर उल्लिखित रूस सार्कोमा वायरस, सामान्य कोशिकीय एसआरसी जीन के उत्परिवर्तित संस्करणों को ले जाने के लिए पाया गया था।[13] उत्परिवर्तित v-src जीन ने एंजाइम गतिविधि के सामान्य अंतर्निहित निषेध को लुप्त कर दिया है जो कोशिकीय एसआरसी (c-src) जीन की विशेषता है। एसआरसी के सदस्यों को कई कोशिकीय प्रक्रियाओं को विनियमित करने के लिए पाया गया है। उदाहरण के लिए, टी-कोशिका एंटीजन रिसेप्टर Lck और Fyn दो प्रोटीनों के सक्रियण द्वारा अंतःकोशिकी सिग्नलिंग की ओर ले जाता है जो संरचनात्मक रूप से एसआरसी के समान होते हैं।
नैदानिक महत्व
कैंसर के उपचार में उनके प्रभाव के कारण टाइरोसिन काइनेसेस वर्तमान में विशेष रूप से महत्वपूर्ण हैं। उत्परिवर्तन जो कुछ टाइरोसिन काइनेसेस को संवैधानिक रूप से सक्रिय बनाता है, कई कैंसर से संयोजित है। इमैटिनिब (ब्रांड नाम ग्लीवेक और ग्लिवेक) औषधि है जो इन टाइरोसिन काइनेसेस के उत्प्रेरक फांक को बाधित करने में सक्षम है, जिससे इसकी गतिविधि बाधित होती है।[14]
टाइरोसिन काइनेज गतिविधि अन्य घटनाओं में भी महत्वपूर्ण रूप से सम्मिलित होती है जिन्हें कभी-कभी अत्यधिक प्रतिकूल माना जाता है। उदाहरण के लिए, एंजाइम की विस्तृत गतिविधि को कोशिका विभाजन जैसी कुछ प्रणालियों के कार्य को अव्यवस्थित करने में सम्मिलित किया गया है। स्थानीय सूजन से संबंधित कई बीमारियां जैसे एथेरोस्क्लेरोसिस और सोरायसिस, या प्रणालीगत सूजन जैसे सेप्सिस और सेप्टिक शॉक भी सम्मिलित हैं।[4] कई वायरस संक्रमण के समय टाइरोसिन काइनेज कार्य को लक्षित करते हैं। पोलियोमा वायरस केन्द्रक आव्यूह के भीतर टाइरोसिन काइनेज गतिविधि को प्रभावित करता है।[3] फाइब्रोब्लास्ट स्तनधारी कोशिकाओं में घाव भरने और कोशिका संरचना निर्माण में सम्मिलित कोशिकाएं हैं। जब इन कोशिकाओं को पोलियोमा वायरस द्वारा रूपांतरित किया जाता है, तो कोशिकीय आव्यूह में उच्च टाइरोसिन गतिविधि देखी जाती है, जो कोशिकीय प्रसार से भी संबंधित होती है।[3] अन्य वायरस जो टाइरोसिन काइनेज को लक्षित करता है, वह है रूस सार्कोमा वायरस, रेट्रोवायरस जो मुर्गियों में सार्कोमा का कारण बनता है। संक्रमित कोशिकाएं स्पष्ट संरचना संशोधनों और कोशिका विकास विनियमन को प्रदर्शित करती हैं जो अधिक असामान्य है।[5] रूस सार्कोमा वायरस द्वारा एन्कोड किए गए प्रोटीन टाइरोसिन काइनेसेस कोशिकीय परिवर्तन का कारण बनते हैं, और इन्हें ओंकोप्रोटीन कहा जाता है।[5] इसके अतिरिक्त, टायरोसिन काइनेज कभी-कभी अनुचित रूप से कार्य कर सकता है जिससे गैर-लघु कोशिका फेफड़ों का कैंसर हो सकता है।[15] सामान्य, व्यापक कैंसर, नॉन-स्मॉल सेल लंग कैंसर, स्तन, कोलोरेक्टल, और प्रोस्टेट कैंसर की कुल संख्या की तुलना में अधिक व्यक्तियों की मृत्यु का कारण है।[15]
शोध से ज्ञात होता है कि सामान्य कोशिकाओं में ट्रांसमेम्ब्रेन रिसेप्टर- और झिल्ली से जुड़े प्रोटीन टाइरोसिन काइनेसेस दोनों द्वारा टाइरोसिन के अवशेषों पर प्रोटीन फॉस्फोरिलन होता है। फॉस्फोराइलेशन कोशिकीय सिग्नलिंग में महत्वपूर्ण भूमिका निभाता है जो विकास कारकों की संख्या और विविधता को नियंत्रित करता है। यह इस अवलोकन से स्पष्ट है कि रूस सार्कोमा वायरस से प्रभावित कोशिकाएं स्पष्ट संरचनात्मक संशोधनों और सामान्य कोशिका वृद्धि विनियमन की कुल कमी प्रदर्शित करती हैं।[5] रूस सार्कोमा वायरस-एन्कोडेड ओंकोप्रोटीन, प्रोटीन टाइरोसिन काइनेसेस हैं जो इस कोशिकीय परिवर्तन का कारण हैं, और इसके लिए आवश्यक भी हैं। कोशिका संरचना और विकास विनियमन में परिवर्तन के साथ टाइरोसिन फॉस्फोरिलन गतिविधि में भी वृद्धि हो जाती है अथवा कमी हो जाती है। इस प्रकार, कोशिकाओं द्वारा प्रदर्शित निश्चित परिवर्तन उस भूमिका पर निर्भर है जो टाइरोसिन काइनेज प्रदर्शित करता है।[5] लिम्फोसाइटों के सक्रियण में प्रोटीन टाइरोसिन काइनेसेस की प्रमुख भूमिका होती है। इसके अतिरिक्त, वे अधिवृक्क क्रोमाफिन, प्लेटलेट्स और तंत्रिका कोशिकाओं जैसे कोशिका प्रकारों में संचार मार्गों की मध्यस्थता में कार्यात्मक हैं।
विचार किए गए प्रभावों, जैसे उत्परिवर्तन और अधिक के कारण टाइरोसिन काइनेज जीव के भीतर अनियमित एंजाइम बन सकता है। यह व्यवहार विनाश का कारण बनता है; जिससे आवश्यक प्रक्रियाएं अव्यवस्थित हो जाती हैं। वह तंत्र जिस पर जीव निर्भर करता है विकृत हो जाता है, जिसके परिणामस्वरूप अधिकांशतः कैंसर होता है। इस प्रकार की परिस्थिति को अवरोधित करना अत्यधिक वांछनीय है। अधिकांश शोधों ने पूर्व ही महत्वपूर्ण प्रभाव को नोट किया है कि वास्तविक रूप से कार्य करने वाले प्रोटीन टाइरोसिन काइनेज एंजाइम के अवरोधकों का संबंधित रोगों पर प्रभाव होता है। (टायरोसिन-काइनेज अवरोधक देखें)
नॉन-स्मॉल सेल लंग कैंसर
नैदानिकजिफिटिनिब परीक्षण में टाइरोसिन काइनेज के अवरोधक के लिए कैंसर की प्रतिक्रिया का मूल्यांकन किया गया था।[15] इस स्थिति में, जिफिटिनिब टाइरोसिन काइनेज का अवरोधक है। अनुचित टाइरोसिन काइनेज कार्य गैर-लघु कोशिका फेफड़ों के कैंसर का कारण बन सकता है।[16] जिफिटिनिब टाइरोसिन काइनेज अवरोधक है जो एपिडर्मल वृद्धि कारक रिसेप्टर को लक्षित करता है तथा गैर-लघु कोशिका फेफड़ों के कैंसर वाले रोगियों में अनुकूल परिणाम उत्पन्न करता है। स्तन, कोलोरेक्टल और प्रोस्टेट कैंसर की तुलना में सामान्य, व्यापक कैंसर, गैर-लघु कोशिका फेफड़ों का कैंसर अधिक व्यक्तियों में मृत्यु का कारण है।[15] यह कैंसर के उपचार में संभावित लक्ष्यों के रूप में टाइरोसिन काइनेज अवरोधकों पर शोध करने के लिए स्थिर प्रेरणा है। जिफिटिनिब, एपिडर्मल वृद्धि कारक रिसेप्टर टाइरोसिन काइनेज इनहिबिटर के रूप में कार्य करता है, नॉन-स्मॉल सेल लंग कैंसर से संबंधित लक्षणों में सुधार करता है और इसके परिणामस्वरूप रेडियोग्राफिक ट्यूमर रिग्रेशन होता है।[15] यह ऐसे अवरोधक की प्रभावकारिता का उदाहरण है। निषेध की प्रक्रिया से ज्ञात होता है कि कैंसर कैसे बना है। एपिडर्मल वृद्धि कारक रिसेप्टर में उत्परिवर्तन कोशिका अस्तित्व को प्रोत्साहित करने वाले सिग्नलिंग मार्ग को सक्रिय करते हैं। नॉन-स्माल सेल लंग कैंसर कोशिकाएं इन जीवित रहने के संकेतों पर निर्भर हो जाती हैं। गैर-लघु कोशिका कैंसर के उपचार के लिए औषधि के रूप में जिफिटिनिब का उत्तरजीविता संकेतों का निषेध इसकी प्रभावकारिता के लिए योगदान कारक हो सकता है।[16]
जिफिटिनिब मनुष्यों द्वारा उचित रूप से स्वीकार किया जाता है, और उपचार के परिणामस्वरूप 43% की लक्षण सुधार दर (33% -53% अंतराल में 95% आत्मविश्वास के साथ) रोगियों के लिए होती है, जिन्हें 250 मिलीग्राम जिफिटिनिब दिया गया था और 35% ( 26%-45% अंतराल में 95% आत्मविश्वास के साथ) प्राप्त होता है, उन व्यक्तियों के लिए जिन्हें 500 मिलीग्राम दिया गया था।[15] परीक्षण में, एपिडर्मल वृद्धि कारक रिसेप्टर ने अवरोधक के लिए तीव्रता से प्रतिक्रिया दिखाई, जैसा कि कैंसर के लक्षणों में सुधार के द्वारा दिखाया गया है। प्रत्येक समूह में, एपिडर्मल वृद्धि कारक रिसेप्टर टाइरोसिन काइनेज इनहिबिटर उपचार के 1 सप्ताह के पश्चात सुधार देखा गया।[15] प्रति दिन 1 बार जिफिटिनिब लगाने से गैर-लघु कोशिका फेफड़ों के कैंसर रोगियों में "तीव्रता से" लक्षण सुधार और ट्यूमर के प्रतिगमन का कारण बनता है।[15] चिकित्सा अनुसंधान के क्षेत्र में, यह टाइरोसिन काइनेज से संयोजित कैंसर के उपचार के लिए अवरोधक के उपयोग का विशेष रूप से महत्वपूर्ण उदाहरण है। इस परीक्षण में किये गए शोधों से पूर्व केवल कीमोथेरेपी, सर्जरी और रेडियोथेरेपी ही प्रमुख विकल्प उपलब्ध थे। प्रति दिन जिफिटिनिब मौखिक उपचार के दुष्प्रभाव महत्वपूर्ण माने गए। 250 मिलीग्राम समूह में 57% और 500 मिलीग्राम समूह के 75% रोगियों में दस्त की सूचना प्राप्त हुई थी।[15] रोगी को ग्रेड 2 की तुलना में अधिक गंभीर दस्त था, जिसमें केवल दिन में छह बार मल त्याग होता था।[15] इसके अतिरिक्त, मृत्यु संभवतः एपिडर्मल वृद्धि कारक रिसेप्टर टाइरोसिन काइनेज इनहिबिटर उपचार के कारण हुई; यद्यपि, सहसंबंध स्पष्ट नहीं है।[15] इसके अतिरिक्त, 250 मिलीग्राम समूह में 62% रोगियों में त्वचा की विषाक्तता देखी गई। तत्पश्चात जिफिटिनिब के दुष्प्रभाव केवल "सामान्यतः सामान्य, प्रबंधनीय, असंचयी और प्रतिवर्ती" थे।[15] दुर्भाग्य से, अवरोधक लेना विवृत करना प्रतिकूल लक्षणों की मात्र परिवर्तित रणनीति हो सकती है।[15] जिफिटिनिब अभी भी अन्य कैंसर उपचारों की तुलना में सुरक्षित और प्रभावी उपचार का प्रतिनिधित्व करता है।
इसके अतिरिक्त, एपिडर्मल वृद्धि कारक रिसेप्टर ट्यूमरजेनिसिस में महत्वपूर्ण भूमिका निभाता है, जो नए ट्यूमर का उत्पादन है।[17] 2010 तक कैंसर के उपचार के लिए दो मोनोक्लोनल एंटीबॉडी और एर्लोटिनिब नामक अन्य छोटे-अणु टाइरोसिन काइनेज अवरोधक को भी विकसित किया गया था।[17]
12 जुलाई, 2013 एफडीए ने मेटास्टैटिक नॉन-स्माल सेल लंग कैंसर (एनएससीएलसी) वाले रोगियों के प्रथम-पंक्ति उपचार के लिए एफैटिनिब मल्टीपल रिसेप्टर, अपरिवर्तनीय टीकेआई को स्वीकृति दी, जिनके ट्यूमर में एपिडर्मल वृद्धि कारक रिसेप्टर (ईजीएफआर) उत्परिवर्तन होता है।
क्रोनिक माइलॉयड ल्यूकेमिया
बीसीआर-एबीएल संवैधानिक रूप से सक्रिय टाइरोसिन काइनेज है जो क्रोनिक माइलॉयड ल्यूकेमिया से संयोजित है। यह संलयन जीन से बनता है जब गुणसूत्र 9 और 22 के खंड विभक्त हो जाते हैं और एक-दूसरे से जुड़ जाते हैं। गुणसूत्र 9 से एबीएल जीन बीसीआर-एबीएल संलयन जीन बनाने के लिए गुणसूत्र 22 पर बीसीआर जीन से जुड़ता है।[18] बीसीआर-एबीएल के परिवर्तन के लिए टाइरोसिन काइनेज गतिविधि महत्वपूर्ण होती है। इसलिए इसे अवरोधित करने से कैंसर के लक्षणों में सुधार होता है। सीएमएल के उपचार के लिए वर्तमान में उपलब्ध बीसीआर-एबीएल टाइरोसिन काइनेज अवरोधकों में इमैटिनिब, डेसैटिनिब, निलोटिनिब, बोसुटिनिब और पोनाटिनिब सम्मिलित हैं।
गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर
गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर (जीआईएसटी) कैंसर के कीमोथेरेपी उपचार के लिए जाने जाते हैं और उन्नत स्थितियों में किसी भी प्रकार की चिकित्सा (2001 में) का उत्तर नहीं देते हैं। यद्यपि, मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रॉमल ट्यूमर वाले रोगी के उपचार में टायरोसिन काइनेज अवरोधक एसटीआई 571 (इमैटिनिब) प्रभावी है।[19] गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर में मेसेंकाईमल नियोप्लाज्म्स का समूह होता है जो गैस्ट्रोइंटेस्टाइनल ट्रैक्ट में संयोजी-ऊतक बनाने वाली कोशिकाओं के अग्रदूतों से बनता है।[19] इनमें से अधिकतर ट्यूमर उदर में पाए जाते हैं, यद्यपि वे छोटी आंत में या आंतों के मार्ग में कहीं और भी स्थित हो सकते हैं। इन ट्यूमर की कोशिकाओं में वृद्धि कारक रिसेप्टर होता है जो टाइरोसिन काइनेज गतिविधि से जुड़ा होता है।[19] इस वृद्धि कारक रिसेप्टर को सी किट कहा जाता है और यह प्रोटो-ओन्कोजीन (सी-किट) द्वारा निर्मित होता है। सी-किट का उत्परिवर्तन टाइरोसिन काइनेज की संवैधानिक गतिविधि का कारण बनता है, जिसके परिणामस्वरूप कैंसर गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर होता है। सी-किट म्यूटेशन के परिणामों में अप्रतिबंधित टाइरोसिन काइनेज गतिविधि और कोशिका प्रसार, सी-किट का अनियमित फॉस्फोराइलेशन और कुछ संचार मार्गों का विघटन सम्मिलित है।[19] इमैटिनिब के साथ उपचार गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर में असामान्य कोशिका सिग्नलिंग तंत्र को बाधित कर सकता है। इसके परिणामस्वरूप रोगियों में महत्वपूर्ण प्रतिक्रिया होती है और निरंतर रोग नियंत्रण होता है। 2001 तक यह संदेह नहीं रह गया था कि यह अवरोधक मनुष्यों में प्रभावी और सुरक्षित हो सकता है।[7] इसी प्रकार, प्रोटीन टायरोसिन काइनेज अवरोधक एसटीआई 571 ट्यूमर के भौतिक आकार को कम करने के लिए पाया गया; परीक्षण के 4 माह में उनका आकार लगभग 65% कम हो गया, और लगातार कम होता गया। नए घाव प्रकट नहीं हुए, और कई यकृत मेटास्टेस पूरी रूप से अस्तित्वहीन हो गए। अध्ययन में सम्मिलित रोगी उपचार के पश्चात स्वस्थ रहा।[19] उन्नत गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर के लिए उपचार का कोई प्रभावी साधन नहीं है, किन्तु एसटीआई 571 प्रारंभिक चरण के कैंसर में प्रभावी उपचार का प्रतिनिधित्व करता है, जो प्रतिकूल टाइरोसिन काइनेज गतिविधि को अवरोधित करके संवैधानिक रूप से सक्रिय सी-किट से संयोजित है।[19]
अवरोधक
एंजाइम गतिविधि को कम करने के लिए, अवरोधक अणु एंजाइमों को बाधित करते हैं। एंजाइम गतिविधि को कम करने से रोगज़नक़ अक्षम हो सकता है या अनुचित रूप से कार्य करने वाली प्रणाली को उचित कर सकता है; जैसे, सामान्य जनता द्वारा औषधिओं के रूप में उपयोग किए जाने के लिए कई एंजाइम अवरोधक विकसित किए गए हैं।
जिस्ट और इमैटिनिब
गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर (जीआईएसटी) मेसेनकाइमल ट्यूमर हैं जो गैस्ट्रोइंटेस्टाइनल ट्रैक्ट को प्रभावित करते हैं।[20] उपचार के विकल्प सीमित कर दिए गए हैं।[20] यद्यपि इमैटिनिब, अनुचित रूप से कार्य करने वाले एंजाइम के अवरोधक के रूप में प्रभावी हो सकता है।[20]
जीर्ण माईलोजेनस रक्त कैंसर और निलोटिनिब
यदि इमैटिनिब कार्य नहीं करता है, तो उन्नत क्रोनिक माइलोजेनस ल्यूकेमिया वाले रोगी़ नीलोटिनिब, डेसैटिनिब, बोसुटिनिब, पोनाटिनिब, या ल्यूकेमिया का कारण बनने वाले अनुचित एंजाइम के लिए अन्य अवरोधक का उपयोग कर सकते हैं।[21] यह अवरोधक अत्यधिक चयनात्मक Bcr-Abl टाइरोसिन काइनेज अवरोधक है।[21]
अन्य
सुनीटिनिब ओरल टाइरोसिन काइनेज इनहिबिटर है जो वैस्कुलर एंडोथेलियल वृद्धि कारक रिसेप्टर (वीईजीएफआर), प्लेटलेट-व्युत्पन्न वृद्धि कारक रिसेप्टर (PDGFR), स्टेम कोशिका फैक्टर रिसेप्टर और कॉलोनी-उत्तेजक कारक -1 रिसेप्टर (बर्स्टीन एट अल। 2008) पर कार्य करता है।
जिफिटिनिब और एर्लोटिनिब एपिडर्मल वृद्धि कारक रिसेप्टर (ईजीएफआर) के टायरोसिन काइनेज डोमेन को अवरोधित करते हैं, फेफड़े और अग्नाशय के कैंसर के उपचार के लिए इसका उपयोग किया जा सकता है, जहां अधिकांशतः इस कोशिका-सतह रिसेप्टर टाइरोसिन काइनेज की अति-अभिव्यक्ति होती है।
काइनेज अवरोधकों की भी मध्यस्थता की जा सकती है। पेराक्रिन सिग्नलिंग एपिडर्मल वृद्धि कारक रिसेप्टर काइनेज इनहिबिटर की प्रतिक्रिया की मध्यस्थता करता है। पैराक्राइन ऐसा करने के लिए ट्यूमर अन्तःस्तरीय कोशिका में एपिडर्मल वृद्धि कारक रिसेप्टर को सक्रिय करता है।[22]
डेसैटिनिब एसआरसी अवरोधक टाइरोसिन काइनेज अवरोधक है जो सेनोलिटिक और क्रोनिक माइलोजेनस ल्यूकेमिया के लिए चिकित्सा के रूप में प्रभावी है।
उदाहरण
इस डोमेन वाले मानव प्रोटीन में सम्मिलित हैं:
AATK; ABL; ABL2; ALK; AXL; BLK; BMX; BTK; CSF1R; CSK; DDR1; DDR2; EGFR; EPHA1; EPHA2; EPHA3; EPHA4; EPHA5; EPHA6; EPHA7; EPHA8; EPHA10; EPHB1; EPHB2; EPHB3; EPHB4; EPHB6; ERBB2; ERBB3; ERBB4; FER (जीन); FES; FGFR3; FGR (जीन); FLT1; FLT3; FLT4; FRK; FYN; GSG2; HCK; IGF1R; ILK; INSR ; INSRR; IRAK4; ITK (जीन); JAK1; JAK2; JAK3; KDR; CD117; KSR1; LCK; LMTK2; LMTK3; LTK; LYN; MATK; MERTK; MET; MLTK; MST1R; MUSK; NPR1; NTRK1; NTRK2; NTRK3; PDGFRA; PDGFRB; PLK4; PTK2; PTK2B; PTK6; PTK7; RET; ROR1; ROR2; ROS1; RYK; SGK493; SRC; SRMS; STYK1; SYK; TEC; TEK; TEX14; TIE1; TNK1; TNK2; TNNI3K; TXK; TYK2; TYRO3; YES1; ZAP70
यह भी देखें
- टाइफॉस्टिन
- Bcr-Abl टाइरोसिन काइनेज अवरोधक
- BYKdb
संदर्भ
- ↑ Hanks SK, Quinn AM, Hunter T (July 1988). "The protein kinase family: conserved features and deduced phylogeny of the catalytic domains". Science. 241 (4861): 42–52. Bibcode:1988Sci...241...42H. doi:10.1126/science.3291115. PMID 3291115.
- ↑ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 2.13 2.14 2.15 2.16 {{cite book | vauthors = Cox M, Nelson DR | title = लेहिंगर: बायोकेमिस्ट्री के सिद्धांत| edition = fifth | publisher = W H Freeman & Co | year = 2008 | isbn = 978-1-4292-2416-1 }
- ↑ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 3.10 3.11 3.12 3.13 3.14 Radha V, Nambirajan S, Swarup G (March 1996). "Association of Lyn tyrosine kinase with the nuclear matrix and cell-cycle-dependent changes in matrix-associated tyrosine kinase activity". European Journal of Biochemistry. 236 (2): 352–359. doi:10.1111/j.1432-1033.1996.00352.x. PMID 8612602.
- ↑ 4.0 4.1 4.2 Ruetten H, Thiemermann C (September 1997). "Effects of tyrphostins and genistein on the circulatory failure and organ dysfunction caused by endotoxin in the rat: a possible role for protein tyrosine kinase". British Journal of Pharmacology. 122 (1): 59–70. doi:10.1038/sj.bjp.0701345. PMC 1564904. PMID 9298529.
- ↑ 5.0 5.1 5.2 5.3 5.4 Schaller MD, Borgman CA, Cobb BS, Vines RR, Reynolds AB, Parsons JT (June 1992). "pp125FAK एक संरचनात्मक रूप से विशिष्ट प्रोटीन-टायरोसिन किनेज है जो फोकल आसंजनों से जुड़ा है". Proceedings of the National Academy of Sciences of the United States of America. 89 (11): 5192–5196. Bibcode:1992PNAS...89.5192S. doi:10.1073/pnas.89.11.5192. PMC 49256. PMID 1594631.
- ↑ Dengjel J, Kratchmarova I, Blagoev B (October 2009). "रिसेप्टर टाइरोसिन किनेज सिग्नलिंग: क्वांटिटेटिव प्रोटिओमिक्स से एक दृश्य". Molecular BioSystems. 5 (10): 1112–1121. doi:10.1039/b909534a. PMID 19756300.
- ↑ 7.0 7.1 7.2 7.3 7.4 {{cite journal | vauthors = Wiley HS, Burke PM | title = एंडोसाइटिक ट्रैफिकिंग द्वारा रिसेप्टर टाइरोसिन किनेज सिग्नलिंग का विनियमन| journal = Traffic | volume = 2 | issue = 1 | pages = 12–18 | date = January 2001 | pmid = 11208164 | doi = 10.1034/j.1600-0854.2001.020103.x | s2cid = 7329602 }
- ↑ {{cite journal | vauthors = Rinker S, Ke Y, Liu Y, Chhabra R, Yan H | title = दूरी पर निर्भर बहुस्तरीय लिगैंड-प्रोटीन बाइंडिंग के लिए स्व-इकट्ठे डीएनए नैनोस्ट्रक्चर| journal = Nature Nanotechnology | volume = 3 | issue = 7 | pages = 418–422 | date = July 2008 | pmid = 18654566 | pmc = 2556356 | doi = 10.1038/nnano.2008.164 }
- ↑ 9.0 9.1 9.2 {{cite journal | vauthors = Silvennoinen O, Saharinen P, Paukku K, Takaluoma K, Kovanen P | title = जेक टाइरोसिन किनेसिस और स्टेट ट्रांसक्रिप्शन कारकों के माध्यम से साइटोकाइन रिसेप्टर सिग्नल ट्रांसडक्शन| journal = APMIS | volume = 105 | issue = 7 | pages = 497–509 | date = July 1997 | pmid = 9269296 | doi = 10.1111/j.1699-0463.1997.tb05047.x | s2cid = 21902484 }
- ↑ Modi V, Dunbrack RL (April 2019). "सक्रिय और निष्क्रिय किनेसेस की संरचनाओं के लिए एक नया नामकरण परिभाषित करना". Proceedings of the National Academy of Sciences of the United States of America. 116 (14): 6818–6827. doi:10.1073/pnas.1814279116. PMC 6452665. PMID 30867294.
- ↑ Bhise SB, Nalawade AD, Wadhawa H (December 2004). "कैंसर चिकित्सा विज्ञान में प्रोटीन टाइरोसिन किनेज अवरोधकों की भूमिका". Indian Journal of Biochemistry & Biophysics. 41 (6): 273–280. PMID 22900354.
- ↑ Gunby RH, Sala E, Tartari CJ, Puttini M, Gambacorti-Passerini C, Mologni L (November 2007). "एंटी-कैंसर थेरेपी के लिए आणविक लक्ष्य के रूप में ऑन्कोजेनिक फ्यूजन टाइरोसिन किनेसिस". Anti-Cancer Agents in Medicinal Chemistry. 7 (6): 594–611. doi:10.2174/187152007784111340. PMID 18045055.
- ↑ Tontonoz, Matthew (December 27, 2017). "कैसे एक मुर्गे ने कैंसर के रहस्य को सुलझाने में मदद की". Memorial Sloan Kettering Cancer Center. Retrieved 27 October 2022.
- ↑ Weinberg RA (2007). The Biology of Cancer. New York: Garland Science, Taylor & Francis Group, LLC. pp. 757–759. ISBN 978-0-8153-4076-8.
- ↑ 15.00 15.01 15.02 15.03 15.04 15.05 15.06 15.07 15.08 15.09 15.10 15.11 15.12 Kris MG, Natale RB, Herbst RS, Lynch TJ, Prager D, Belani CP, et al. (October 2003). "Efficacy of gefitinib, an inhibitor of the epidermal growth factor receptor tyrosine kinase, in symptomatic patients with non-small cell lung cancer: a randomized trial". JAMA. 290 (16): 2149–2158. doi:10.1001/jama.290.16.2149. PMID 14570950.
- ↑ 16.0 16.1 Sordella R, Bell DW, Haber DA, Settleman J (August 2004). "Gefitinib-sensitizing EGFR mutations in lung cancer activate anti-apoptotic pathways". Science. 305 (5687): 1163–1167. Bibcode:2004Sci...305.1163S. doi:10.1126/science.1101637. PMID 15284455. S2CID 34389318.
- ↑ 17.0 17.1 Okamoto I (January 2010). "Epidermal growth factor receptor in relation to tumor development: EGFR-targeted anticancer therapy". The FEBS Journal. 277 (2): 309–315. doi:10.1111/j.1742-4658.2009.07449.x. PMID 19922468.
- ↑ {{cite journal | vauthors = Druker BJ, Talpaz M, Resta DJ, Peng B, Buchdunger E, Ford JM, Lydon NB, Kantarjian H, Capdeville R, Ohno-Jones S, Sawyers CL | display-authors = 6 | title = जीर्ण माइलॉयड ल्यूकेमिया में बीसीआर-एबीएल टाइरोसिन किनसे के एक विशिष्ट अवरोधक की प्रभावकारिता और सुरक्षा| journal = The New England Journal of Medicine | volume = 344 | issue = 14 | pages = 1031–1037 | date = April 2001 | pmid = 11287972 | doi = 10.1056/NEJM200104053441401 | url = http://pdfs.semanticscholar.org/1abb/4b6b3dcdf06bbd6761e3509c9d23645aa487.pdf | url-status = dead | s2cid = 8399298 | archive-url = https://web.archive.org/web/20190219204727/http://pdfs.semanticscholar.org/1abb/4b6b3dcdf06bbd6761e3509c9d23645aa487.pdf | archive-date = 2019-02-19 }
- ↑ 19.0 19.1 19.2 19.3 19.4 19.5 {{cite journal | vauthors = Joensuu H, Roberts PJ, Sarlomo-Rikala M, Andersson LC, Tervahartiala P, Tuveson D, Silberman S, Capdeville R, Dimitrijevic S, Druker B, Demetri GD | display-authors = 6 | title = मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर वाले रोगी में टाइरोसिन किनेज अवरोधक STI571 का प्रभाव| journal = The New England Journal of Medicine | volume = 344 | issue = 14 | pages = 1052–1056 | date = April 2001 | pmid = 11287975 | doi = 10.1056/NEJM200104053441404 }
- ↑ 20.0 20.1 20.2 Blanke CD, Demetri GD, von Mehren M, Heinrich MC, Eisenberg B, Fletcher JA, et al. (February 2008). "केआईटी को व्यक्त करने वाले अनियंत्रित या मेटास्टैटिक गैस्ट्रोइंटेस्टाइनल स्ट्रोमल ट्यूमर वाले रोगियों के लिए मानक-बनाम उच्च-खुराक इमैटिनिब मेसाइलेट के एक यादृच्छिक चरण II परीक्षण से दीर्घकालिक परिणाम". Journal of Clinical Oncology. 26 (4): 620–625. CiteSeerX 10.1.1.690.6356. doi:10.1200/JCO.2007.13.4403. PMID 18235121.
- ↑ 21.0 21.1 {{cite journal | vauthors = le Coutre P, Ottmann OG, Giles F, Kim DW, Cortes J, Gattermann N, Apperley JF, Larson RA, Abruzzese E, O'Brien SG, Kuliczkowski K, Hochhaus A, Mahon FX, Saglio G, Gobbi M, Kwong YL, Baccarani M, Hughes T, Martinelli G, Radich JP, Zheng M, Shou Y, Kantarjian H | display-authors = 6 | title = Nilotinib (पूर्व में AMN107), एक अत्यधिक चयनात्मक BCR-ABL टाइरोसिन किनसे अवरोधक, इमैटिनिब-प्रतिरोधी या -इन्टॉलरेंट त्वरित-चरण क्रोनिक मायलोजेनस ल्यूकेमिया वाले रोगियों में सक्रिय है।| journal = Blood | volume = 111 | issue = 4 | pages = 1834–1839 | date = February 2008 | pmid = 18048643 | doi = 10.1182/blood-2007-04-083196 | doi-access = free }
- ↑ Kuwai T, Nakamura T, Sasaki T, Kim SJ, Fan D, Villares GJ, et al. (May 2008). "ट्यूमर से जुड़े एंडोथेलियल कोशिकाओं पर फॉस्फोराइलेटेड एपिडर्मल ग्रोथ फैक्टर रिसेप्टर टाइरोसिन किनेज इनहिबिटर के साथ थेरेपी का प्राथमिक लक्ष्य है". Neoplasia. 10 (5): 489–500. doi:10.1593/neo.08200. PMC 2373870. PMID 18472966.
- ↑ Rivera-Torres J, San José E (2019). "Src टायरोसिन किनेज इनहिबिटर्स: उनके इम्यून, एंटीवायरल और सेनोथेराप्यूटिक पोटेंशियल पर नए दृष्टिकोण". Frontiers in Pharmacology. 10: 1011. doi:10.3389/fphar.2019.01011. PMC 6759511. PMID 31619990.
बाहरी संबंध
- Eukaryotic Linear Motif resource motif class MOD_TYR_CSK
- Tyrosine Kinases on KinCore: the Kinase Conformation Resource: A web resource for protein kinase sequence, structure and phylogeny
- The Tyrosine Kinase group
- Overview of all the structural information available in the PDB for UniProt: P08631 (Tyrosine-protein kinase HCK) at the PDBe-KB.
- Overview of all the structural information available in the PDB for UniProt: P00520 (Tyrosine-protein kinase ABL1) at the PDBe-KB.
- Overview of all the structural information available in the PDB for UniProt: O60674 (Tyrosine-protein kinase JAK2) at the PDBe-KB.