आणविक कक्षक: Difference between revisions
No edit summary |
No edit summary |
||
| Line 1: | Line 1: | ||
{{Short description|Wave-like behavior of an electron in a molecule}} | {{Short description|Wave-like behavior of an electron in a molecule}} | ||
{{See also|आणविक कक्षीय सिद्धांत|आणविक कक्षीय आरेख}} | {{See also|आणविक कक्षीय सिद्धांत|आणविक कक्षीय आरेख}} | ||
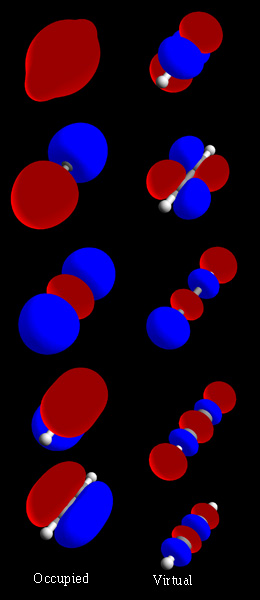
[[File:Orbitals acetylene.jpg|right|thumb|पूर्ण [[एसिटिलीन]] (H-C≡C-H) आणविक कक्षीय सेट। बायां स्तंभ एमओ को दर्शाता है जो जमीनी अवस्था में व्याप्त हैं, शीर्ष पर सबसे कम ऊर्जा कक्षीय है। कुछ MO में दिखाई देने वाली सफेद और भूरे रंग की रेखा नाभिक से | [[File:Orbitals acetylene.jpg|right|thumb|पूर्ण [[एसिटिलीन]] (H-C≡C-H) आणविक कक्षीय सेट। बायां स्तंभ एमओ को दर्शाता है जो जमीनी अवस्था में व्याप्त हैं, शीर्ष पर सबसे कम ऊर्जा कक्षीय है। कुछ MO में दिखाई देने वाली सफेद और भूरे रंग की रेखा नाभिक से निकलने वाली आणविक धुरी है। कक्षीय तरंग कार्य लाल क्षेत्रों में सकारात्मक और नीले क्षेत्रों में नकारात्मक होते हैं। दायां कॉलम आभासी एमओ को दर्शाता है जो जमीनी अवस्था में खाली हैं, किन्तु उत्तेजित अवस्था में व्याप्त हो सकते हैं।]][[रसायन विज्ञान]] में, आणविक कक्षक ({{IPAc-en|ɒr|b|ə|d|l}}) [[फ़ंक्शन (गणित)|फलन (गणित)]] है जो [[अणु]] में [[इलेक्ट्रॉन]] के स्थान और पदार्थ तरंग जैसे व्यवहार का वर्णन करता है। इस फलन का उपयोग रासायनिक और भौतिक गुणों की गणना करने के लिए किया जा सकता है जैसे कि किसी विशिष्ट क्षेत्र में इलेक्ट्रॉन खोजने की संभावना परमाणु कक्षक और आणविक कक्षक शब्द {{efn|Prior to Mulliken, the word "orbital" was used only as an [[adjective]], for example "orbital velocity" or "orbital wave function."<ref>{{cite book |title=orbital |publisher=[[Merriam-Webster]] |work=Dictionary by Merriam-Webster: America's most-trusted online dictionary |url=https://www.merriam-webster.com/dictionary/orbital |accessdate=April 18, 2021}}</ref> Mulliken used orbital as a [[noun]], when he suggested the terms "atomic orbitals" and "molecular orbitals" to describe the electronic structures of polyatomic molecules.<ref name="muller1932"/><ref>{{cite book | last = Brown | first = Theodore | title = Chemistry : the central science | publisher = Prentice Hall | location = Upper Saddle River, NJ | year = 2002 | isbn = 0-13-066997-0 }}</ref>}} को 1932 में रॉबर्ट एस. मुल्लिकेन द्वारा एक-इलेक्ट्रॉन कक्षीय तरंग कार्यों के अर्थ में प्रयुक्त किया गया था।<ref name="muller1932">{{cite journal| last=Mulliken | first=Robert S. | title=बहुपरमाणुक अणुओं और संयोजकता की इलेक्ट्रॉनिक संरचनाएँ। द्वितीय. सामान्य विचार|date=July 1932| journal=[[Physical Review]] | volume=41 | issue=1 | pages=49–71 | bibcode = 1932PhRv...41...49M | doi = 10.1103/PhysRev.41.49}}</ref> प्रारंभिक स्तर पर, उनका उपयोग अंतरिक्ष के उस क्षेत्र का वर्णन करने के लिए किया जाता है जिसमें किसी फलन का महत्वपूर्ण आयाम होता है। | ||
एक पृथक परमाणु में, कक्षीय इलेक्ट्रॉनों का स्थान [[परमाणु कक्षक]] नामक कार्यों द्वारा निर्धारित होता है। जब कई परमाणु रासायनिक रूप से अणु में संयोजित होते हैं, जिससे इलेक्ट्रॉनों का स्थान समग्र रूप से अणु द्वारा निर्धारित होता है, इसलिए परमाणु कक्षाएँ मिलकर आणविक कक्षाएँ बनाती हैं। घटक परमाणुओं से इलेक्ट्रॉन आणविक कक्षाओं पर अभिग्रहण कर लेते हैं। गणितीय रूप से, आणविक कक्षाएँ अणु के [[परमाणु नाभिक]] के क्षेत्र में इलेक्ट्रॉनों के लिए श्रोडिंगर समीकरण का अनुमानित समाधान हैं। इनका निर्माण सामान्यतः अणु के प्रत्येक परमाणु से परमाणु ऑर्बिटल्स परमाणु ऑर्बिटल्स या [[ संकर कक्षीय |संकर कक्षीय]] या परमाणुओं के समूहों से अन्य आणविक ऑर्बिटल्स के रैखिक संयोजन द्वारा किया जाता है। उन्हें हार्ट्री-फॉक विधि हार्ट्री-फॉक या सेल्फ-कंसिस्टेंट फील्ड (एससीएफ) विधियों का उपयोग करके मात्रात्मक रूप से गणना की जा सकती है। | एक पृथक परमाणु में, कक्षीय इलेक्ट्रॉनों का स्थान [[परमाणु कक्षक]] नामक कार्यों द्वारा निर्धारित होता है। जब कई परमाणु रासायनिक रूप से अणु में संयोजित होते हैं, जिससे इलेक्ट्रॉनों का स्थान समग्र रूप से अणु द्वारा निर्धारित होता है, इसलिए परमाणु कक्षाएँ मिलकर आणविक कक्षाएँ बनाती हैं। घटक परमाणुओं से इलेक्ट्रॉन आणविक कक्षाओं पर अभिग्रहण कर लेते हैं। गणितीय रूप से, आणविक कक्षाएँ अणु के [[परमाणु नाभिक]] के क्षेत्र में इलेक्ट्रॉनों के लिए श्रोडिंगर समीकरण का अनुमानित समाधान हैं। इनका निर्माण सामान्यतः अणु के प्रत्येक परमाणु से परमाणु ऑर्बिटल्स परमाणु ऑर्बिटल्स या [[ संकर कक्षीय |संकर कक्षीय]] या परमाणुओं के समूहों से अन्य आणविक ऑर्बिटल्स के रैखिक संयोजन द्वारा किया जाता है। उन्हें हार्ट्री-फॉक विधि हार्ट्री-फॉक या सेल्फ-कंसिस्टेंट फील्ड (एससीएफ) विधियों का उपयोग करके मात्रात्मक रूप से गणना की जा सकती है। | ||
| Line 10: | Line 10: | ||
एक आणविक कक्षक (एमओ) का उपयोग अणु में उन क्षेत्रों का प्रतिनिधित्व करने के लिए किया जा सकता है जहां उस कक्षक पर अभिग्रहण करने वाले [[ऋणावेशित सूक्ष्म अणु का विन्यास]] पाए जाने की संभावना है। आणविक कक्षाएँ अणु के [[परमाणु नाभिक]] के विद्युत क्षेत्र में इलेक्ट्रॉनों के लिए श्रोडिंगर समीकरण के अनुमानित समाधान हैं। चूँकि इस समीकरण से सीधे ऑर्बिटल्स की गणना करना बहुत ही कठिन समस्या है। इसके अतिरिक्त वे परमाणु कक्षाओं के संयोजन से प्राप्त होते हैं, जो परमाणु में इलेक्ट्रॉन के स्थान की पूर्वानुमान करते हैं। आणविक कक्षक अणु के इलेक्ट्रॉन विन्यास को निर्दिष्ट कर सकता है: (या जोड़ी) इलेक्ट्रॉन का स्थानिक वितरण और ऊर्जा सामान्यतः एमओ को परमाणु कक्षाओं के रैखिक संयोजन आणविक कक्षीय विधि (एलसीएओ-एमओ विधि) के रूप में दर्शाया जाता है, विशेष रूप से गुणात्मक या बहुत अनुमानित उपयोग में वे [[आणविक कक्षीय सिद्धांत]] के माध्यम से समझे गए अणुओं में बंध का सरल मॉडल प्रदान करने में अमूल्य हैं। | एक आणविक कक्षक (एमओ) का उपयोग अणु में उन क्षेत्रों का प्रतिनिधित्व करने के लिए किया जा सकता है जहां उस कक्षक पर अभिग्रहण करने वाले [[ऋणावेशित सूक्ष्म अणु का विन्यास]] पाए जाने की संभावना है। आणविक कक्षाएँ अणु के [[परमाणु नाभिक]] के विद्युत क्षेत्र में इलेक्ट्रॉनों के लिए श्रोडिंगर समीकरण के अनुमानित समाधान हैं। चूँकि इस समीकरण से सीधे ऑर्बिटल्स की गणना करना बहुत ही कठिन समस्या है। इसके अतिरिक्त वे परमाणु कक्षाओं के संयोजन से प्राप्त होते हैं, जो परमाणु में इलेक्ट्रॉन के स्थान की पूर्वानुमान करते हैं। आणविक कक्षक अणु के इलेक्ट्रॉन विन्यास को निर्दिष्ट कर सकता है: (या जोड़ी) इलेक्ट्रॉन का स्थानिक वितरण और ऊर्जा सामान्यतः एमओ को परमाणु कक्षाओं के रैखिक संयोजन आणविक कक्षीय विधि (एलसीएओ-एमओ विधि) के रूप में दर्शाया जाता है, विशेष रूप से गुणात्मक या बहुत अनुमानित उपयोग में वे [[आणविक कक्षीय सिद्धांत]] के माध्यम से समझे गए अणुओं में बंध का सरल मॉडल प्रदान करने में अमूल्य हैं। | ||
कम्प्यूटेशनल रसायन विज्ञान में अधिकांश वर्तमान विधियां सिस्टम के एमओ की गणना से प्रारंभ होती हैं। आणविक कक्षक नाभिक द्वारा उत्पन्न विद्युत क्षेत्र में इलेक्ट्रॉन के व्यवहार और अन्य इलेक्ट्रॉनों के कुछ औसत वितरण का वर्णन करता है। एक ही कक्षा में रहने वाले दो इलेक्ट्रॉनों के स्थिति में, [[पाउली सिद्धांत]] की मांग है कि उनके पास विपरीत स्पिन हो आवश्यक रूप से यह अनुमान है, और आणविक इलेक्ट्रॉनिक तरंग फलन के अत्यधिक स्पष्ट विवरण में ऑर्बिटल्स नहीं होते हैं ([[कॉन्फ़िगरेशन इंटरेक्शन]] देखें)। | कम्प्यूटेशनल रसायन विज्ञान में अधिकांश वर्तमान विधियां सिस्टम के एमओ की गणना से प्रारंभ होती हैं। आणविक कक्षक नाभिक द्वारा उत्पन्न विद्युत क्षेत्र में इलेक्ट्रॉन के व्यवहार और अन्य इलेक्ट्रॉनों के कुछ औसत वितरण का वर्णन करता है। एक ही कक्षा में रहने वाले दो इलेक्ट्रॉनों के स्थिति में, [[पाउली सिद्धांत]] की मांग है कि उनके पास विपरीत स्पिन हो आवश्यक रूप से यह अनुमान है, और आणविक इलेक्ट्रॉनिक तरंग फलन के अत्यधिक स्पष्ट विवरण में ऑर्बिटल्स नहीं होते हैं ([[कॉन्फ़िगरेशन इंटरेक्शन|विन्यास इंटरेक्शन]] देखें)। | ||
सामान्यतः, आणविक कक्षाएँ पूरे अणु में स्थानीयकृत होती हैं। इसके अतिरिक्त, यदि अणु में समरूपता तत्व हैं, तो इसके गैर-अपक्षयी आणविक कक्षाएँ इनमें से किसी भी समरूपता के संबंध में या तो सममित या एंटीसिमेट्रिक हैं। दूसरे शब्दों में, आणविक कक्षीय ψ में समरूपता ऑपरेशन | सामान्यतः, आणविक कक्षाएँ पूरे अणु में स्थानीयकृत होती हैं। इसके अतिरिक्त, यदि अणु में समरूपता तत्व हैं, तो इसके गैर-अपक्षयी आणविक कक्षाएँ इनमें से किसी भी समरूपता के संबंध में या तो सममित या एंटीसिमेट्रिक हैं। दूसरे शब्दों में, आणविक कक्षीय ψ में समरूपता ऑपरेशन s (उदाहरण के लिए, प्रतिबिंब, घूर्णन, या व्युत्क्रम) के अनुप्रयोग के परिणामस्वरूप आणविक कक्षक अपरिवर्तित होता है या इसके गणितीय चिह्न को उलट देता है: Sψ = ±ψ। उदाहरण के लिए, तलीय अणुओं में, आणविक तल में परावर्तन के संबंध में आणविक कक्षाएँ या तो सममित ([[सिग्मा बांड]]) या एंटीसिमेट्रिक (पीआई बांड) होती हैं। यदि विकृत कक्षीय ऊर्जा वाले अणुओं पर भी विचार किया जाता है, तो अधिक सामान्य कथन यह है कि आणविक कक्षाएँ अणु के [[समरूपता समूह]] के [[अघुलनशील प्रतिनिधित्व]] के लिए आधार बनाती हैं।<ref>{{Cite book|url=https://archive.org/details/isbn_9780471510949/page/102|title=समूह सिद्धांत के रासायनिक अनुप्रयोग|last=Cotton|first=F. Albert|date=1990|publisher=Wiley|isbn=0471510947|edition=3rd|location=New York|pages=[https://archive.org/details/isbn_9780471510949/page/102 102]|oclc=19975337|url-access=registration}}</ref> आणविक ऑर्बिटल्स के समरूपता गुणों का कारण है कि डेलोकलाइज़ेशन आणविक ऑर्बिटल सिद्धांत की अंतर्निहित विशेषता है और इसे मूल रूप से (और पूरक) वैलेंस बॉन्ड सिद्धांत से अलग बनाता है, जिसमें बॉन्ड को स्थानीयकृत इलेक्ट्रॉन जोड़े के रूप में देखा जाता है, [[अनुनाद (रसायन विज्ञान)]] के लिए छूट के साथ स्थानीयकरण के लिए किया जाता है. | ||
इन समरूपता-अनुकूलित विहित आणविक कक्षाओं के विपरीत, विहित कक्षाओं में कुछ गणितीय परिवर्तन प्रयुक्त करके [[स्थानीयकृत आणविक कक्षाएँ]] बनाई जा सकती हैं। इस दृष्टिकोण का लाभ यह है कि ऑर्बिटल्स अणु के बंधनों के अधिक निकट से मेल खाएंगे जैसा कि लुईस संरचना द्वारा दर्शाया गया है। इस प्रकार हानि के रूप में, इन स्थानीयकृत कक्षाओं के ऊर्जा स्तर का अब भौतिक अर्थ नहीं रह गया है। (इस लेख के अतिरिक्त भाग में चर्चा कैनोनिकल आणविक ऑर्बिटल्स पर केंद्रित होगी। स्थानीयकृत आणविक ऑर्बिटल्स पर आगे की चर्चा के लिए, देखें: प्राकृतिक बॉन्ड ऑर्बिटल और सिग्मा-पीआई और समकक्ष-ऑर्बिटल मॉडल।) | इन समरूपता-अनुकूलित विहित आणविक कक्षाओं के विपरीत, विहित कक्षाओं में कुछ गणितीय परिवर्तन प्रयुक्त करके [[स्थानीयकृत आणविक कक्षाएँ]] बनाई जा सकती हैं। इस दृष्टिकोण का लाभ यह है कि ऑर्बिटल्स अणु के बंधनों के अधिक निकट से मेल खाएंगे जैसा कि लुईस संरचना द्वारा दर्शाया गया है। इस प्रकार हानि के रूप में, इन स्थानीयकृत कक्षाओं के ऊर्जा स्तर का अब भौतिक अर्थ नहीं रह गया है। (इस लेख के अतिरिक्त भाग में चर्चा कैनोनिकल आणविक ऑर्बिटल्स पर केंद्रित होगी। स्थानीयकृत आणविक ऑर्बिटल्स पर आगे की चर्चा के लिए, देखें: प्राकृतिक बॉन्ड ऑर्बिटल और सिग्मा-पीआई और समकक्ष-ऑर्बिटल मॉडल।) | ||
| Line 74: | Line 74: | ||
{{Further|फ़ाई बांड}} | {{Further|फ़ाई बांड}} | ||
{{multiple image | {{multiple image | ||
| footer = | | footer = फाई आणविक कक्षक (एक फाई बंधन) बनाने के लिए उपयुक्त रूप से संरेखित एफ परमाणु कक्षाएँ ओवरलैप होती हैं | ||
| width = 120 | | width = 120 | ||
| image1 = Phi-bond-f-orbitals-2D.png | | image1 = Phi-bond-f-orbitals-2D.png | ||
| image2 = Phi-bond-boundary-surface-diagram-2D.png | | image2 = Phi-bond-boundary-surface-diagram-2D.png | ||
| caption = | | caption = उपयुक्त रूप से संरेखित f परमाणु ऑर्बिटल्स एक फाई आणविक ऑर्बिटल (एक फाई बॉन्ड) बनाने के लिए ओवरलैप कर सकते हैं | ||
}} | }} | ||
सैद्धांतिक रसायनज्ञों ने अनुमान लगाया है कि उच्च-क्रम के बंध, जैसे कि एफ परमाणु कक्षाओं के ओवरलैप के अनुरूप फाई बांड, संभव हैं। फाई बांड युक्त अणु का कोई ज्ञात उदाहरण नहीं है। | सैद्धांतिक रसायनज्ञों ने अनुमान लगाया है कि उच्च-क्रम के बंध, जैसे कि एफ परमाणु कक्षाओं के ओवरलैप के अनुरूप फाई बांड, संभव हैं। फाई बांड युक्त अणु का कोई ज्ञात उदाहरण नहीं है। | ||
| Line 156: | Line 156: | ||
====H<sub>2</sub>==== | ====H<sub>2</sub>==== | ||
[[File:H2OrbitalsAnimation.gif|thumb|right|300px|एक अकेले हाइड्रोजन परमाणु (बाएं और दाएं) के परमाणु कक्षक और | [[File:H2OrbitalsAnimation.gif|thumb|right|300px|एक अकेले हाइड्रोजन परमाणु (बाएं और दाएं) के परमाणु कक्षक और H<sub>2</sub> के संबंधित बंध (नीचे) और प्रतिरक्षी (ऊपर) आणविक कक्षा के लिए इलेक्ट्रॉन तरंग कार्य अणु. तरंगक्रिया का वास्तविक भाग नीला वक्र है, और [[काल्पनिक भाग]] लाल वक्र है। लाल बिंदु नाभिक के स्थान को चिह्नित करते हैं। इलेक्ट्रॉन तरंग फलन श्रोडिंगर तरंग समीकरण के अनुसार दोलन करता है, और ऑर्बिटल्स इसकी खड़ी तरंगें हैं। स्थायी तरंग आवृत्ति कक्षीय की गतिज ऊर्जा के समानुपाती होती है। (यह कथानक त्रि-आयामी प्रणाली का आयामी टुकड़ा है।)]]एक सरल MO उदाहरण के रूप में, [[हाइड्रोजन]] अणु, H<sub>2</sub> में इलेक्ट्रॉनों पर विचार करें (MO आरेख डायटोमिक MO आरेख देखें), दो परमाणुओं को H' और H लेबल के साथ। सबसे कम ऊर्जा वाले परमाणु कक्षक, 1s' और 1s, अणु की समरूपता के अनुसार परिवर्तित नहीं होते हैं। चूँकि, निम्नलिखित समरूपता अनुकूलित परमाणु कक्षाएँ करती हैं: | ||
{| class="wikitable" | {| class="wikitable" | ||
| Line 169: | Line 169: | ||
====He<sub>2</sub>==== | ====He<sub>2</sub>==== | ||
दूसरी ओर, He<sub>2</sub> के काल्पनिक अणु पर विचार करें He' और He लेबल वाले परमाणुओं के साथ। जैसा कि | दूसरी ओर, He<sub>2</sub> के काल्पनिक अणु पर विचार करें He' और He लेबल वाले परमाणुओं के साथ। जैसा कि H<sub>2</sub> के साथ है, सबसे कम ऊर्जा वाले परमाणु ऑर्बिटल्स 1s' और 1s हैं, और अणु की समरूपता के अनुसार परिवर्तित नहीं होते हैं, जबकि समरूपता अनुकूलित परमाणु ऑर्बिटल्स करते हैं। सममित संयोजन - बॉन्डिंग ऑर्बिटल - आधार ऑर्बिटल्स की तुलना में ऊर्जा में कम है, और एंटीसिमेट्रिक संयोजन - एंटीबॉन्डिंग ऑर्बिटल - अधिक है। H<sub>2</sub> के विपरीत, दो वैलेंस इलेक्ट्रॉनों के साथ, He<sub>2</sub> इसकी तटस्थ जमीनी अवस्था में चार हैं। दो इलेक्ट्रॉन निम्न-ऊर्जा बंध कक्षक, σ<sub>g</sub>(1s) को भरते हैं, जबकि शेष दो उच्च-ऊर्जा प्रतिरक्षी कक्षक, σ<sub>u</sub>*(1s) को भरते हैं. इस प्रकार, अणु के चारों ओर परिणामी इलेक्ट्रॉन घनत्व दो परमाणुओं के बीच बंध के गठन का समर्थन नहीं करता है; परमाणुओं को साथ बांधे रखने वाले स्थिर बंध के बिना, अणु के अस्तित्व की उम्मीद नहीं की जा सकती है। इसे देखने का दूसरा तरीका यह है कि दो बंधनकारी इलेक्ट्रॉन और दो प्रतिरक्षी इलेक्ट्रॉन हैं; इसलिए, बंध क्रम 0 है और कोई बंध उपस्थित नहीं है (अणु में वान डेर वाल्स क्षमता द्वारा समर्थित बाध्य अवस्था है)। | ||
==== | ====He<sub>2</sub>==== | ||
[[डिलिथियम]] | [[डिलिथियम]] Li<sub>2</sub> दो ली परमाणुओं के 1s और 2s परमाणु कक्षाओं (आधार सेट) के ओवरलैप से बनता है। प्रत्येक ली परमाणु बॉन्डिंग इंटरैक्शन के लिए तीन इलेक्ट्रॉनों का योगदान देता है, और छह इलेक्ट्रॉन सबसे कम ऊर्जा के तीन एमओ को भरते हैं, σ<sub>g</sub>(1एस), p<sub>u</sub>*(1s), और p<sub>g</sub>(2s). बांड क्रम के लिए समीकरण का उपयोग करते हुए, यह पाया गया है कि डाइलिथियम का बंध क्रम एक, एकल बंध है।<ref>{{Cite journal |last=König |first=Burkhard |date=1995-02-21 |title=Chemical Bonding. VonM. J. Winter. 90 S., ISBN 0-19-855694-2. – Organometallics 1. Complexes with Transition Metal-Carbon σ-Bonds. VonM. Bochmann. 91 S., ISBN 0-19-855751-5. – Organometallics 2. Complexes with Transition Metal-Carbon π-Bonds. VonM. Bochmann. 89 S., ISBN 0-19-855813-9. – Bifunctional Compounds. VonR. S. Ward. 90 S., ISBN 0-19-855808-2. – Alle aus der Reihe: Oxford Chemistry Primers, Oxford University Press, Oxford, 1994, Broschur, je 4.99 £ |url=https://onlinelibrary.wiley.com/doi/10.1002/ange.19951070434 |journal=Angewandte Chemie |language=de |volume=107 |issue=4 |pages=540–540 |doi=10.1002/ange.19951070434}}</ref> | ||
====उत्कृष्ट गैसें==== | ====उत्कृष्ट गैसें==== | ||
He | He<sub>2</sub> के काल्पनिक अणु पर विचार करना, चूँकि परमाणु कक्षकों का आधार समुच्चय H<sub>2</sub> के स्थिति जैसा ही है, हम पाते हैं कि बॉन्डिंग और एंटीबॉन्डिंग ऑर्बिटल्स दोनों भरे हुए हैं, इसलिए जोड़ी को कोई ऊर्जा लाभ नहीं है। He को थोड़ा ऊर्जा लाभ होगा, किन्तु H<sub>2</sub> + 2 जितना नहीं वह, इसलिए अणु बहुत अस्थिर है और हाइड्रोजन और हीलियम में विघटित होने से पहले केवल कुछ समय के लिए ही उपस्थित रहता है। सामान्यतः, हम पाते हैं कि हे जैसे परमाणु जिनमें पूर्ण ऊर्जा कोश होते हैं वे संभवतः ही कभी अन्य परमाणुओं के साथ बंधते हैं। अल्पकालिक [[वैन डेर वाल्स बॉन्डिंग]] को छोड़कर, बहुत कम [[उत्कृष्ट गैस यौगिक]] ज्ञात हैं। | ||
===हेटेरोन्यूक्लियर डायटोमिक्स=== | ===हेटेरोन्यूक्लियर डायटोमिक्स=== | ||
| Line 182: | Line 182: | ||
====एचएफ==== | ====एचएफ==== | ||
[[ हाइड्रोजिन फ्लोराइड | हाइड्रोजिन फ्लोराइड]] में | [[ हाइड्रोजिन फ्लोराइड | हाइड्रोजिन फ्लोराइड]] में H 1 s और एफ 2 s ऑर्बिटल्स के बीच एचएफ ओवरलैप को समरूपता द्वारा अनुमति दी जाती है किन्तु दो परमाणु ऑर्बिटल्स के बीच ऊर्जा में अंतर उन्हें आणविक ऑर्बिटल बनाने के लिए परस्पर क्रिया करने से रोकता है। H 1s और F 2p<sub>z</sub> के बीच ओवरलैप ऑर्बिटल्स में भी समरूपता की अनुमति है, और इन दो परमाणु ऑर्बिटल्स में थोड़ी ऊर्जा पृथक्करण है। इस प्रकार, वे परस्पर क्रिया करते हैं, जिससे σ और σ* MOs और 1 के बंध क्रम के साथ अणु का निर्माण होता है। चूंकि HF गैर-सेंट्रोसिमेट्रिक अणु है, समरूपता लेबल g और u इसके आणविक कक्षाओं पर प्रयुक्त नहीं होते हैं।<ref>Catherine E. Housecroft, Alan G, Sharpe, Inorganic Chemistry, Pearson Prentice Hall; 2nd Edition, 2005, {{ISBN|0130-39913-2}}, p. 41-43.</ref> | ||
==मात्रात्मक दृष्टिकोण== | ==मात्रात्मक दृष्टिकोण== | ||
आणविक ऊर्जा स्तरों के लिए मात्रात्मक मान प्राप्त करने के लिए, किसी को ऐसे आणविक ऑर्बिटल्स की आवश्यकता होती है जो | आणविक ऊर्जा स्तरों के लिए मात्रात्मक मान प्राप्त करने के लिए, किसी को ऐसे आणविक ऑर्बिटल्स की आवश्यकता होती है जो विन्यास इंटरैक्शन (सीआई) विस्तार [[पूर्ण कॉन्फ़िगरेशन इंटरैक्शन|पूर्ण विन्यास इंटरैक्शन]] सीमा की ओर तेजी से परिवर्तित हो जाती है। ऐसे कार्यों को प्राप्त करने की सबसे सामान्य विधि हार्ट्री-फॉक विधि है, जो आणविक कक्षाओं को [[फॉक ऑपरेटर]] के [[eigenfunction|ईजेनफंक्शन]] के रूप में व्यक्त करती है। सामान्यतः परमाणु नाभिक पर केंद्रित गाऊसी कार्यों के रैखिक संयोजन के रूप में आणविक कक्षाओं का विस्तार करके इस समस्या को हल किया जाता है (परमाणु कक्षाओं का रैखिक संयोजन आणविक कक्षीय विधि और [[आधार सेट (रसायन विज्ञान)]] देखें)। इन रैखिक संयोजनों के गुणांकों के लिए समीकरण सामान्यीकृत [[eigenvalue|आइजेनवैल्यू]] समीकरण है जिसे [[रूथान समीकरण]] के रूप में जाना जाता है, जो वास्तव में हार्ट्री-फॉक समीकरण का विशेष प्रतिनिधित्व है। ऐसे कई कार्य हैं जिनमें [[स्पार्टन (रसायन विज्ञान सॉफ्टवेयर)]] सहित एमओ की क्वांटम रासायनिक गणना की जा सकती है। | ||
सरल खाते अधिकांशतः सुझाव देते हैं कि प्रयोगात्मक आणविक कक्षीय ऊर्जा वैलेंस ऑर्बिटल्स के लिए [[पराबैंगनी फोटोइलेक्ट्रॉन स्पेक्ट्रोस्कोपी]] और कोर ऑर्बिटल्स के लिए [[एक्स - रे फ़ोटोइलैक्ट्रॉन स्पेक्ट्रोस्कोपी]] के | सरल खाते अधिकांशतः सुझाव देते हैं कि प्रयोगात्मक आणविक कक्षीय ऊर्जा वैलेंस ऑर्बिटल्स के लिए [[पराबैंगनी फोटोइलेक्ट्रॉन स्पेक्ट्रोस्कोपी]] और कोर ऑर्बिटल्स के लिए [[एक्स - रे फ़ोटोइलैक्ट्रॉन स्पेक्ट्रोस्कोपी|एक्स रे फ़ोटोइलैक्ट्रॉन स्पेक्ट्रोस्कोपी]] के विधियों से प्राप्त की जा सकती है। चूँकि, यह गलत है क्योंकि ये प्रयोग आयनीकरण ऊर्जा को मापते हैं, अणु और इलेक्ट्रॉन को हटाने के परिणामस्वरूप आयनों में से के बीच ऊर्जा में अंतर कूपमैन्स प्रमेय द्वारा आयनीकरण ऊर्जाएँ लगभग कक्षीय ऊर्जाओं से जुड़ी होती हैं। जबकि कुछ अणुओं के लिए इन दोनों मूल्यों के बीच समझौता निकट हो सकता है, अन्य मामलों में यह बहुत व्यर्थ हो सकता है। | ||
==टिप्पणियाँ== | ==टिप्पणियाँ == | ||
{{notes}} | {{notes}} | ||
==संदर्भ== | ==संदर्भ == | ||
{{Reflist}} | {{Reflist}} | ||
Revision as of 10:16, 11 July 2023
रसायन विज्ञान में, आणविक कक्षक (/ɒrbədl/) फलन (गणित) है जो अणु में इलेक्ट्रॉन के स्थान और पदार्थ तरंग जैसे व्यवहार का वर्णन करता है। इस फलन का उपयोग रासायनिक और भौतिक गुणों की गणना करने के लिए किया जा सकता है जैसे कि किसी विशिष्ट क्षेत्र में इलेक्ट्रॉन खोजने की संभावना परमाणु कक्षक और आणविक कक्षक शब्द [lower-alpha 1] को 1932 में रॉबर्ट एस. मुल्लिकेन द्वारा एक-इलेक्ट्रॉन कक्षीय तरंग कार्यों के अर्थ में प्रयुक्त किया गया था।[2] प्रारंभिक स्तर पर, उनका उपयोग अंतरिक्ष के उस क्षेत्र का वर्णन करने के लिए किया जाता है जिसमें किसी फलन का महत्वपूर्ण आयाम होता है।
एक पृथक परमाणु में, कक्षीय इलेक्ट्रॉनों का स्थान परमाणु कक्षक नामक कार्यों द्वारा निर्धारित होता है। जब कई परमाणु रासायनिक रूप से अणु में संयोजित होते हैं, जिससे इलेक्ट्रॉनों का स्थान समग्र रूप से अणु द्वारा निर्धारित होता है, इसलिए परमाणु कक्षाएँ मिलकर आणविक कक्षाएँ बनाती हैं। घटक परमाणुओं से इलेक्ट्रॉन आणविक कक्षाओं पर अभिग्रहण कर लेते हैं। गणितीय रूप से, आणविक कक्षाएँ अणु के परमाणु नाभिक के क्षेत्र में इलेक्ट्रॉनों के लिए श्रोडिंगर समीकरण का अनुमानित समाधान हैं। इनका निर्माण सामान्यतः अणु के प्रत्येक परमाणु से परमाणु ऑर्बिटल्स परमाणु ऑर्बिटल्स या संकर कक्षीय या परमाणुओं के समूहों से अन्य आणविक ऑर्बिटल्स के रैखिक संयोजन द्वारा किया जाता है। उन्हें हार्ट्री-फॉक विधि हार्ट्री-फॉक या सेल्फ-कंसिस्टेंट फील्ड (एससीएफ) विधियों का उपयोग करके मात्रात्मक रूप से गणना की जा सकती है।
आणविक कक्षाएँ तीन प्रकार की होती हैं: आबंधन आणविक कक्षाएँ जिनकी ऊर्जा उन्हें बनाने वाले परमाणु कक्षाओं की ऊर्जा से कम होती है, और इस प्रकार उन रासायनिक बंधों को बढ़ावा देती है जो अणु को साथ रखते हैं; प्रतिरक्षी आणविक ऑर्बिटल्स जिनकी ऊर्जा उनके घटक परमाणु ऑर्बिटल्स की ऊर्जा से अधिक होती है, और इसलिए अणु के बंध का विरोध करते हैं, और गैर-बंध ऑर्बिटल्स जिनकी ऊर्जा उनके घटक परमाणु ऑर्बिटल्स के समान होती है और इस प्रकार बॉन्डिंग पर कोई प्रभाव नहीं पड़ता है .
अवलोकन
एक आणविक कक्षक (एमओ) का उपयोग अणु में उन क्षेत्रों का प्रतिनिधित्व करने के लिए किया जा सकता है जहां उस कक्षक पर अभिग्रहण करने वाले ऋणावेशित सूक्ष्म अणु का विन्यास पाए जाने की संभावना है। आणविक कक्षाएँ अणु के परमाणु नाभिक के विद्युत क्षेत्र में इलेक्ट्रॉनों के लिए श्रोडिंगर समीकरण के अनुमानित समाधान हैं। चूँकि इस समीकरण से सीधे ऑर्बिटल्स की गणना करना बहुत ही कठिन समस्या है। इसके अतिरिक्त वे परमाणु कक्षाओं के संयोजन से प्राप्त होते हैं, जो परमाणु में इलेक्ट्रॉन के स्थान की पूर्वानुमान करते हैं। आणविक कक्षक अणु के इलेक्ट्रॉन विन्यास को निर्दिष्ट कर सकता है: (या जोड़ी) इलेक्ट्रॉन का स्थानिक वितरण और ऊर्जा सामान्यतः एमओ को परमाणु कक्षाओं के रैखिक संयोजन आणविक कक्षीय विधि (एलसीएओ-एमओ विधि) के रूप में दर्शाया जाता है, विशेष रूप से गुणात्मक या बहुत अनुमानित उपयोग में वे आणविक कक्षीय सिद्धांत के माध्यम से समझे गए अणुओं में बंध का सरल मॉडल प्रदान करने में अमूल्य हैं।
कम्प्यूटेशनल रसायन विज्ञान में अधिकांश वर्तमान विधियां सिस्टम के एमओ की गणना से प्रारंभ होती हैं। आणविक कक्षक नाभिक द्वारा उत्पन्न विद्युत क्षेत्र में इलेक्ट्रॉन के व्यवहार और अन्य इलेक्ट्रॉनों के कुछ औसत वितरण का वर्णन करता है। एक ही कक्षा में रहने वाले दो इलेक्ट्रॉनों के स्थिति में, पाउली सिद्धांत की मांग है कि उनके पास विपरीत स्प