यूनिकैक: Difference between revisions
No edit summary |
No edit summary |
||
| Line 1: | Line 1: | ||
{{short description|Model of phase equilibrium in statistical thermodynamics}} | {{short description|Model of phase equilibrium in statistical thermodynamics}} | ||
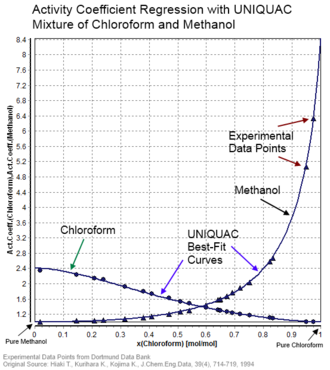
[[File:UNIQUACRegressionChloroformMethanol.png|thumb|गतिविधि गुणांकों का यूनिकैक [[प्रतिगमन विश्लेषण]] ([[ क्लोरोफार्म ]]/[[मेथनॉल]] मिश्रण)]][[सांख्यिकीय ऊष्मप्रवैगिकी]] में, '''यूनिकैक''' ('''सार्वभौमिक अर्ध-रासायनिक की प्रतिकृति''') एक [[गतिविधि गुणांक]] मॉडल है जिसका उपयोग [[चरण संतुलन]] के विवरण में किया जाता है।<ref name="AbramsPrausnitz1975">{{cite journal|last1=Abrams|first1=Denis S.|last2=Prausnitz|first2=John M.|title=Statistical thermodynamics of liquid mixtures: A new expression for the excess Gibbs energy of partly or completely miscible systems|journal=AIChE Journal|volume=21|issue=1|year=1975|pages=116–128|issn=0001-1541|doi=10.1002/aic.690210115}}</ref><ref name=":1">{{cite journal|last1=Maurer|first1=G.|last2=Prausnitz|first2=J.M.|title=अद्वितीय समीकरण की व्युत्पत्ति और विस्तार पर|journal=Fluid Phase Equilibria|volume=2|issue=2|year=1978|pages=91–99|issn=0378-3812|doi=10.1016/0378-3812(78)85002-X}}</ref> मॉडल एक तथाकथित लैटिस मॉडल है और अणु सतहों के परस्पर क्रिया के पहले क्रम के अनुमान से लिया गया है। हालांकि, मॉडल अपने दो-[[समाधान (रसायन विज्ञान)|तरल (रसायन विज्ञान)]] दृष्टिकोण के कारण पूरी तरह से ऊष्मप्रवैगिकी रूप से संगत नहीं है।<ref name=":1" /> इस दृष्टिकोण में एक केंद्रीय अणु के आसपास की स्थानीय सांद्रता को दूसरे प्रकार के अणु के आसपास की स्थानीय संरचना से स्वतंत्र माना जाता है। | [[File:UNIQUACRegressionChloroformMethanol.png|thumb|गतिविधि गुणांकों का यूनिकैक [[प्रतिगमन विश्लेषण]] ([[ क्लोरोफार्म ]]/[[मेथनॉल]] मिश्रण)]][[सांख्यिकीय ऊष्मप्रवैगिकी]] में, '''यूनिकैक''' ('''सार्वभौमिक अर्ध-रासायनिक की प्रतिकृति''') एक [[गतिविधि गुणांक]] मॉडल है जिसका उपयोग [[चरण संतुलन|प्रावस्था संतुलन]] के विवरण में किया जाता है।<ref name="AbramsPrausnitz1975">{{cite journal|last1=Abrams|first1=Denis S.|last2=Prausnitz|first2=John M.|title=Statistical thermodynamics of liquid mixtures: A new expression for the excess Gibbs energy of partly or completely miscible systems|journal=AIChE Journal|volume=21|issue=1|year=1975|pages=116–128|issn=0001-1541|doi=10.1002/aic.690210115}}</ref><ref name=":1">{{cite journal|last1=Maurer|first1=G.|last2=Prausnitz|first2=J.M.|title=अद्वितीय समीकरण की व्युत्पत्ति और विस्तार पर|journal=Fluid Phase Equilibria|volume=2|issue=2|year=1978|pages=91–99|issn=0378-3812|doi=10.1016/0378-3812(78)85002-X}}</ref> मॉडल एक तथाकथित लैटिस मॉडल है और अणु सतहों के परस्पर क्रिया के पहले क्रम के अनुमान से लिया गया है। हालांकि, मॉडल अपने दो-[[समाधान (रसायन विज्ञान)|तरल (रसायन विज्ञान)]] दृष्टिकोण के कारण पूरी तरह से ऊष्मप्रवैगिकी रूप से संगत नहीं है।<ref name=":1" /> इस दृष्टिकोण में एक केंद्रीय अणु के आसपास की स्थानीय सांद्रता को दूसरे प्रकार के अणु के आसपास की स्थानीय संरचना से स्वतंत्र माना जाता है। | ||
यूनिकैक मॉडल को दूसरी पीढ़ी का गतिविधि गुणांक माना जा सकता है क्योंकि [[गिब्स ऊर्जा]] की अधिकता के लिए इसकी अभिव्यक्ति में [[तापीय धारिता]] शब्द के अतिरिक्त एक [[ एन्ट्रापी |एन्ट्रापी]] शब्द भी सम्मिलित है। पहले के गतिविधि गुणांक मॉडल जैसे कि विल्सन समीकरण और [[गैर-यादृच्छिक दो-तरल मॉडल]] (एनआरटीएल मॉडल) में केवल एन्थैल्पी शब्द होते हैं। | यूनिकैक मॉडल को दूसरी पीढ़ी का गतिविधि गुणांक माना जा सकता है क्योंकि [[गिब्स ऊर्जा]] की अधिकता के लिए इसकी अभिव्यक्ति में [[तापीय धारिता]] शब्द के अतिरिक्त एक [[ एन्ट्रापी |एन्ट्रापी]] शब्द भी सम्मिलित है। पहले के गतिविधि गुणांक मॉडल जैसे कि विल्सन समीकरण और [[गैर-यादृच्छिक दो-तरल मॉडल]] (एनआरटीएल मॉडल) में केवल एन्थैल्पी शब्द होते हैं। | ||
आज यूनिकैक मॉडल प्रायः चरण संतुलन (अर्थात तरल-ठोस, तरल-तरल या वाष्प-तरल संतुलन) के विवरण में प्रयुक्त होता है। यूनिकैक मॉडल समूह योगदान पद्धति [[UNIFAC|यूनिकैक कार्यात्मक-समूह गतिविधि गुणांक]] के विकास के आधार के रूप में भी कार्य करता है,<ref name=":0">{{cite journal|last1=Fredenslund|first1=Aage|last2=Jones|first2=Russell L.|last3=Prausnitz|first3=John M.|title=गैर-आदर्श तरल मिश्रण में गतिविधि गुणांकों का समूह-योगदान अनुमान|journal=AIChE Journal|volume=21|issue=6|year=1975|pages=1086–1099|issn=0001-1541|doi=10.1002/aic.690210607}}</ref> जहां अणुओं को [[कार्यात्मक समूह|कार्यात्मक समूहो]] में विभाजित किया जाता है। वास्तव में, यूनिकैक अणुओं के मिश्रण के लिए यूनिकैक कार्यात्मक-समूह गतिविधि गुणांक के समान है, जो उप-विभाजित नहीं हैं; उदाहरण द्वि-आधारी पद्धत्ति जल-मेथनॉल | आज यूनिकैक मॉडल प्रायः चरण संतुलन (अर्थात तरल-ठोस, तरल-तरल या वाष्प-तरल संतुलन) के विवरण में प्रयुक्त होता है। यूनिकैक मॉडल समूह योगदान पद्धति [[UNIFAC|यूनिकैक कार्यात्मक-समूह गतिविधि गुणांक]] के विकास के आधार के रूप में भी कार्य करता है,<ref name=":0">{{cite journal|last1=Fredenslund|first1=Aage|last2=Jones|first2=Russell L.|last3=Prausnitz|first3=John M.|title=गैर-आदर्श तरल मिश्रण में गतिविधि गुणांकों का समूह-योगदान अनुमान|journal=AIChE Journal|volume=21|issue=6|year=1975|pages=1086–1099|issn=0001-1541|doi=10.1002/aic.690210607}}</ref> जहां अणुओं को [[कार्यात्मक समूह|कार्यात्मक समूहो]] में विभाजित किया जाता है। वास्तव में, यूनिकैक अणुओं के मिश्रण के लिए यूनिकैक कार्यात्मक-समूह गतिविधि गुणांक के समान है, जो उप-विभाजित नहीं हैं; उदाहरण द्वि-आधारी पद्धत्ति जल-मेथनॉल, मेथनॉल-एक्रिओनाइट्राइल और फॉर्मलडिहाइड-डीएमएफ उप-विभाजित नहीं होते है। | ||
यूनिकैक का एक अधिक ऊष्मप्रवैगिकी रूप से सुसंगत रूप हाल ही के [[COSMOSPACE|कॉस्मो-सतह-युग्म गतिविधि गुणांक समीकरण]] और समकक्ष जीईक्यूएसी मॉडल द्वारा दिया गया है।<ref name="EgnerGaube1997">{{cite journal|last1=Egner|first1=K.|last2=Gaube|first2=J.|last3=Pfennig|first3=A.|title=GEQUAC, संबद्ध और गैर-सहयोगी तरल मिश्रण के एक साथ वर्णन के लिए एक अतिरिक्त गिब्स ऊर्जा मॉडल|journal=Berichte der Bunsengesellschaft für Physikalische Chemie|volume=101|issue=2|year=1997|pages=209–218|issn=0005-9021|doi=10.1002/bbpc.19971010208}}</ref> | यूनिकैक का एक अधिक ऊष्मप्रवैगिकी रूप से सुसंगत रूप हाल ही के [[COSMOSPACE|कॉस्मो-सतह-युग्म गतिविधि गुणांक समीकरण]] और समकक्ष जीईक्यूएसी मॉडल द्वारा दिया गया है।<ref name="EgnerGaube1997">{{cite journal|last1=Egner|first1=K.|last2=Gaube|first2=J.|last3=Pfennig|first3=A.|title=GEQUAC, संबद्ध और गैर-सहयोगी तरल मिश्रण के एक साथ वर्णन के लिए एक अतिरिक्त गिब्स ऊर्जा मॉडल|journal=Berichte der Bunsengesellschaft für Physikalische Chemie|volume=101|issue=2|year=1997|pages=209–218|issn=0005-9021|doi=10.1002/bbpc.19971010208}}</ref> | ||
| Line 29: | Line 29: | ||
:<math>\ln \gamma_i^C = (1 - V_i + \ln V_i) - \frac{z}{2} q_i \left( 1 - \frac{V_i}{F_i} + | :<math>\ln \gamma_i^C = (1 - V_i + \ln V_i) - \frac{z}{2} q_i \left( 1 - \frac{V_i}{F_i} + | ||
\ln \frac{V_i}{F_i}\right)</math> | \ln \frac{V_i}{F_i}\right)</math> | ||
प्रति मिश्रण मोल अंश के आयतन अंश के साथ | प्रति मिश्रण मोल अंश के आयतन अंश के साथ V<sub>i,</sub> i<sup>वें</sup> घटक के लिए द्वारा दिया गया: | ||
:<math>V_i = \frac{r_i}{\sum_j x_j r_j}</math> | :<math>V_i = \frac{r_i}{\sum_j x_j r_j}</math> | ||
i<sup>वे</sup> घटक के लिए सतह क्षेत्र अंश प्रति मिश्रण मोलीय अंश | i<sup>वे</sup> घटक के लिए सतह क्षेत्र अंश प्रति मिश्रण मोलीय अंश F<sub>i</sub>, के द्वारा दिया गया है: | ||
:<math>F_i = \frac{ q_i}{\sum_j x_j q_j}</math> | :<math>F_i = \frac{ q_i}{\sum_j x_j q_j}</math> | ||
सांयोगिक पद के दक्षिण पथ की ओर पहले तीन पद फ्लोरी-हगिंस योगदान बनाते हैं, जबकि शेष पद, गुगेनहेम-स्टावरमैन संशोधन, इसे कम करते हैं क्योंकि संयोजक भाग को समष्टि में सभी दिशाओं में नहीं रखा जा सकता है। यह स्थानिक संशोधन फ्लोरी-हगिंस पद के परिणाम को लगभग 5% एक आदर्श समाधान की ओर ले जाता है। समन्वय संख्या | सांयोगिक पद के दक्षिण पथ की ओर पहले तीन पद फ्लोरी-हगिंस योगदान बनाते हैं, जबकि शेष पद, गुगेनहेम-स्टावरमैन संशोधन, इसे कम करते हैं क्योंकि संयोजक भाग को समष्टि में सभी दिशाओं में नहीं रखा जा सकता है। यह स्थानिक संशोधन फ्लोरी-हगिंस पद के परिणाम को लगभग 5% एक आदर्श समाधान की ओर ले जाता है। समन्वय संख्या z, अर्थात एक केंद्रीय अणु के आस-पास परस्पर क्रिया करने वाले अणुओं की संख्या, प्रायः 10 पर प्रतिस्थापित होती है। इसे एक औसत मान के रूप में माना जा सकता है जो घनीय (z = 6) और षट्कोणीय पैकिंग (z = 12) के बीच होता है। अणु जो गोले द्वारा सरलीकृत होते हैं। | ||
द्विआधारी मिश्रण के लिए अनंत तनुकरण के स्थिति में, संयोजी योगदान के लिए समीकरण कम हो जाते हैं: | द्विआधारी मिश्रण के लिए अनंत तनुकरण के स्थिति में, संयोजी योगदान के लिए समीकरण कम हो जाते हैं: | ||
Revision as of 07:59, 13 April 2023
सांख्यिकीय ऊष्मप्रवैगिकी में, यूनिकैक (सार्वभौमिक अर्ध-रासायनिक की प्रतिकृति) एक गतिविधि गुणांक मॉडल है जिसका उपयोग प्रावस्था संतुलन के विवरण में किया जाता है।[1][2] मॉडल एक तथाकथित लैटिस मॉडल है और अणु सतहों के परस्पर क्रिया के पहले क्रम के अनुमान से लिया गया है। हालांकि, मॉडल अपने दो-तरल (रसायन विज्ञान) दृष्टिकोण के कारण पूरी तरह से ऊष्मप्रवैगिकी रूप से संगत नहीं है।[2] इस दृष्टिकोण में एक केंद्रीय अणु के आसपास की स्थानीय सांद्रता को दूसरे प्रकार के अणु के आसपास की स्थानीय संरचना से स्वतंत्र माना जाता है।
यूनिकैक मॉडल को दूसरी पीढ़ी का गतिविधि गुणांक माना जा सकता है क्योंकि गिब्स ऊर्जा की अधिकता के लिए इसकी अभिव्यक्ति में तापीय धारिता शब्द के अतिरिक्त एक एन्ट्रापी शब्द भी सम्मिलित है। पहले के गतिविधि गुणांक मॉडल जैसे कि विल्सन समीकरण और गैर-यादृच्छिक दो-तरल मॉडल (एनआरटीएल मॉडल) में केवल एन्थैल्पी शब्द होते हैं।
आज यूनिकैक मॉडल प्रायः चरण संतुलन (अर्थात तरल-ठोस, तरल-तरल या वाष्प-तरल संतुलन) के विवरण में प्रयुक्त होता है। यूनिकैक मॉडल समूह योगदान पद्धति यूनिकैक कार्यात्मक-समूह गतिविधि गुणांक के विकास के आधार के रूप में भी कार्य करता है,[3] जहां अणुओं को कार्यात्मक समूहो में विभाजित किया जाता है। वास्तव में, यूनिकैक अणुओं के मिश्रण के लिए यूनिकैक कार्यात्मक-समूह गतिविधि गुणांक के समान है, जो उप-विभाजित नहीं हैं; उदाहरण द्वि-आधारी पद्धत्ति जल-मेथनॉल, मेथनॉल-एक्रिओनाइट्राइल और फॉर्मलडिहाइड-डीएमएफ उप-विभाजित नहीं होते है।
यूनिकैक का एक अधिक ऊष्मप्रवैगिकी रूप से सुसंगत रूप हाल ही के कॉस्मो-सतह-युग्म गतिविधि गुणांक समीकरण और समकक्ष जीईक्यूएसी मॉडल द्वारा दिया गया है।[4]
समीकरण
अधिकांश स्थानीय रचना मॉडल की तरह, यूनिकैक अतिरिक्त गिब्स मुक्त ऊर्जा को एक संयोजी और एक अवशिष्ट योगदान में विभाजित करता है:
iवें घटक के परिकलित गतिविधि गुणांक फिर इसी तरह विभाजित होते हैं:
पहला अणु आकार में अंतर के परिणामस्वरूप आदर्श विलेयता से विचलन को मापने वाला एक एंट्रोपिक शब्द है। बाद वाला एक एन्थैल्पिक[nb 1] संशोधन है जो मिश्रण पर विभिन्न अणुओं के बीच परस्पर क्रिया करने वाली शक्तियों में परिवर्तन के कारण होता है।
मिश्रित योगदान
सांयोगिक योगदान अणुओं के बीच आकार के अंतर के लिए संचित है और मिश्रण की एन्ट्रापी को प्रभावित करता है और यह लैटिस सिद्धांत पर आधारित है। स्टैवरमैन-गुगेनहाइम समीकरण का उपयोग सापेक्ष वान डेर वाल्स संस्करण ri और सतह क्षेत्र qi[nb 2] शुद्ध रसायनों का उपयोग करते हुए शुद्ध रासायनिक मापदंडों से इस पद को अनुमानित करने के लिए किया जाता है।:
अवकल करने से अतिरिक्त एन्ट्रॉपी γC प्राप्त होता है,
प्रति मिश्रण मोल अंश के आयतन अंश के साथ Vi, iवें घटक के लिए द्वारा दिया गया:
iवे घटक के लिए सतह क्षेत्र अंश प्रति मिश्रण मोलीय अंश Fi, के द्वारा दिया गया है:
सांयोगिक पद के दक्षिण पथ की ओर पहले तीन पद फ्लोरी-हगिंस योगदान बनाते हैं, जबकि शेष पद, गुगेनहेम-स्टावरमैन संशोधन, इसे कम करते हैं क्योंकि संयोजक भाग को समष्टि में सभी दिशाओं में नहीं रखा जा सकता है। यह स्थानिक संशोधन फ्लोरी-हगिंस पद के परिणाम को लगभग 5% एक आदर्श समाधान की ओर ले जाता है। समन्वय संख्या z, अर्थात एक केंद्रीय अणु के आस-पास परस्पर क्रिया करने वाले अणुओं की संख्या, प्रायः 10 पर प्रतिस्थापित होती है। इसे एक औसत मान के रूप में माना जा सकता है जो घनीय (z = 6) और षट्कोणीय पैकिंग (z = 12) के बीच होता है। अणु जो गोले द्वारा सरलीकृत होते हैं।
द्विआधारी मिश्रण के लिए अनंत तनुकरण के स्थिति में, संयोजी योगदान के लिए समीकरण कम हो जाते हैं: