वेसिकल (जीव विज्ञान और रसायन विज्ञान): Difference between revisions
No edit summary |
No edit summary |
||
| Line 45: | Line 45: | ||
घनत्व के आधार पर विभिन्न प्रकार के ईवी को भिन्न किया जा सकता है<ref name=vdPol2012/>{{rp|Table 1}} (ग्रेडिएंट [[अंतर केन्द्रापसारक]] द्वारा), आकार, या सतह मार्कर।<ref>{{cite journal | vauthors = Mateescu B, Kowal EJ, van Balkom BW, Bartel S, Bhattacharyya SN, Buzás EI, Buck AH, de Candia P, Chow FW, Das S, Driedonks TA, Fernández-Messina L, Haderk F, Hill AF, Jones JC, Van Keuren-Jensen KR, Lai CP, Lässer C, Liegro ID, Lunavat TR, Lorenowicz MJ, Maas SL, Mäger I, Mittelbrunn M, Momma S, Mukherjee K, Nawaz M, Pegtel DM, Pfaffl MW, Schiffelers RM, Tahara H, Théry C, Tosar JP, Wauben MH, Witwer KW, Nolte-'t Hoen EN | display-authors = 6 | title = बाह्य पुटिका आरएनए के कार्यात्मक विश्लेषण में बाधाएं और अवसर - एक आईएसईवी स्थिति पत्र| journal = Journal of Extracellular Vesicles | volume = 6 | issue = 1 | pages = 1286095 | date = 2017 | pmid = 28326170 | pmc = 5345583 | doi = 10.1080/20013078.2017.1286095 }}</ref> चूँकि , EV उपप्रकारों में अतिव्यापी आकार और घनत्व सीमाएँ होती हैं, और उपप्रकार-अद्वितीय मार्करों को सेल-बाय-सेल आधार पर स्थापित किया जाना चाहिए। इसलिए, बायोजेनेसिस मार्ग को इंगित करना मुश्किल है जिसने सेल छोड़ने के बाद विशेष ईवी को जन्म दिया।<ref name="MISEV2018" /> | घनत्व के आधार पर विभिन्न प्रकार के ईवी को भिन्न किया जा सकता है<ref name=vdPol2012/>{{rp|Table 1}} (ग्रेडिएंट [[अंतर केन्द्रापसारक]] द्वारा), आकार, या सतह मार्कर।<ref>{{cite journal | vauthors = Mateescu B, Kowal EJ, van Balkom BW, Bartel S, Bhattacharyya SN, Buzás EI, Buck AH, de Candia P, Chow FW, Das S, Driedonks TA, Fernández-Messina L, Haderk F, Hill AF, Jones JC, Van Keuren-Jensen KR, Lai CP, Lässer C, Liegro ID, Lunavat TR, Lorenowicz MJ, Maas SL, Mäger I, Mittelbrunn M, Momma S, Mukherjee K, Nawaz M, Pegtel DM, Pfaffl MW, Schiffelers RM, Tahara H, Théry C, Tosar JP, Wauben MH, Witwer KW, Nolte-'t Hoen EN | display-authors = 6 | title = बाह्य पुटिका आरएनए के कार्यात्मक विश्लेषण में बाधाएं और अवसर - एक आईएसईवी स्थिति पत्र| journal = Journal of Extracellular Vesicles | volume = 6 | issue = 1 | pages = 1286095 | date = 2017 | pmid = 28326170 | pmc = 5345583 | doi = 10.1080/20013078.2017.1286095 }}</ref> चूँकि , EV उपप्रकारों में अतिव्यापी आकार और घनत्व सीमाएँ होती हैं, और उपप्रकार-अद्वितीय मार्करों को सेल-बाय-सेल आधार पर स्थापित किया जाना चाहिए। इसलिए, बायोजेनेसिस मार्ग को इंगित करना मुश्किल है जिसने सेल छोड़ने के बाद विशेष ईवी को जन्म दिया।<ref name="MISEV2018" /> | ||
मनुष्यों में, अंतर्जात बाह्य पुटिका जमावट, अंतरकोशिकीय संकेतन और अपशिष्ट प्रबंधन में भूमिका निभाते हैं।<ref name=vdPol2012>{{cite journal | vauthors = van der Pol E, Böing AN, Harrison P, Sturk A, Nieuwland R | title = बाह्य पुटिकाओं का वर्गीकरण, कार्य और नैदानिक प्रासंगिकता| journal = Pharmacological Reviews | volume = 64 | issue = 3 | pages = 676–705 | date = July 2012 | pmid = 22722893 | doi = 10.1124/pr.112.005983 | s2cid = 7764903 }} Free full text</ref> वे कैंसर सहित अनेक बीमारियों में सम्मिलित पैथोफिजियोलॉजिकल प्रक्रियाओं में भी सम्मिलित हैं।<ref>{{cite journal | vauthors = Dhondt B, Rousseau Q, De Wever O, Hendrix A | title = मेटास्टेसिस में बाह्य पुटिका से जुड़े miRNAs का कार्य| journal = Cell and Tissue Research | volume = 365 | issue = 3 | pages = 621–41 | date = September 2016 | pmid = 27289232 | doi = 10.1007/s00441-016-2430-x | s2cid = 2746182 | hdl = 1854/LU-7250365 | url = https://figshare.com/articles/journal_contribution/Function_of_extracellular_vesicle-associated_miRNAs_in_metastasis/7067858 }}</ref> एक्स्ट्रासेलुलर वेसिकल्स ने इंटरसेलुलर संचार में उनकी भूमिका, | मनुष्यों में, अंतर्जात बाह्य पुटिका जमावट, अंतरकोशिकीय संकेतन और अपशिष्ट प्रबंधन में भूमिका निभाते हैं।<ref name=vdPol2012>{{cite journal | vauthors = van der Pol E, Böing AN, Harrison P, Sturk A, Nieuwland R | title = बाह्य पुटिकाओं का वर्गीकरण, कार्य और नैदानिक प्रासंगिकता| journal = Pharmacological Reviews | volume = 64 | issue = 3 | pages = 676–705 | date = July 2012 | pmid = 22722893 | doi = 10.1124/pr.112.005983 | s2cid = 7764903 }} Free full text</ref> वे कैंसर सहित अनेक बीमारियों में सम्मिलित पैथोफिजियोलॉजिकल प्रक्रियाओं में भी सम्मिलित हैं।<ref>{{cite journal | vauthors = Dhondt B, Rousseau Q, De Wever O, Hendrix A | title = मेटास्टेसिस में बाह्य पुटिका से जुड़े miRNAs का कार्य| journal = Cell and Tissue Research | volume = 365 | issue = 3 | pages = 621–41 | date = September 2016 | pmid = 27289232 | doi = 10.1007/s00441-016-2430-x | s2cid = 2746182 | hdl = 1854/LU-7250365 | url = https://figshare.com/articles/journal_contribution/Function_of_extracellular_vesicle-associated_miRNAs_in_metastasis/7067858 }}</ref> एक्स्ट्रासेलुलर वेसिकल्स ने इंटरसेलुलर संचार में उनकी भूमिका, सरलता से सुलभ शरीर के तरल पदार्थ में रिलीज और रिलीजिंग कोशिकाओं के लिए उनकी आणविक सामग्री के समानता के कारण बायोमार्कर खोज के संभावित स्रोत के रूप में रुचि बढ़ाई है।<ref>{{cite journal | vauthors = Dhondt B, Van Deun J, Vermaerke S, de Marco A, Lumen N, De Wever O, Hendrix A | title = Urinary extracellular vesicle biomarkers in urological cancers: From discovery towards clinical implementation | journal = The International Journal of Biochemistry & Cell Biology | volume = 99 | pages = 236–256 | date = June 2018 | pmid = 29654900 | doi = 10.1016/j.biocel.2018.04.009 | hdl = 1854/LU-8559155 | s2cid = 4876604 | url = https://figshare.com/articles/journal_contribution/Urinary_extracellular_vesicle_biomarkers_in_urological_cancers_From_discovery_towards_clinical_implementation/7067903 }}</ref> [[मेसेनकाइमल स्टेम सेल]] के बाह्य पुटिका | (मेसेनकाइमल) स्टेम सेल, जिसे [[स्टेम सेल स्रावी]] के रूप में भी जाना जाता है, पर शोध किया जा रहा है और चिकित्सीय उद्देश्यों के लिए लागू किया जा रहा है, मुख्य रूप से [[अपक्षयी रोग]], ऑटोइम्यून रोग | ऑटो-इम्यून और / या इम्यून-मध्यस्थ सूजन रोग रोग .<ref>{{cite journal | vauthors = Teixeira FG, Carvalho MM, Sousa N, Salgado AJ | title = Mesenchymal stem cells secretome: a new paradigm for central nervous system regeneration? | journal = Cellular and Molecular Life Sciences | volume = 70 | issue = 20 | pages = 3871–82 | date = October 2013 | pmid = 23456256 | doi = 10.1007/s00018-013-1290-8 | s2cid = 18640402 | hdl = 1822/25128 | hdl-access = free }}</ref> | ||
ग्राम-नेगेटिव बैक्टीरिया में, बाहरी झिल्ली को बंद करके ईवी का उत्पादन किया जाता है; चूँकि , ईवीएस ग्राम-पॉजिटिव बैक्टीरिया, माइकोबैक्टीरिया और कवक की मोटी कोशिका भित्ति से कैसे बचते हैं यह अभी भी अज्ञात है। इन ईवी में न्यूक्लिक एसिड, टॉक्सिन्स, लिपोप्रोटीन और एंजाइम सहित विभिन्न कार्गो होते हैं और माइक्रोबियल फिजियोलॉजी और रोगजनन में महत्वपूर्ण भूमिका होती है। होस्ट-पैथोजेन इंटरैक्शन में, ग्राम नकारात्मक बैक्टीरिया पुटिकाओं का उत्पादन करते हैं जो उपनिवेशीकरण आला स्थापित करने में भूमिका निभाते हैं, विषाणु कारकों को मेजबान कोशिकाओं में ले जाते हैं और प्रसारित करते हैं और मेजबान रक्षा और प्रतिक्रिया को संशोधित करते हैं।<ref name=Kuehn2005>{{cite journal | vauthors = Kuehn MJ, Kesty NC | title = बैक्टीरियल बाहरी झिल्ली पुटिका और मेजबान-रोगज़नक़ बातचीत| journal = Genes & Development | volume = 19 | issue = 22 | pages = 2645–55 | date = November 2005 | pmid = 16291643 | doi = 10.1101/gad.1299905 | doi-access = free }}</ref> | ग्राम-नेगेटिव बैक्टीरिया में, बाहरी झिल्ली को बंद करके ईवी का उत्पादन किया जाता है; चूँकि , ईवीएस ग्राम-पॉजिटिव बैक्टीरिया, माइकोबैक्टीरिया और कवक की मोटी कोशिका भित्ति से कैसे बचते हैं यह अभी भी अज्ञात है। इन ईवी में न्यूक्लिक एसिड, टॉक्सिन्स, लिपोप्रोटीन और एंजाइम सहित विभिन्न कार्गो होते हैं और माइक्रोबियल फिजियोलॉजी और रोगजनन में महत्वपूर्ण भूमिका होती है। होस्ट-पैथोजेन इंटरैक्शन में, ग्राम नकारात्मक बैक्टीरिया पुटिकाओं का उत्पादन करते हैं जो उपनिवेशीकरण आला स्थापित करने में भूमिका निभाते हैं, विषाणु कारकों को मेजबान कोशिकाओं में ले जाते हैं और प्रसारित करते हैं और मेजबान रक्षा और प्रतिक्रिया को संशोधित करते हैं।<ref name=Kuehn2005>{{cite journal | vauthors = Kuehn MJ, Kesty NC | title = बैक्टीरियल बाहरी झिल्ली पुटिका और मेजबान-रोगज़नक़ बातचीत| journal = Genes & Development | volume = 19 | issue = 22 | pages = 2645–55 | date = November 2005 | pmid = 16291643 | doi = 10.1101/gad.1299905 | doi-access = free }}</ref> | ||
महासागर [[साइनोबैक्टीरीया]] खुले समुद्र में प्रोटीन, डीएनए और आरएनए युक्त पुटिकाओं को लगातार छोड़ते पाए गए हैं। विविध जीवाणुओं से डीएनए ले जाने वाले वेसिकल्स तटीय और खुले समुद्र के समुद्री जल के नमूनों में प्रचुर मात्रा में हैं।<ref name=Biller2014>{{cite journal | vauthors = Biller SJ, Schubotz F, Roggensack SE, Thompson AW, Summons RE, Chisholm SW | title = समुद्री पारिस्थितिक तंत्र में जीवाणु पुटिकाएँ| journal = Science | volume = 343 | issue = 6167 | pages = 183–6 | date = January 2014 | pmid = 24408433 | doi = 10.1126/science.1243457 | s2cid = 206551356 | bibcode = 2014Sci...343..183B | hdl = 1721.1/84545 | hdl-access = free }}</ref> | महासागर [[साइनोबैक्टीरीया]] खुले समुद्र में प्रोटीन, डीएनए और आरएनए युक्त पुटिकाओं को लगातार छोड़ते पाए गए हैं। विविध जीवाणुओं से डीएनए ले जाने वाले वेसिकल्स तटीय और खुले समुद्र के समुद्री जल के नमूनों में प्रचुर मात्रा में हैं।<ref name=Biller2014>{{cite journal | vauthors = Biller SJ, Schubotz F, Roggensack SE, Thompson AW, Summons RE, Chisholm SW | title = समुद्री पारिस्थितिक तंत्र में जीवाणु पुटिकाएँ| journal = Science | volume = 343 | issue = 6167 | pages = 183–6 | date = January 2014 | pmid = 24408433 | doi = 10.1126/science.1243457 | s2cid = 206551356 | bibcode = 2014Sci...343..183B | hdl = 1721.1/84545 | hdl-access = free }}</ref> | ||
| Line 90: | Line 90: | ||
==== पृथक पुटिका ==== | ==== पृथक पुटिका ==== | ||
कोशिका की विभिन्न झिल्लियों की | कोशिका की विभिन्न झिल्लियों की परीक्षण करने के लिए झिल्ली पुटिकाओं का निर्माण विधि है। जीवित ऊतक को निलंबन (रसायन) में कुचलने के बाद, विभिन्न झिल्लियां छोटे बंद बुलबुले बनाती हैं। कुचली हुई कोशिकाओं के बड़े टुकड़ों को कम गति के सेंट्रीफ्यूगेशन द्वारा भिन्न किया जा सकता है और बाद में ज्ञात मूल ([[ plasmalemma ]], [[ tonoplast ]], आदि) के अंश को घनत्व प्रवणता में सटीक उच्च गति सेंट्रीफ्यूगेशन द्वारा भिन्न किया जा सकता है। [[आसमाटिक झटका]] का उपयोग करके, अस्थायी रूप से पुटिकाओं को खोलना (उन्हें आवश्यक समाधान के साथ भरना) संभव है और फिर फिर से सेंट्रीफ्यूगेट करें और भिन्न समाधान में पुन: निलंबित करें। [[वैलिनोमाइसिन]] जैसे आयनोफोरस को लागू करने से जीवित कोशिकाओं के अंदर के ग्रेडिएंट्स की तुलना में इलेक्ट्रोकेमिकल ग्रेडिएंट्स बन सकते हैं। | ||
Vesicles मुख्य रूप से दो प्रकार के शोधों में उपयोग किए जाते हैं: | Vesicles मुख्य रूप से दो प्रकार के शोधों में उपयोग किए जाते हैं: | ||
* झिल्ली रिसेप्टर्स को खोजने और बाद में भिन्न करने के लिए जो विशेष रूप से हार्मोन और अन्य महत्वपूर्ण पदार्थों को बांधते हैं।<ref>{{cite journal | vauthors = Sidhu VK, Vorhölter FJ, Niehaus K, Watt SA | title = पौधे के रोगजनक जीवाणु ज़ैंथोमोनस कैंपेस्ट्रिस पीवी से पृथक बाहरी झिल्ली पुटिका से जुड़े प्रोटीन का विश्लेषण। campestris| journal = BMC Microbiology | volume = 8 | pages = 87 | date = June 2008 | pmid = 18518965 | pmc = 2438364 | doi = 10.1186/1471-2180-8-87 }}</ref> | * झिल्ली रिसेप्टर्स को खोजने और बाद में भिन्न करने के लिए जो विशेष रूप से हार्मोन और अन्य महत्वपूर्ण पदार्थों को बांधते हैं।<ref>{{cite journal | vauthors = Sidhu VK, Vorhölter FJ, Niehaus K, Watt SA | title = पौधे के रोगजनक जीवाणु ज़ैंथोमोनस कैंपेस्ट्रिस पीवी से पृथक बाहरी झिल्ली पुटिका से जुड़े प्रोटीन का विश्लेषण। campestris| journal = BMC Microbiology | volume = 8 | pages = 87 | date = June 2008 | pmid = 18518965 | pmc = 2438364 | doi = 10.1186/1471-2180-8-87 }}</ref> | ||
*दिए गए प्रकार की झिल्ली के पार विभिन्न आयनों या अन्य पदार्थों के परिवहन की | *दिए गए प्रकार की झिल्ली के पार विभिन्न आयनों या अन्य पदार्थों के परिवहन की परीक्षण करना।<ref>{{cite journal |vauthors=Scherer GG, Martiny-Baron G |title=K+/H+ exchange transport in plantmembranevesicles is evidence for K+ transport |journal=Plant Science |volume=41 |issue=3 |pages=161–8 |year=1985 |doi=10.1016/0168-9452(85)90083-4 }}</ref> जबकि [[ पैच दबाना |पैच दबाना]] प्रौद्योगिकी के साथ परिवहन की अधिक सरलता से परीक्षण की जा सकती है, पुटिकाओं को उन वस्तुओं से भी भिन्न किया जा सकता है जिनके लिए पैच क्लैंप लागू नहीं होता है। | ||
===कृत्रिम वेसिकल्स=== | ===कृत्रिम वेसिकल्स=== | ||
{{See also|यूनिमेलर लिपोसोम | {{See also|यूनिमेलर लिपोसोम | ||
}} | }} | ||
कृत्रिम वेसिकल्स को उनके आकार के आधार पर तीन समूहों में वर्गीकृत किया गया है: 20–100 एनएम के आकार की सीमा के साथ छोटे यूनीमेलर लिपोसोम्स/वेसिकल्स (एसयूवी), 100–1000 एनएम के आकार की सीमा के साथ बड़े यूनीमेलर लिपोसोम्स/वेसिकल्स (एलयूवी) और विशाल यूनीमेलर लाइपोसोम/वेसिकल्स (जीयूवी) जिनका आकार 1–200 माइक्रोमीटर होता है।<ref>{{cite journal | vauthors = Walde P, Cosentino K, Engel H, Stano P | title = Giant vesicles: preparations and applications | journal = ChemBioChem | volume = 11 | issue = 7 | pages = 848–65 | date = May 2010 | pmid = 20336703 | doi = 10.1002/cbic.201000010 | s2cid = 30723166 }}</ref> जीवित कोशिकाओं में पाए जाने वाले ट्रैफिकिंग वेसिकल्स के समान आकार की छोटी पुटिकाएं प्रायः जैव रसायन और संबंधित क्षेत्रों में उपयोग की जाती हैं। ऐसे अध्ययनों के लिए, एक्सट्रूज़न या [[ sonication ]] द्वारा सजातीय फॉस्फोलिपिड पुटिका निलंबन तैयार किया जा सकता है,<ref>{{cite journal | vauthors = Barenholz Y, Gibbes D, Litman BJ, Goll J, Thompson TE, Carlson RD | title = सजातीय फॉस्फोलिपिड पुटिकाओं की तैयारी के लिए एक सरल विधि| journal = Biochemistry | volume = 16 | issue = 12 | pages = 2806–10 | date = June 1977 | pmid = 889789 | doi = 10.1021/bi00631a035 }}</ref> या जलीय बफर समाधान में फॉस्फोलिपिड समाधान के तेजी से इंजेक्शन द्वारा।<ref>{{cite journal | vauthors = Batzri S, Korn ED | title = सिंगल बाइलेयर लिपोसोम बिना सोनिकेशन के तैयार किए गए| journal = Biochimica et Biophysica Acta (BBA) - Biomembranes | volume = 298 | issue = 4 | pages = 1015–9 | date = April 1973 | pmid = 4738145 | doi = 10.1016/0005-2736(73)90408-2 }}</ref> इस तरह, विभिन्न फॉस्फोलिपिड संरचना के साथ-साथ विभिन्न आकार के पुटिकाओं के जलीय पुटिका समाधान तैयार किए जा सकते हैं। कोशिका झिल्लियों की नकल करने के लिए कोशिका जीव विज्ञान में इन विट्रो अध्ययनों के लिए GUVs जैसे बड़े कृत्रिम रूप से बने पुटिकाओं का उपयोग किया जाता है। पारंपरिक प्रतिदीप्ति प्रकाश माइक्रोस्कोपी का उपयोग करके इन पुटिकाओं का अध्ययन किया जाना काफी बड़ा है। इस तरह के पुटिकाओं के अंदर प्रोटीन समाधान जैसे जैविक अभिकारकों को समाहित करने के लिए अनेक तरह के तरीके उपस्थित हैं, जो GUVs को सेल-जैसे मॉडल झिल्ली वातावरण में सेल फ़ंक्शंस के इन विट्रो रिक्रिएशन (और जांच) के लिए आदर्श प्रणाली बनाते हैं।<ref>{{cite journal | vauthors = Litschel T, Schwille P | title = जायंट यूनीमेलर वेसिकल्स के अंदर प्रोटीन का पुनर्गठन| journal = Annual Review of Biophysics | date = March 2021 | volume = 50 | pages = 525–548 | pmid = 33667121 | doi = 10.1146/annurev-biophys-100620-114132 | s2cid = 232131463 }}</ref> इन विधियों में माइक्रोफ्लुइडिक विधियाँ सम्मिलित हैं, जो लगातार आकार वाले पुटिकाओं के उच्च-उपज उत्पादन की अनुमति देती हैं।<ref>{{cite journal | vauthors = Sato Y, Takinoue M | title = माइक्रोफ्लुइडिक्स टेक्नोलॉजीज द्वारा प्रवर्तित कृत्रिम कोशिका जैसी संरचनाओं का निर्माण| journal = Micromachines | volume = 10 | issue = 4 | pages = 216 | date = March 2019 | pmid = 30934758 | pmc = 6523379 | doi = 10.3390/mi10040216 | doi-access = free }}</ref> | कृत्रिम वेसिकल्स को उनके आकार के आधार पर तीन समूहों में वर्गीकृत किया गया है: 20–100 एनएम के आकार की सीमा के साथ छोटे यूनीमेलर लिपोसोम्स/वेसिकल्स (एसयूवी), 100–1000 एनएम के आकार की सीमा के साथ बड़े यूनीमेलर लिपोसोम्स/वेसिकल्स (एलयूवी) और विशाल यूनीमेलर लाइपोसोम/वेसिकल्स (जीयूवी) जिनका आकार 1–200 माइक्रोमीटर होता है।<ref>{{cite journal | vauthors = Walde P, Cosentino K, Engel H, Stano P | title = Giant vesicles: preparations and applications | journal = ChemBioChem | volume = 11 | issue = 7 | pages = 848–65 | date = May 2010 | pmid = 20336703 | doi = 10.1002/cbic.201000010 | s2cid = 30723166 }}</ref> जीवित कोशिकाओं में पाए जाने वाले ट्रैफिकिंग वेसिकल्स के समान आकार की छोटी पुटिकाएं प्रायः जैव रसायन और संबंधित क्षेत्रों में उपयोग की जाती हैं। ऐसे अध्ययनों के लिए, एक्सट्रूज़न या[[ sonication ]]द्वारा सजातीय फॉस्फोलिपिड पुटिका निलंबन तैयार किया जा सकता है,<ref>{{cite journal | vauthors = Barenholz Y, Gibbes D, Litman BJ, Goll J, Thompson TE, Carlson RD | title = सजातीय फॉस्फोलिपिड पुटिकाओं की तैयारी के लिए एक सरल विधि| journal = Biochemistry | volume = 16 | issue = 12 | pages = 2806–10 | date = June 1977 | pmid = 889789 | doi = 10.1021/bi00631a035 }}</ref> या जलीय बफर समाधान में फॉस्फोलिपिड समाधान के तेजी से इंजेक्शन द्वारा।<ref>{{cite journal | vauthors = Batzri S, Korn ED | title = सिंगल बाइलेयर लिपोसोम बिना सोनिकेशन के तैयार किए गए| journal = Biochimica et Biophysica Acta (BBA) - Biomembranes | volume = 298 | issue = 4 | pages = 1015–9 | date = April 1973 | pmid = 4738145 | doi = 10.1016/0005-2736(73)90408-2 }}</ref> इस तरह, विभिन्न फॉस्फोलिपिड संरचना के साथ-साथ विभिन्न आकार के पुटिकाओं के जलीय पुटिका समाधान तैयार किए जा सकते हैं। कोशिका झिल्लियों की नकल करने के लिए कोशिका जीव विज्ञान में इन विट्रो अध्ययनों के लिए GUVs जैसे बड़े कृत्रिम रूप से बने पुटिकाओं का उपयोग किया जाता है। पारंपरिक प्रतिदीप्ति प्रकाश माइक्रोस्कोपी का उपयोग करके इन पुटिकाओं का अध्ययन किया जाना काफी बड़ा है। इस तरह के पुटिकाओं के अंदर प्रोटीन समाधान जैसे जैविक अभिकारकों को समाहित करने के लिए अनेक तरह के तरीके उपस्थित हैं, जो GUVs को सेल-जैसे मॉडल झिल्ली वातावरण में सेल फ़ंक्शंस के इन विट्रो रिक्रिएशन (और जांच) के लिए आदर्श प्रणाली बनाते हैं।<ref>{{cite journal | vauthors = Litschel T, Schwille P | title = जायंट यूनीमेलर वेसिकल्स के अंदर प्रोटीन का पुनर्गठन| journal = Annual Review of Biophysics | date = March 2021 | volume = 50 | pages = 525–548 | pmid = 33667121 | doi = 10.1146/annurev-biophys-100620-114132 | s2cid = 232131463 }}</ref> इन विधियों में माइक्रोफ्लुइडिक विधियाँ सम्मिलित हैं, जो लगातार आकार वाले पुटिकाओं के उच्च-उपज उत्पादन की अनुमति देती हैं।<ref>{{cite journal | vauthors = Sato Y, Takinoue M | title = माइक्रोफ्लुइडिक्स टेक्नोलॉजीज द्वारा प्रवर्तित कृत्रिम कोशिका जैसी संरचनाओं का निर्माण| journal = Micromachines | volume = 10 | issue = 4 | pages = 216 | date = March 2019 | pmid = 30934758 | pmc = 6523379 | doi = 10.3390/mi10040216 | doi-access = free }}</ref> | ||
== यह भी देखें == | == यह भी देखें == | ||
{{Div col|colwidth=30em}} | {{Div col|colwidth=30em}} | ||
Revision as of 16:16, 10 March 2023
कोशिका जीव विज्ञान में, वेसिकल संरचना intracellular या बाह्यकोशिकीय कोशिका (जीव विज्ञान) है, जिसमें लिपिड बिलेयर द्वारा संलग्न तरल या साइटोप्लाज्म होता है। स्राव (एक्सोसाइटोसिस), अपटेक (एंडोसाइटोसिस) और प्लाज़्मा झिल्ली के अंदर सामग्रियों के परिवहन की प्रक्रियाओं के समय वेसिकल्स स्वाभाविक रूप से बनते हैं। वैकल्पिक रूप से, उन्हें कृत्रिम रूप से तैयार किया जा सकता है, जिस स्थिति में उन्हें लाइपोसोम कहा जाता है (लाइसोसोम के साथ भ्रमित नहीं होना)। यदि केवल फ़ॉस्फ़ोलिपिड बाइलेयर है, तो पुटिकाओं को "एकतरफा लिपोसोम" कहा जाता है; अन्यथा उन्हें 'मल्टीमेलर लिपोसोम्स' कहा जाता है।[1] पुटिका को घेरने वाली झिल्ली भी लैमेलर चरण है, जो प्लाज्मा झिल्ली के समान है, और इंट्रासेल्युलर वेसिकल कोशिका के बाहर अपनी सामग्री को छोड़ने के लिए प्लाज्मा झिल्ली के साथ फ्यूज कर सकते हैं। पुटिकाएं कोशिका के अंदर अन्य जीवों के साथ भी मिल सकती हैं। कोशिका से मुक्त वेसिकल को बाह्य पुटिका के रूप में जाना जाता है।
पुटिकाएं अनेक प्रकार के कार्य करती हैं। क्योंकि यह साइटोसोल से भिन्न होता है, पुटिका के अंदर को साइटोसोलिक वातावरण से भिन्न बनाया जा सकता है। इस कारण से, कोशिकीय पदार्थों को व्यवस्थित करने के लिए पुटिका कोशिका द्वारा उपयोग किया जाने वाला बुनियादी उपकरण है। पुटिकाएं चयापचय, परिवहन, उछाल नियंत्रण में सम्मिलित होती हैं,[2] और भोजन और एंजाइमों का अस्थायी भंडारण। वे रासायनिक प्रतिक्रिया कक्षों के रूप में भी कार्य कर सकते हैं।
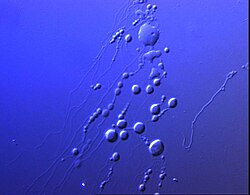
Closed structure formed by amphiphilic molecules that contains solvent (usually water).[3]
फिजियोलॉजी या मेडिसिन में 2013 का नोबेल पुरस्कार जेम्स रोथमैन, रैंडी शेकमैन और थॉमस सुधोफ द्वारा उनकी भूमिका के लिए साझा किया गया था (पहले के शोध पर निर्माण, उनमें से कुछ उनके आकाओं द्वारा) कोशिका पुटिकाओं के मेकअप और कार्य, विशेष रूप से यीस्ट में और में मनुष्य, प्रत्येक पुटिका के हिस्सों और उन्हें कैसे इकट्ठा किया जाता है, के बारे में जानकारी सहित। वेसिकल डिसफंक्शन को अल्जाइमर रोग, मधुमेह, मिर्गी के कुछ कठिन-से-इलाज वाले मामलों, कुछ कैंसर और प्रतिरक्षा संबंधी विकारों और कुछ न्यूरोवास्कुलर स्थितियों में योगदान करने के लिए माना जाता है।[4][5]
वेसिकुलर संरचनाओं के प्रकार
रिक्तिकाएं
रिक्तिकाएं कोशिकीय अंग हैं जिनमें ज्यादातर पानी होता है।
- पादप कोशिकाओं में कोशिका के केंद्र में बड़ी केंद्रीय रसधानी होती है जिसका उपयोग osmoregulation और पादप पोषण भंडारण के लिए किया जाता है।
- संकुचनशील रिक्तिकाएँ कुछ प्रोटिस्टों में पाई जाती हैं, विशेष रूप से फाइलमसिलिओफोरा में। ये रिक्तिकाएँ साइटोप्लाज्म से पानी लेती हैं और आसमाटिक दबाव के कारण फटने से बचने के लिए इसे कोशिका से बाहर निकालती हैं।
लाइसोसोम
- लाइसोसोम कोशिकीय पाचन में सम्मिलित होते हैं। एंडोसाइटोसिस नामक प्रक्रिया द्वारा भोजन को कोशिका के बाहर से भोजन रिक्तिका में ले जाया जा सकता है। ये खाद्य रिक्तिकाएँ लाइसोसोम के साथ मिल जाती हैं जो घटकों को तोड़ देती हैं जिससे कि उन्हें कोशिका में उपयोग किया जा सके। कोशिकीय खाने के इस रूप को phagocytosis कहा जाता है।
- लाइसोसोम का उपयोगभोजी नामक प्रक्रिया में दोषपूर्ण या क्षतिग्रस्त अंगों को नष्ट करने के लिए भी किया जाता है। वे क्षतिग्रस्त ऑर्गेनेल की झिल्ली के साथ फ्यूज हो जाते हैं, इसे पचाते हैं।
परिवहन वेसिकल्स
- परिवहन पुटिकाएँ कोशिका के अंदर के स्थानों के मध्य अणुओं को स्थानांतरित कर सकती हैं, उदाहरण के लिए, किसी न किसीअन्तः प्रदव्ययी जलिका से गोल्गी उपकरण तक प्रोटीन।
- झिल्ली-बद्ध और स्रावित प्रोटीन रफ अन्तर्द्रव्यी जालिका में पाए जाने वाले राइबोसोम पर बनते हैं। इनमें से अधिकांश प्रोटीन अपने अंतिम गंतव्य पर जाने से पहले गोल्गी तंत्र में परिपक्व होते हैं जो लाइसोसोम, पेरोक्सीसोम्स या कोशिका के बाहर हो सकते हैं। ये प्रोटीन परिवहन पुटिकाओं के अंदर कोशिका के अंदर यात्रा करते हैं।
स्रावी पुटिका
स्रावी पुटिकाओं में ऐसे पदार्थ होते हैं जिन्हें कोशिका से बाहर निकालना होता है। कोशिकाओं के पदार्थों को बाहर निकालने के अनेक कारण होते हैं।
एक कारण कचरे का निपटान करना है। एक अन्य कारण कोशिका के कार्य से जुड़ा है। बड़े जीव के भीतर, कुछ कोशिकाएं कुछ रसायनों का उत्पादन करने के लिए विशिष्ट होती हैं। इन रसायनों को स्रावी पुटिकाओं में संग्रहित किया जाता है और आवश्यकता पड़ने पर छोड़ा जाता है।
प्रकार
- सिनैप्टिक पुटिका ्स न्यूरॉन्स में प्रीसानेप्टिक टर्मिनलों पर स्थित होते हैं और स्नायुसंचारी स्टोर करते हैं। जब संकेत अक्षतंतु के नीचे आता है, तो अन्तर्ग्रथनी पुटिकाएं कोशिका झिल्ली के साथ मिलकर न्यूरोट्रांसमीटर को छोड़ती हैं जिससे कि अगले तंत्रिका कोशिका पर रिसेप्टर (जैव रसायन) अणुओं द्वारा इसका पता लगाया जा सके।
- जानवरों में अंतःस्रावी तंत्र रक्तधारा में हार्मोन छोड़ते हैं। ये हार्मोन स्रावी पुटिकाओं के अंदर जमा होते हैं। अच्छा उदाहरण अग्न्याशय में लैंगरहैंस के आइलेट्स में पाया जाने वाला अंतःस्रावी ऊतक है। इस ऊतक (जीव विज्ञान) में अनेक कोशिका प्रकार होते हैं जो परिभाषित होते हैं कि वे किस हार्मोन का उत्पादन करते हैं।
- स्रावी पुटिकाओं में वे एंजाइम होते हैं जिनका उपयोग पादप कोशिका, protist, कवक, जीवाणु और आर्किया कोशिकाओं की कोशिका भित्ति के साथ-साथ पशु कोशिकाओं के बाह्य मैट्रिक्स को बनाने के लिए किया जाता है।
- बैक्टीरिया, आर्किया, कवक और परजीवी विविध लेकिन विशेष जहरीले यौगिकों और जैव रासायनिक संकेत अणुओं से युक्त झिल्ली पुटिका (एमवी) छोड़ते हैं, जो सूक्ष्म जीव के पक्ष में प्रक्रिया शुरू करने के लिए लक्षित कोशिकाओं तक ले जाए जाते हैं, जिसमें मेजबान कोशिकाओं पर आक्रमण और प्रतिस्पर्धी की हत्या सम्मिलित है। ही आला में रोगाणुओं।[6]
बाह्य कोशिकीय
एक्स्ट्रासेलुलर वेसिकल्स (ईवीएस) जीवन के सभी डोमेन द्वारा निर्मित लिपिड बाइलेयर-सीमांकित कण हैं, जिनमें जटिल यूकेरियोट्स, ग्राम-नकारात्मक और ग्राम-पॉजिटिव बैक्टीरिया, माइकोबैक्टीरिया और कवक दोनों सम्मिलित हैं।[7][8]
प्रकार
- माइक्रोवेसिकल्स|एक्टोसोम/माइक्रोवेसिकल्स प्लाज्मा झिल्ली से सीधे बहाए जाते हैं और आकार में लगभग 30 नैनोमीटर से व्यास में माइक्रोन से बड़े हो सकते हैं[9]: Table 1 ). इनमें बूँद (कोशिका जीव विज्ञान) जैसे बड़े कण सम्मिलित हो सकते हैं # मरने वाली कोशिकाओं द्वारा जारी एपोप्टोटिक कार्य,[10][9]: Table 1 नेमाटोड न्यूरॉन्स द्वारा जारी कुछ कैंसर कोशिकाओं, या exophers द्वारा जारी बड़े ओंकोसोम[11] और माउस कार्डियोमायोसाइट्स।
- एक्सोसोम (पुटिका) एस: एंडोसाइटिक उत्पत्ति (30-100 एनएम व्यास) के झिल्लीदार पुटिका।[9]: Table 1
घनत्व के आधार पर विभिन्न प्रकार के ईवी को भिन्न किया जा सकता है[9]: Table 1 (ग्रेडिएंट अंतर केन्द्रापसारक द्वारा), आकार, या सतह मार्कर।[12] चूँकि , EV उपप्रकारों में अतिव्यापी आकार और घनत्व सीमाएँ होती हैं, और उपप्रकार-अद्वितीय मार्करों को सेल-बाय-सेल आधार पर स्थापित किया जाना चाहिए। इसलिए, बायोजेनेसिस मार्ग को इंगित करना मुश्किल है जिसने सेल छोड़ने के बाद विशेष ईवी को जन्म दिया।[8]
मनुष्यों में, अंतर्जात बाह्य पुटिका जमावट, अंतरकोशिकीय संकेतन और अपशिष्ट प्रबंधन में भूमिका निभाते हैं।[9] वे कैंसर सहित अनेक बीमारियों में सम्मिलित पैथोफिजियोलॉजिकल प्रक्रियाओं में भी सम्मिलित हैं।[13] एक्स्ट्रासेलुलर वेसिकल्स ने इंटरसेलुलर संचार में उनकी भूमिका, सरलता से सुलभ शरीर के तरल पदार्थ में रिलीज और रिलीजिंग कोशिकाओं के लिए उनकी आणविक सामग्री के समानता के कारण बायोमार्कर खोज के संभावित स्रोत के रूप में रुचि बढ़ाई है।[14] मेसेनकाइमल स्टेम सेल के बाह्य पुटिका | (मेसेनकाइमल) स्टेम सेल, जिसे स्टेम सेल स्रावी के रूप में भी जाना जाता है, पर शोध किया जा रहा है और चिकित्सीय उद्देश्यों के लिए लागू किया जा रहा है, मुख्य रूप से अपक्षयी रोग, ऑटोइम्यून रोग | ऑटो-इम्यून और / या इम्यून-मध्यस्थ सूजन रोग रोग .[15] ग्राम-नेगेटिव बैक्टीरिया में, बाहरी झिल्ली को बंद करके ईवी का उत्पादन किया जाता है; चूँकि , ईवीएस ग्राम-पॉजिटिव बैक्टीरिया, माइकोबैक्टीरिया और कवक की मोटी कोशिका भित्ति से कैसे बचते हैं यह अभी भी अज्ञात है। इन ईवी में न्यूक्लिक एसिड, टॉक्सिन्स, लिपोप्रोटीन और एंजाइम सहित विभिन्न कार्गो होते हैं और माइक्रोबियल फिजियोलॉजी और रोगजनन में महत्वपूर्ण भूमिका होती है। होस्ट-पैथोजेन इंटरैक्शन में, ग्राम नकारात्मक बैक्टीरिया पुटिकाओं का उत्पादन करते हैं जो उपनिवेशीकरण आला स्थापित करने में भूमिका निभाते हैं, विषाणु कारकों को मेजबान कोशिकाओं में ले जाते हैं और प्रसारित करते हैं और मेजबान रक्षा और प्रतिक्रिया को संशोधित करते हैं।[16] महासागर साइनोबैक्टीरीया खुले समुद्र में प्रोटीन, डीएनए और आरएनए युक्त पुटिकाओं को लगातार छोड़ते पाए गए हैं। विविध जीवाणुओं से डीएनए ले जाने वाले वेसिकल्स तटीय और खुले समुद्र के समुद्री जल के नमूनों में प्रचुर मात्रा में हैं।[17]
अन्य प्रकार
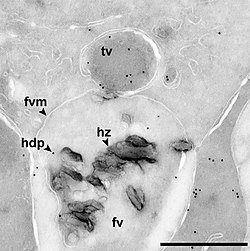
गैस पुटिकाओं का उपयोग आर्किया, बैक्टीरिया और प्लवक सूक्ष्मजीवों द्वारा किया जाता है, संभवतः गैस सामग्री को विनियमित करके ऊर्ध्वाधर प्रवास को नियंत्रित करने के लिए और इस तरह उछाल, या संभवतः अधिकतम सौर प्रकाश संचयन के लिए सेल की स्थिति के लिए। ये पुटिकाएं सामान्यतः नींबू के आकार की या बेलनाकार ट्यूब होती हैं जो प्रोटीन से बनी होती हैं;[18] उनका व्यास पुटिका की ताकत को निर्धारित करता है जिसमें बड़े कमजोर होते हैं। पुटिका का व्यास भी इसकी मात्रा को प्रभावित करता है और यह कितनी कुशलता से उछाल प्रदान कर सकता है। सायनोबैक्टीरिया में प्राकृतिक चयन ने वेसिकल्स बनाने का काम किया है जो संरचनात्मक रूप से स्थिर होते हुए भी अधिकतम व्यास पर हैं। प्रोटीन त्वचा गैसों के लिए पारगम्य है, लेकिन पानी नहीं, पुटिकाओं को बाढ़ से बचाए रखता है।[2]
एक्स्ट्रासेलुलर मैट्रिक्स वेसिकल्स एक्स्ट्रासेलुलर स्पेस या मैट्रिक्स के अंदर स्थित होते हैं। इलेक्ट्रॉन माइक्रोस्कोपी का उपयोग करते हुए उन्हें 1967 में एच. क्लार्क एंडरसन द्वारा स्वतंत्र रूप से खोजा गया था[19] और एरमानो बोनुची।[20] ये कोशिका-व्युत्पन्न पुटिका हड्डी, उपास्थि और दंतधातु सहित विभिन्न प्रकार के ऊतकों में मैट्रिक्स के जैवखनिजीकरण को आरंभ करने के लिए विशिष्ट हैं। सामान्य कड़ा हो जाना के दौरान, कोशिकाओं में कैल्शियम और फॉस्फेट आयनों का बड़ा प्रवाह सेलुलर apoptosis (आनुवंशिक रूप से निर्धारित आत्म-विनाश) और मैट्रिक्स पुटिका गठन के साथ होता है। कैल्शियम-लोडिंग से फॉस्फेटीडाइलसिरिन का निर्माण भी होता है: कैल्शियम: प्लाज्मा झिल्ली में फॉस्फेट परिसरों को उपांग नामक प्रोटीन द्वारा मध्यस्थ किया जाता है। बाह्य मैट्रिक्स के साथ संपर्क के स्थलों पर प्लाज्मा झिल्ली से मैट्रिक्स पुटिकाएं निकलती हैं। इस प्रकार, मैट्रिक्स वेसिकल्स बाह्य मैट्रिक्स कैल्शियम, फॉस्फेट, लिपिड और एनेक्सिन को व्यक्त करते हैं जो न्यूक्लियेट खनिज गठन के लिए कार्य करते हैं। जब तक गोल्गी उपस्थित न हो, तब तक ऊतक के मैट्रिक्स के खनिजीकरण को उचित स्थान और समय पर लाने के लिए इन प्रक्रियाओं को सटीक रूप से समन्वित किया जाता है।
इंडोसोम , या एमवीबी, झिल्ली-बद्ध पुटिका है जिसमें अनेक छोटे पुटिका होते हैं।
गठन और परिवहन
| Cell biology | |
|---|---|
| Animal cell diagram | |
 Components of a typical animal cell:
|
कुछ पुटिकाएं तब बनती हैं जब झिल्ली का भाग एंडोप्लाज्मिक रेटिकुलम या गोल्गी कॉम्प्लेक्स को बंद कर देता है। अन्य तब बनते हैं जब कोशिका के बाहर कोई वस्तु कोशिका झिल्ली से घिरी होती है।
वेसिकल कोट और कार्गो अणु
पुटिका कोट प्रोटीन का संग्रह है जो दाता झिल्ली की वक्रता को आकार देने के लिए काम करता है, जिससे गोल पुटिका का आकार बनता है। कोट प्रोटीन कार्गो रिसेप्टर्स कहे जाने वाले विभिन्न ट्रांसमेम्ब्रेन रिसेप्टर प्रोटीन को बाँधने का कार्य कर सकता है। ये रिसेप्टर्स यह चुनने में मदद करते हैं कि रिसेप्टर-मध्यस्थता वाले एंडोसाइटोसिस या इंट्रासेल्युलर ट्रांसपोर्ट में कौन सी सामग्री एंडोसाइटोज्ड है।
पुटिका कोट तीन प्रकार के होते हैं: क्लैथ्रिन, COPI और COPII। विभिन्न प्रकार के कोट प्रोटीन पुटिकाओं को उनके अंतिम गंतव्य तक छांटने में मदद करते हैं। क्लैथ्रिन कोट गोल्गी उपकरण और प्लाज्मा झिल्ली, गोल्गी और एंडोसोम और प्लाज्मा झिल्ली और एंडोसोम के मध्य तस्करी करने वाले पुटिकाओं पर पाए जाते हैं। COPI कोटेड वेसिकल्स, Golgi से ER तक रेट्रोग्रेड ट्रांसपोर्ट के लिए जिम्मेदार होते हैं, जबकि COPII कोटेड वेसिकल्स ER से Golgi तक एथेरोग्रेड ट्रांसपोर्ट के लिए जिम्मेदार होते हैं।
माना जाता है कि नियामक जी प्रोटीन के जवाब में क्लैथ्रिन कोट इकट्ठा होता है। एडीपी राइबोसाइलेशन कारक (ARF) प्रोटीन के कारण प्रोटीन कोट असेंबल और डिसअसेंबल होता है।
वेसिकल डॉकिंग
SNAREs नामक भूतल प्रोटीन पुटिका के कार्गो की पहचान करते हैं और लक्ष्य झिल्ली पर पूरक SNAREs पुटिका और लक्ष्य झिल्ली के संलयन का कारण बनते हैं। इस तरह के v-SNARES को पुटिका झिल्ली पर उपस्थित होने की परिकल्पना की जाती है, जबकि लक्ष्य झिल्ली पर पूरक को t-SNAREs के रूप में जाना जाता है।
प्रायः पुटिकाओं या लक्ष्य झिल्लियों से जुड़े SNAREs को केवल v- या t-SNAREs की तुलना में अधिक भिन्नता के कारण Qa, Qb, Qc, या R SNAREs के रूप में वर्गीकृत किया जाता है। विभिन्न SNARE परिसरों की सरणी विभिन्न ऊतकों और उपकोशिकीय डिब्बों में देखी जा सकती है, जिसमें वर्तमान में मनुष्यों में पहचाने जाने वाले 36 आइसोफॉर्म हैं।
विनियामक रब (ग-प्रोटीन) प्रोटीन को SNAREs के सम्मिलित होने का निरीक्षण करने के लिए माना जाता है। रब प्रोटीन नियामक जीटीपी-बाध्यकारी प्रोटीन है और रब प्रोटीन के लिए अपने बाध्य जीटीपी को हाइड्रोलाइज करने और झिल्ली पर पुटिका को बंद करने के लिए लंबे समय तक इन पूरक जालों के बंधन को नियंत्रित करता है।
कवक और जानवरों की तुलना में पौधों में SNAREs को समझा जाता है। सेल वनस्पतिशास्त्री नताशा रीचेल ने इस क्षेत्र में कुछ बुनियादी शोध किए हैं, जिसमें झेंग और अन्य 1999 सम्मिलित हैं, जिसमें उन्होंने और उनकी टीम ने AtVTI1a को Golgi उपकरण⇄वैक्यूल परिवहन के लिए आवश्यक पाया।[21]
वेसिकल फ्यूजन
वेसिकल फ्यूजन दो तरीकों में से में हो सकता है: फुल फ्यूजन या किस-एंड-रन फ्यूजन। संलयन के लिए दो झिल्लियों को दूसरे के 1.5 एनएम के अंदर लाने की आवश्यकता होती है। ऐसा होने के लिए पानी को पुटिका झिल्ली की सतह से विस्थापित किया जाना चाहिए। यह ऊर्जावान रूप से प्रतिकूल है और साक्ष्य बताते हैं कि इस प्रक्रिया के लिए एडेनोसाइन ट्रायफ़ोस्फेट, गुआनोसिन ट्राइफॉस्फेट और एसिटाइल कोआ की आवश्यकता होती है। फ्यूजन भी नवोदित से जुड़ा हुआ है, यही वजह है कि नवोदित और फ्यूजिंग शब्द उत्पन्न होता है।
रिसेप्टर डाउनरेगुलेशन में
रिसेप्टर (जैव रसायन) के रूप में काम करने वाले मेम्ब्रेन प्रोटीन को कभी-कभी ubiquitin के अटैचमेंट द्वारा डाउनरेगुलेशन के लिए टैग किया जाता है। ऊपर वर्णित मार्ग के माध्यम से एंडोसोम पहुंचने के बाद, एंडोसोम के अंदर पुटिकाओं का निर्माण शुरू हो जाता है, उनके साथ गिरावट के लिए झिल्ली प्रोटीन ले जाते हैं; जब एंडोसोम या तो लाइसोसोम बनने के लिए परिपक्व हो जाता है या के साथ जुड़ जाता है, तो वेसिकल्स पूरी तरह से ख़राब हो जाते हैं। इस तंत्र के बिना, झिल्ली प्रोटीन का केवल बाह्य भाग लाइसोसोम के लुमेन तक पहुंचेगा और केवल इस भाग का क्षरण होगा।[22] यह इन पुटिकाओं के कारण है कि एंडोसोम को कभी-कभी बहुकोशिकीय शरीर के रूप में जाना जाता है। उनके गठन का मार्ग पूरी तरह से समझा नहीं गया है; ऊपर वर्णित अन्य पुटिकाओं के विपरीत, पुटिकाओं की बाहरी सतह साइटोसोल के संपर्क में नहीं है।
तैयारी
पृथक पुटिका
कोशिका की विभिन्न झिल्लियों की परीक्षण करने के लिए झिल्ली पुटिकाओं का निर्माण विधि है। जीवित ऊतक को निलंबन (रसायन) में कुचलने के बाद, विभिन्न झिल्लियां छोटे बंद बुलबुले बनाती हैं। कुचली हुई कोशिकाओं के बड़े टुकड़ों को कम गति के सेंट्रीफ्यूगेशन द्वारा भिन्न किया जा सकता है और बाद में ज्ञात मूल (plasmalemma , tonoplast , आदि) के अंश को घनत्व प्रवणता में सटीक उच्च गति सेंट्रीफ्यूगेशन द्वारा भिन्न किया जा सकता है। आसमाटिक झटका का उपयोग करके, अस्थायी रूप से पुटिकाओं को खोलना (उन्हें आवश्यक समाधान के साथ भरना) संभव है और फिर फिर से सेंट्रीफ्यूगेट करें और भिन्न समाधान में पुन: निलंबित करें। वैलिनोमाइसिन जैसे आयनोफोरस को लागू करने से जीवित कोशिकाओं के अंदर के ग्रेडिएंट्स की तुलना में इलेक्ट्रोकेमिकल ग्रेडिएंट्स बन सकते हैं।
Vesicles मुख्य रूप से दो प्रकार के शोधों में उपयोग किए जाते हैं:
- झिल्ली रिसेप्टर्स को खोजने और बाद में भिन्न करने के लिए जो विशेष रूप से हार्मोन और अन्य महत्वपूर्ण पदार्थों को बांधते हैं।[23]
- दिए गए प्रकार की झिल्ली के पार विभिन्न आयनों या अन्य पदार्थों के परिवहन की परीक्षण करना।[24] जबकि पैच दबाना प्रौद्योगिकी के साथ परिवहन की अधिक सरलता से परीक्षण की जा सकती है, पुटिकाओं को उन वस्तुओं से भी भिन्न किया जा सकता है जिनके लिए पैच क्लैंप लागू नहीं होता है।
कृत्रिम वेसिकल्स
कृत्रिम वेसिकल्स को उनके आकार के आधार पर तीन समूहों में वर्गीकृत किया गया है: 20–100 एनएम के आकार की सीमा के साथ छोटे यूनीमेलर लिपोसोम्स/वेसिकल्स (एसयूवी), 100–1000 एनएम के आकार की सीमा के साथ बड़े यूनीमेलर लिपोसोम्स/वेसिकल्स (एलयूवी) और विशाल यूनीमेलर लाइपोसोम/वेसिकल्स (जीयूवी) जिनका आकार 1–200 माइक्रोमीटर होता है।[25] जीवित कोशिकाओं में पाए जाने वाले ट्रैफिकिंग वेसिकल्स के समान आकार की छोटी पुटिकाएं प्रायः जैव रसायन और संबंधित क्षेत्रों में उपयोग की जाती हैं। ऐसे अध्ययनों के लिए, एक्सट्रूज़न याsonication द्वारा सजातीय फॉस्फोलिपिड पुटिका निलंबन तैयार किया जा सकता है,[26] या जलीय बफर समाधान में फॉस्फोलिपिड समाधान के तेजी से इंजेक्शन द्वारा।[27] इस तरह, विभिन्न फॉस्फोलिपिड संरचना के साथ-साथ विभिन्न आकार के पुटिकाओं के जलीय पुटिका समाधान तैयार किए जा सकते हैं। कोशिका झिल्लियों की नकल करने के लिए कोशिका जीव विज्ञान में इन विट्रो अध्ययनों के लिए GUVs जैसे बड़े कृत्रिम रूप से बने पुटिकाओं का उपयोग किया जाता है। पारंपरिक प्रतिदीप्ति प्रकाश माइक्रोस्कोपी का उपयोग करके इन पुटिकाओं का अध्ययन किया जाना काफी बड़ा है। इस तरह के पुटिकाओं के अंदर प्रोटीन समाधान जैसे जैविक अभिकारकों को समाहित करने के लिए अनेक तरह के तरीके उपस्थित हैं, जो GUVs को सेल-जैसे मॉडल झिल्ली वातावरण में सेल फ़ंक्शंस के इन विट्रो रिक्रिएशन (और जांच) के लिए आदर्श प्रणाली बनाते हैं।[28] इन विधियों में माइक्रोफ्लुइडिक विधियाँ सम्मिलित हैं, जो लगातार आकार वाले पुटिकाओं के उच्च-उपज उत्पादन की अनुमति देती हैं।[29]
यह भी देखें
- ब्लीब (कोशिका जीव विज्ञान)
- मेजबान-रोगज़नक़ इंटरफ़ेस
- झिल्ली संपर्क साइट
- झिल्ली नैनोट्यूब
- मेम्ब्रेन वेसिकल ट्रैफिकिंग
- मिसेल
- माइक्रोसोम
- प्रोटोसेल
- स्पिट्ज़ेंकोर्पर, कवक तंतु में पाए जाने वाले कई छोटे पुटिकाओं की एक संरचना
संदर्भ
- ↑ Akbarzadeh A, Rezaei-Sadabady R, Davaran S, Joo SW, Zarghami N, Hanifehpour Y, Samiei M, Kouhi M, Nejati-Koshki K (February 2013). "Liposome: classification, preparation, and applications". Nanoscale Res Lett. 8 (1): 102. Bibcode:2013NRL.....8..102A. doi:10.1186/1556-276X-8-102. PMC 3599573. PMID 23432972.
- ↑ 2.0 2.1 Walsby AE (March 1994). "गैस पुटिका". Microbiological Reviews. 58 (1): 94–144. doi:10.1128/mmbr.58.1.94-144.1994. PMC 372955. PMID 8177173.
- ↑ Slomkowski S, Alemán JV, Gilbert RG, Hess M, Horie K, Jones RG, et al. (2011). "Terminology of polymers and polymerization processes in dispersed systems (IUPAC Recommendations 2011)" (PDF). Pure and Applied Chemistry. 83 (12): 2229–2259. doi:10.1351/PAC-REC-10-06-03. S2CID 96812603.
- ↑ "Nobel medical prize goes to 2 Americans, 1 German". CNN. 2005-10-19. Retrieved 2013-10-09.
- ↑ 2013 Nobel Prize in Physiology or Medicine, press release 2013-10-07
- ↑ Deatherage BL, Cookson BT (June 2012). "Membrane vesicle release in bacteria, eukaryotes, and archaea: a conserved yet underappreciated aspect of microbial life". Infection and Immunity. 80 (6): 1948–57. doi:10.1128/IAI.06014-11. PMC 3370574. PMID 22409932.
- ↑ Yáñez-Mó M, Siljander PR, Andreu Z, Zavec AB, Borràs FE, Buzas EI, et al. (2015). "बाह्य पुटिकाओं के जैविक गुण और उनके शारीरिक कार्य". Journal of Extracellular Vesicles. 4: 27066. doi:10.3402/jev.v4.27066. PMC 4433489. PMID 25979354.
- ↑ 8.0 8.1 Théry C, Witwer KW, Aikawa E, Alcaraz MJ, Anderson JD, Andriantsitohaina R, et al. (2018). "Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines". Journal of Extracellular Vesicles. 7 (1): 1535750. doi:10.1080/20013078.2018.1535750. PMC 6322352. PMID 30637094.
- ↑ 9.0 9.1 9.2 9.3 9.4 van der Pol E, Böing AN, Harrison P, Sturk A, Nieuwland R (July 2012). "बाह्य पुटिकाओं का वर्गीकरण, कार्य और नैदानिक प्रासंगिकता". Pharmacological Reviews. 64 (3): 676–705. doi:10.1124/pr.112.005983. PMID 22722893. S2CID 7764903.
{{cite journal}}: zero width space character in|title=at position 46 (help) Free full text - ↑ van der Pol E, Böing AN, Gool EL, Nieuwland R (January 2016). "बाह्य पुटिकाओं के नामकरण, उपस्थिति, अलगाव, पता लगाने और नैदानिक प्रभाव में हाल के विकास". Journal of Thrombosis and Haemostasis. 14 (1): 48–56. doi:10.1111/jth.13190. PMID 26564379.
{{cite journal}}: zero width space character in|title=at position 65 (help) - ↑ Melentijevic I, Toth ML, Arnold ML, Guasp RJ, Harinath G, Nguyen KC, et al. (February 2017). "सी। एलिगेंस न्यूरॉन्स जेटीसन प्रोटीन समुच्चय और माइटोकॉन्ड्रिया न्यूरोटॉक्सिक तनाव के तहत". Nature. 542 (7641): 367–371. Bibcode:2017Natur.542..367M. doi:10.1038/nature21362. PMC 5336134. PMID 28178240.
- ↑ Mateescu B, Kowal EJ, van Balkom BW, Bartel S, Bhattacharyya SN, Buzás EI, et al. (2017). "बाह्य पुटिका आरएनए के कार्यात्मक विश्लेषण में बाधाएं और अवसर - एक आईएसईवी स्थिति पत्र". Journal of Extracellular Vesicles. 6 (1): 1286095. doi:10.1080/20013078.2017.1286095. PMC 5345583. PMID 28326170.
- ↑ Dhondt B, Rousseau Q, De Wever O, Hendrix A (September 2016). "मेटास्टेसिस में बाह्य पुटिका से जुड़े miRNAs का कार्य". Cell and Tissue Research. 365 (3): 621–41. doi:10.1007/s00441-016-2430-x. hdl:1854/LU-7250365. PMID 27289232. S2CID 2746182.
- ↑ Dhondt B, Van Deun J, Vermaerke S, de Marco A, Lumen N, De Wever O, Hendrix A (June 2018). "Urinary extracellular vesicle biomarkers in urological cancers: From discovery towards clinical implementation". The International Journal of Biochemistry & Cell Biology. 99: 236–256. doi:10.1016/j.biocel.2018.04.009. hdl:1854/LU-8559155. PMID 29654900. S2CID 4876604.
- ↑ Teixeira FG, Carvalho MM, Sousa N, Salgado AJ (October 2013). "Mesenchymal stem cells secretome: a new paradigm for central nervous system regeneration?". Cellular and Molecular Life Sciences. 70 (20): 3871–82. doi:10.1007/s00018-013-1290-8. hdl:1822/25128. PMID 23456256. S2CID 18640402.
- ↑ Kuehn MJ, Kesty NC (November 2005). "बैक्टीरियल बाहरी झिल्ली पुटिका और मेजबान-रोगज़नक़ बातचीत". Genes & Development. 19 (22): 2645–55. doi:10.1101/gad.1299905. PMID 16291643.
- ↑ Biller SJ, Schubotz F, Roggensack SE, Thompson AW, Summons RE, Chisholm SW (January 2014). "समुद्री पारिस्थितिक तंत्र में जीवाणु पुटिकाएँ". Science. 343 (6167): 183–6. Bibcode:2014Sci...343..183B. doi:10.1126/science.1243457. hdl:1721.1/84545. PMID 24408433. S2CID 206551356.
- ↑ Pfeifer F (October 2012). "गैस पुटिकाओं का वितरण, निर्माण और नियमन". Nature Reviews. Microbiology. 10 (10): 705–15. doi:10.1038/nrmicro2834. PMID 22941504. S2CID 9926129.
- ↑ Anderson HC (October 1967). "प्रेरित उपास्थि विकास और कैल्सीफिकेशन का इलेक्ट्रॉन सूक्ष्म अध्ययन". The Journal of Cell Biology. 35 (1): 81–101. doi:10.1083/jcb.35.1.81. PMC 2107116. PMID 6061727.
- ↑ Bonucci E (September 1967). "प्रारंभिक उपास्थि कैल्सीफिकेशन की ठीक संरचना". Journal of Ultrastructure Research. 20 (1): 33–50. doi:10.1016/S0022-5320(67)80034-0. PMID 4195919.
- ↑ Raikhel, Natasha V. (2017-04-28). "मजबूती से लगा हुआ, हमेशा चलता रहता है". Annual Review of Plant Biology. Annual Reviews. 68 (1): 1–27. doi:10.1146/annurev-arplant-042916-040829. ISSN 1543-5008. PMID 27860488.
- ↑ Katzmann DJ, Odorizzi G, Emr SD (December 2002). "रिसेप्टर डाउनरेगुलेशन और मल्टीविस्कुलर-बॉडी सॉर्टिंग". Nature Reviews. Molecular Cell Biology. 3 (12): 893–905. doi:10.1038/nrm973. PMID 12461556. S2CID 1344520.
- ↑ Sidhu VK, Vorhölter FJ, Niehaus K, Watt SA (June 2008). "पौधे के रोगजनक जीवाणु ज़ैंथोमोनस कैंपेस्ट्रिस पीवी से पृथक बाहरी झिल्ली पुटिका से जुड़े प्रोटीन का विश्लेषण। campestris". BMC Microbiology. 8: 87. doi:10.1186/1471-2180-8-87. PMC 2438364. PMID 18518965.
- ↑ Scherer GG, Martiny-Baron G (1985). "K+/H+ exchange transport in plantmembranevesicles is evidence for K+ transport". Plant Science. 41 (3): 161–8. doi:10.1016/0168-9452(85)90083-4.
- ↑ Walde P, Cosentino K, Engel H, Stano P (May 2010). "Giant vesicles: preparations and applications". ChemBioChem. 11 (7): 848–65. doi:10.1002/cbic.201000010. PMID 20336703. S2CID 30723166.
- ↑ Barenholz Y, Gibbes D, Litman BJ, Goll J, Thompson TE, Carlson RD (June 1977). "सजातीय फॉस्फोलिपिड पुटिकाओं की तैयारी के लिए एक सरल विधि". Biochemistry. 16 (12): 2806–10. doi:10.1021/bi00631a035. PMID 889789.
- ↑ Batzri S, Korn ED (April 1973). "सिंगल बाइलेयर लिपोसोम बिना सोनिकेशन के तैयार किए गए". Biochimica et Biophysica Acta (BBA) - Biomembranes. 298 (4): 1015–9. doi:10.1016/0005-2736(73)90408-2. PMID 4738145.
- ↑ Litschel T, Schwille P (March 2021). "जायंट यूनीमेलर वेसिकल्स के अंदर प्रोटीन का पुनर्गठन". Annual Review of Biophysics. 50: 525–548. doi:10.1146/annurev-biophys-100620-114132. PMID 33667121. S2CID 232131463.
- ↑ Sato Y, Takinoue M (March 2019). "माइक्रोफ्लुइडिक्स टेक्नोलॉजीज द्वारा प्रवर्तित कृत्रिम कोशिका जैसी संरचनाओं का निर्माण". Micromachines. 10 (4): 216. doi:10.3390/mi10040216. PMC 6523379. PMID 30934758.
अग्रिम पठन
- Alberts, Bruce; et al. (1998). Essential Cell Biology: An Introduction to the Molecular Biology of the Cell. Garland Pub. ISBN 978-0-8153-2971-8.
